Clear Sky Science · it
Forze silenziose, correnti nascoste: l'influsso della stimolazione con campo magnetico statico sulla biofisica tumorale
Aiutanti nascosti nella lotta contro il cancro
I trattamenti oncologici moderni come chemioterapia e radioterapia possono salvare vite, ma spesso comportano effetti collaterali pesanti. Questa rassegna esplora un'alternativa intrigante: l'uso di campi magnetici stazionari, non pulsati — simili per principio a quelli presenti negli scanner MRI — come modo delicato per spingere e sollecitare le cellule tumorali. Modificando sottilmente il movimento, la divisione e la gestione energetica delle cellule cancerose, i campi magnetici statici potrebbero un giorno diventare un partner a basso costo e non invasivo alle terapie esistenti.
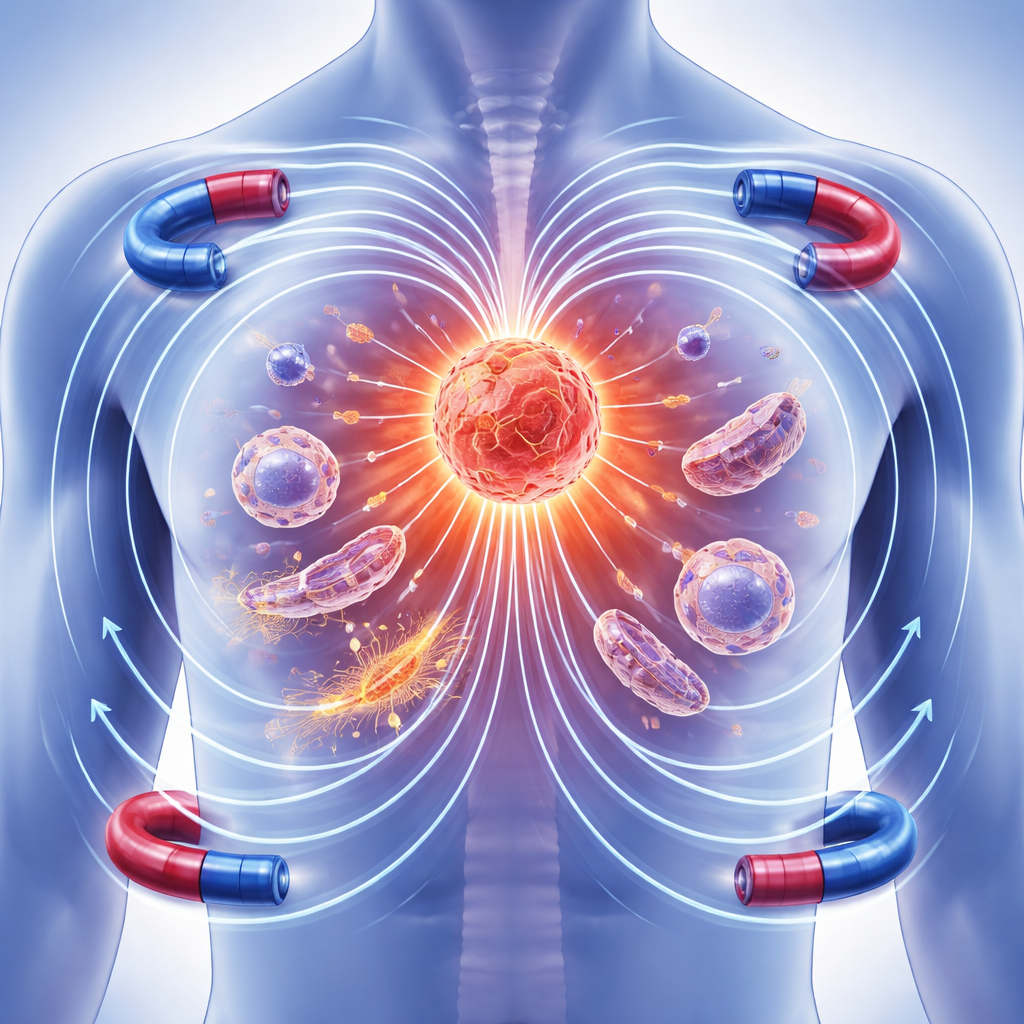
Come il magnetismo immobile può muovere le cellule viventi
Di solito immaginiamo i magneti come attirati dai metalli, ma all'interno del corpo agiscono su particelle cariche e su molecole. Gli autori descrivono tre principali modalità con cui i campi magnetici statici possono influenzare le cellule. Primo, particelle cariche in movimento come gli ioni avvertono una spinta laterale chiamata forza di Lorentz, che può alterare leggermente le loro traiettorie. Secondo, molte strutture cellulari — come fibre proteiche e membrane — sono debolmente respinte o allineate dai campi magnetici e possono ruotare per disporsi in fila, come tronchi in una corrente lenta. Terzo, i magneti possono modificare il comportamento delle cosiddette “coppie radicaliche”, specie chimiche reattive a vita breve che contribuiscono a regolare lo stress ossidativo cellulare. Insieme, questi effetti possono rimodellare l'architettura cellulare, l'uso di energia e la segnalazione.
Colpire l'impalcatura, la membrana e lo scheletro del tumore
All'interno dei tumori, è stato dimostrato che i campi magnetici statici riallineano le fibre di collagene — l'impalcatura proteica a cui le cellule tumorali si aggrappano — così che sia le fibre sia le cellule vicine cambiano orientamento. Anche le membrane cellulari, comprese quelle delle piccole centrali energetiche chiamate mitocondri, rispondono: i canali ionici possono aprirsi o chiudersi più lentamente, il potenziale di membrana può spostarsi e il flusso di calcio nelle cellule può aumentare o diminuire. Più in profondità nella cellula, lo scheletro strutturale composto da microtubuli e filamenti di actina può riorientarsi o disassemblarsi sotto campi intensi, perturbando la separazione ordinata dei cromosomi durante la divisione cellulare. In molti esperimenti questi cambiamenti rallentano la proliferazione delle cellule tumorali, attivano programmi di morte cellulare o rendono le cellule meno capaci di migrare e invadere.
Aumentare la pressione ossidativa e danneggiare il DNA tumorale
Un altro effetto importante dei campi magnetici statici riguarda le specie reattive dell'ossigeno — forme chimiche reattive dell'ossigeno che possono indurre adattamenti cellulari oppure, a livelli elevati, spingere le cellule verso la morte. In molti tipi di cellule tumorali, l'esposizione a campi di intensità moderata o elevata aumenta queste molecole reattive o depleta gli antiossidanti che normalmente le neutralizzano. Questa pressione ossidativa può danneggiare il DNA, accorciare le estremità protettive dei cromosomi chiamate telomeri e bloccare la replicazione del DNA, determinando arresti in fasi sensibili del ciclo cellulare. Tuttavia la risposta non è uniforme: in alcuni contesti o a certe intensità, l'esposizione magnetica riduce lo stress ossidativo e in realtà favorisce la crescita tumorale, sottolineando quanto sia importante calibrare con precisione le condizioni.
Operare fianco a fianco con farmaci e radiazioni
Poiché i tumori sono già sotto stress da chemioterapia e radioterapia, l'aggiunta di un campo magnetico statico può spostare l'equilibrio verso la morte delle cellule cancerose. Gli studi mostrano che tali campi possono rendere le membrane cellulari più permeabili, aumentando l'assorbimento di farmaci come cisplatino, doxorubicina e paclitaxel. Possono anche accentuare il danno ossidativo indotto dai farmaci, disturbare i microtubuli che molti farmaci già prendono di mira e favorire l'arresto del ciclo cellulare. Negli animali, magneti orientati con cura posti vicino ai tumori hanno ridotto la crescita e, se associati ai farmaci, hanno permesso di usare dosi inferiori ottenendo un controllo tumorale simile o migliore, talvolta con meno effetti collaterali. Tuttavia la direzione del campo, l'intensità, la durata dell'esposizione e persino la densità cellulare tumorale influenzano fortemente i risultati, e in alcuni casi i magneti sembrano attenuare i benefici del trattamento.
Prospettive, insidie e la strada verso terapie reali
Per le cellule non cancerose e per gli animali interi, i campi magnetici statici fino e oltre le intensità della risonanza magnetica appaiono generalmente sicuri negli studi a breve termine, sebbene alcuni tipi cellulari mostrino crescita rallentata mentre altri crescono più rapidamente o si riorientano nel campo. La rassegna conclude che i campi magnetici statici non sono una soluzione miracolosa ma uno strumento sottile: nelle condizioni giuste possono mettere sotto stress le impalcature tumorali, scombussolare la divisione cellulare e amplificare il danno ossidativo, specialmente se combinati con farmaci standard o raggi X. Per trasformare queste “forze silenziose” in terapie oncologiche affidabili, i ricercatori devono tracciare quali intensità, direzioni e schemi di esposizione danneggiano selettivamente i tumori risparmiando i tessuti sani, e devono standardizzare il modo in cui tali esperimenti vengono riportati in modo che i risultati promettenti in laboratorio possano essere tradotti in trial clinici progettati con cura.
Citazione: Verma, P., Varshney, A., Lais, M. et al. Silent forces, hidden currents: the influence of static magnetic field stimulation on tumor biophysics. npj Biomed. Innov. 3, 19 (2026). https://doi.org/10.1038/s44385-026-00071-z
Parole chiave: campi magnetici statici, biofisica del cancro, specie reattive dell'ossigeno, terapia combinata, microambiente tumorale