Clear Sky Science · it
Ottimizzare l’induzione dell’infiammazione in organoidi dell’epitelio intestinale derivati da neonati pretermine
Perché questo è importante per i neonati fragili
I neonati nati molto precocemente affrontano una combinazione pericolosa: un intestino immaturo e una comunità microbica in rapida evoluzione. Insieme possono innescare un’infiammazione incontrollata che danneggia l’intestino e porta a condizioni potenzialmente fatali come l’enterocolite necrotizzante. Poiché non è possibile sperimentare direttamente sui neonati pretermine, gli scienziati hanno bisogno di modelli di laboratorio realistici del loro intestino per testare cosa guida l’infiammazione e come fermarla. Questo studio affina un tale modello utilizzando piccoli tessuti intestinali coltivati in laboratorio, offrendo un modo più chiaro per indagare quali segnali microbici fanno pendere l’equilibrio da una difesa normale a un’infiammazione dannosa.
Far crescere un intestino pretermine in una piastra
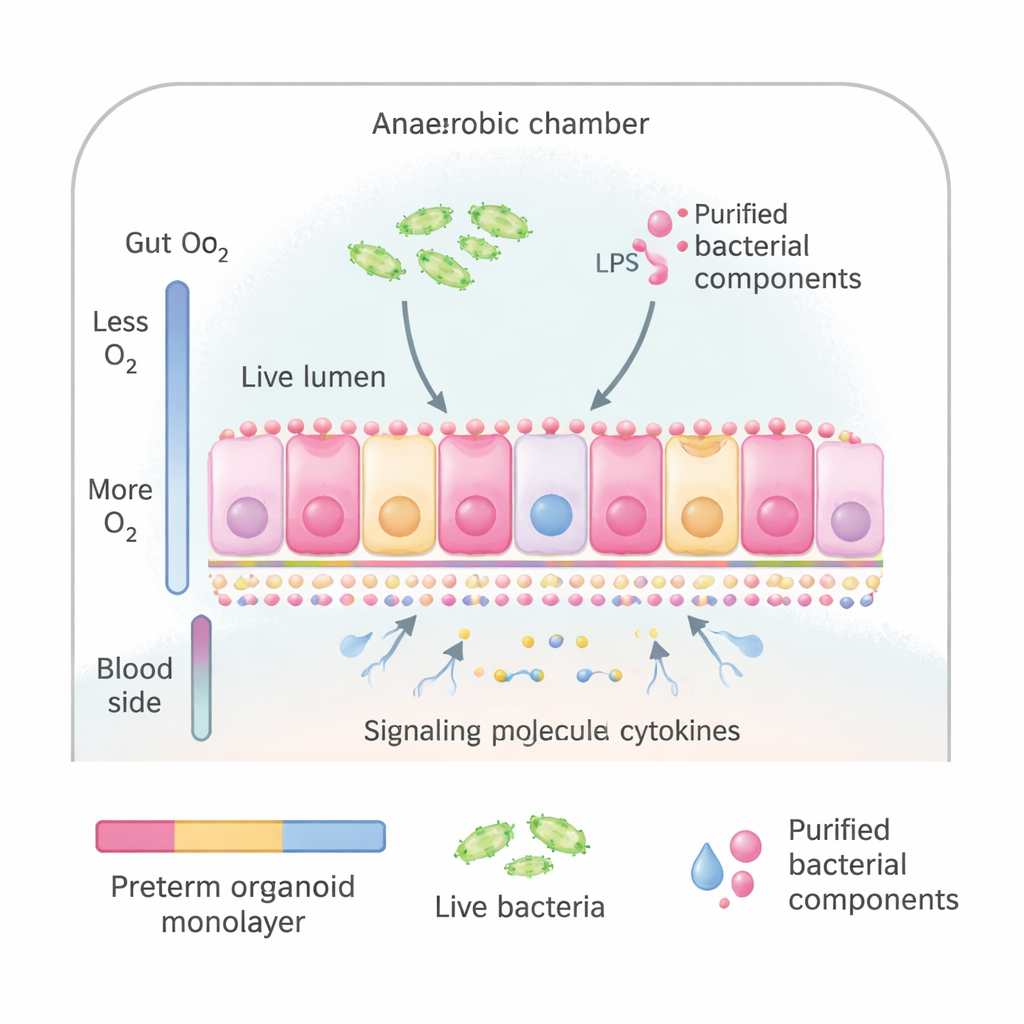
I ricercatori hanno utilizzato organoidi intestinali—versioni in miniatura della mucosa intestinale coltivate da cellule staminali prelevate da neonati pretermine durante interventi chirurgici. Questi organoidi possono essere appiattiti in un sottile foglio di cellule che somiglia e si comporta molto come la superficie interna dell’intestino tenue, compresa la corretta polarità (la parte superiore rivolta verso il contenuto intestinale e quella inferiore rivolta verso il flusso sanguigno). Il gruppo ha collocato questi fogli in un sistema di coltura speciale che imita il naturale gradiente di ossigeno dell’intestino: bassa ossigenazione sul lato rivolto ai microbi e ossigenazione maggiore sul lato sanguigno. Questo ha permesso di esporre la «superficie intestinale» sia a batteri interi prelevati da neonati pretermine sia a componenti batteriche purificate note per attivare il sistema immunitario.
Testare cosa scatena meglio l’allarme infiammatorio
Gli scienziati hanno confrontato diverse modalità di provocare l’infiammazione: un mix di batteri vivi comunemente riscontrati in neonati pretermine malati; gli stessi batteri inattivati con il calore; e due segnali batterici purificati, il lipopolisaccaride (LPS) dalle pareti cellulari batteriche e la flagellina dalle code batteriche. Hanno misurato il rilascio di IL‑8, una proteina segnale che attrae cellule immunitarie e funge da marcatore generale di infiammazione, e hanno utilizzato analisi proteiche su larga scala per vedere come cambiava il funzionamento interno delle cellule intestinali. Sorprendentemente, batteri vivi o morti non aumentarono fortemente l’IL‑8 in questo sistema, neppure dopo 24 ore. Al contrario, la flagellina e in particolare la combinazione di flagellina e LPS provocarono un chiaro aumento di IL‑8 già dopo sole tre ore, mostrando che questi segnali purificati potevano attivare in modo affidabile uno stato infiammatorio.
Trovare l’allestimento più realistico ed efficiente
Per meglio corrispondere alla biologia intestinale reale, il gruppo si è quindi concentrato su dove ciascun segnale agisce naturalmente. LPS è solitamente percepito sul lato della mucosa rivolto verso il lume intestinale, mentre la flagellina viene principalmente rilevata dal lato tissutale. Usando dosi molto più basse, più fisiologiche rispetto a esperimenti precedenti, hanno applicato LPS sulla parte superiore (rivolta al lume) e la flagellina sul lato inferiore (rivolta al sangue) del foglio di organoide. Questo semplice cambiamento ha prodotto una risposta forte e ampia entro tre ore: molte molecole infiammatorie—including IL‑8, TNF e diversi chemochine—sono state secrete da entrambi i lati del tessuto. Allo stesso tempo, centinaia di proteine cellulari variarono in abbondanza, indicando un’attivazione su larga scala delle vie di difesa.
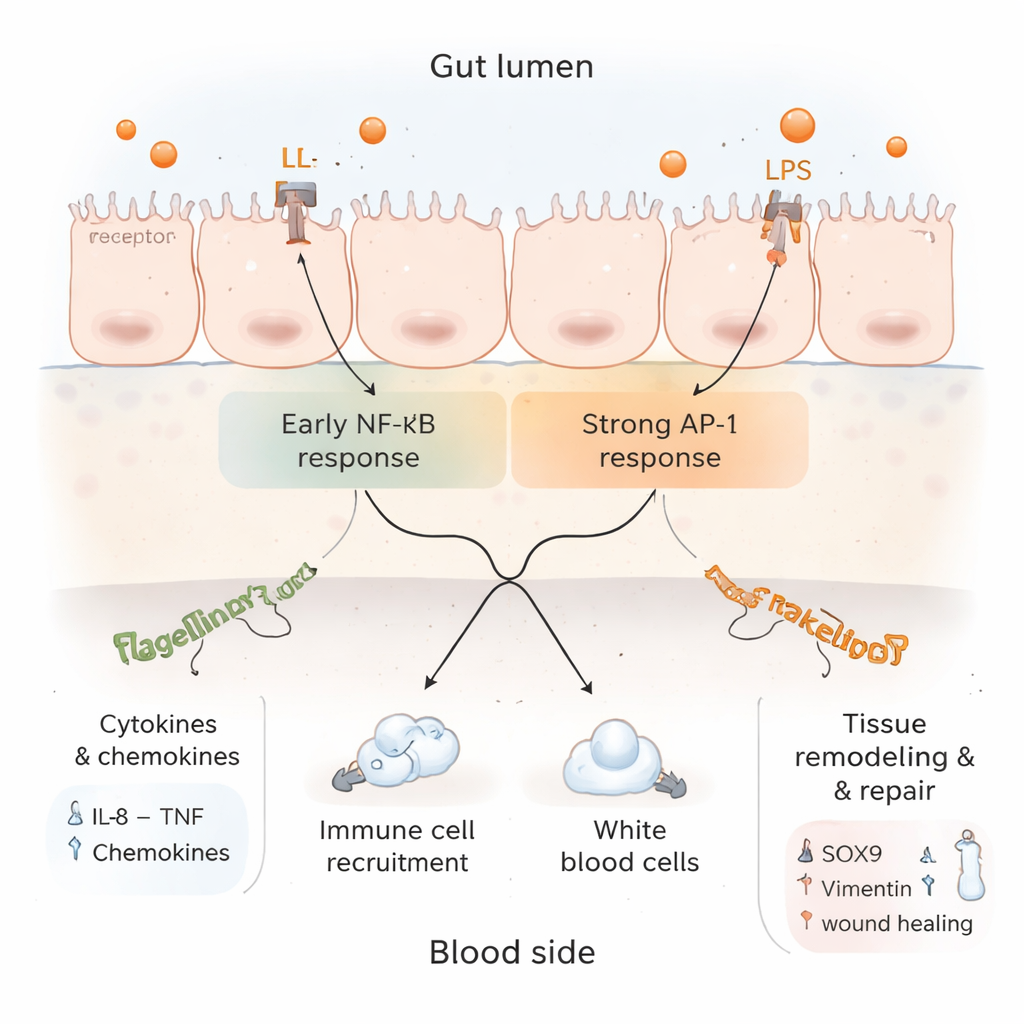
Infiammazione, freni e riparazione nello stesso modello
Approfondendo i dati proteici, i ricercatori hanno trovato un quadro complesso. Da un lato, sono aumentati i marcatori di infiammazione attiva e reclutamento di cellule immunitarie, e sono state attivate vie di segnalazione legate a TNF e IL‑17—entrambe centrali per la difesa immunitaria intestinale. Dall’altro, diversi componenti della classica via NF‑κB, che guida molti geni infiammatori, sono stati modulati al ribasso, mentre una via alternativa che coinvolge AP‑1 è rimasta attiva. Ciò suggerisce che dopo un allarme iniziale il tessuto inizia ad applicare freni per prevenire danni incontrollati. Contemporaneamente, sono aumentate proteine associate alla rigenerazione tissutale, al rimodellamento strutturale e a una morte cellulare regolata, suggerendo che l’epitelio intestinale non era solo infiammato ma stava anche tentando di rimodellarsi e ripararsi.
Cosa significa per i trattamenti futuri
Confrontando in modo sistematico diversi stimoli microbici, dosi, posizioni e tempi di esposizione, gli autori concludono che un’esposizione di tre ore a LPS a bassa dose sul lato intestinale insieme a flagellina sul lato sanguigno è il modo più solido e riproducibile per indurre infiammazione in organoidi intestinali derivati da pretermine. Questo modello perfezionato cattura non solo l’esplosione infiammatoria, ma anche i freni intrinseci, i meccanismi di tolleranza e le risposte di riparazione dell’intestino fragile del pretermine. Fornisce un progetto pratico per altri laboratori per studiare come specifici microbi, farmaci o fattori nutrizionali possano peggiorare o calmare l’infiammazione intestinale nei neonati molto prematuri—un passo essenziale verso strategie mirate e più sicure per prevenire malattie intestinali devastanti in questo gruppo vulnerabile.
Citazione: Chapman, J.A., Frey, A.M., Dueñas, M.E. et al. Optimising the induction of inflammation within preterm infant-derived intestinal epithelial organoids. npj Gut Liver 3, 5 (2026). https://doi.org/10.1038/s44355-026-00054-2
Parole chiave: intestino del neonato pretermine, organoidi intestinali, infiammazione intestinale, microbioma, enterocolite necrotizzante