Clear Sky Science · it
Trasduzione chemomeccanica non in equilibrio dello svolgimento proteico guidato da ATP nel proteasoma 26S
Come una piccola macchina mantiene ordinate le nostre proteine
All’interno di ogni cellula, un trituratore microscopico chiamato proteasoma 26S distrugge costantemente proteine danneggiate o non più necessarie, mantenendo la cellula in salute. Al centro di questa macchina c’è un motore ad anello che brucia carburante chimico (ATP) per afferrare, districare e tirare le proteine in una camera centrale dove vengono scomposte. Questo articolo utilizza simulazioni al computer avanzate per rivelare come quel motore converta energia chimica in moto meccanico, offrendo un quadro dettagliato e quantitativo di un processo che sta alla base dell’invecchiamento, delle malattie cerebrali, dell’immunità e del cancro.
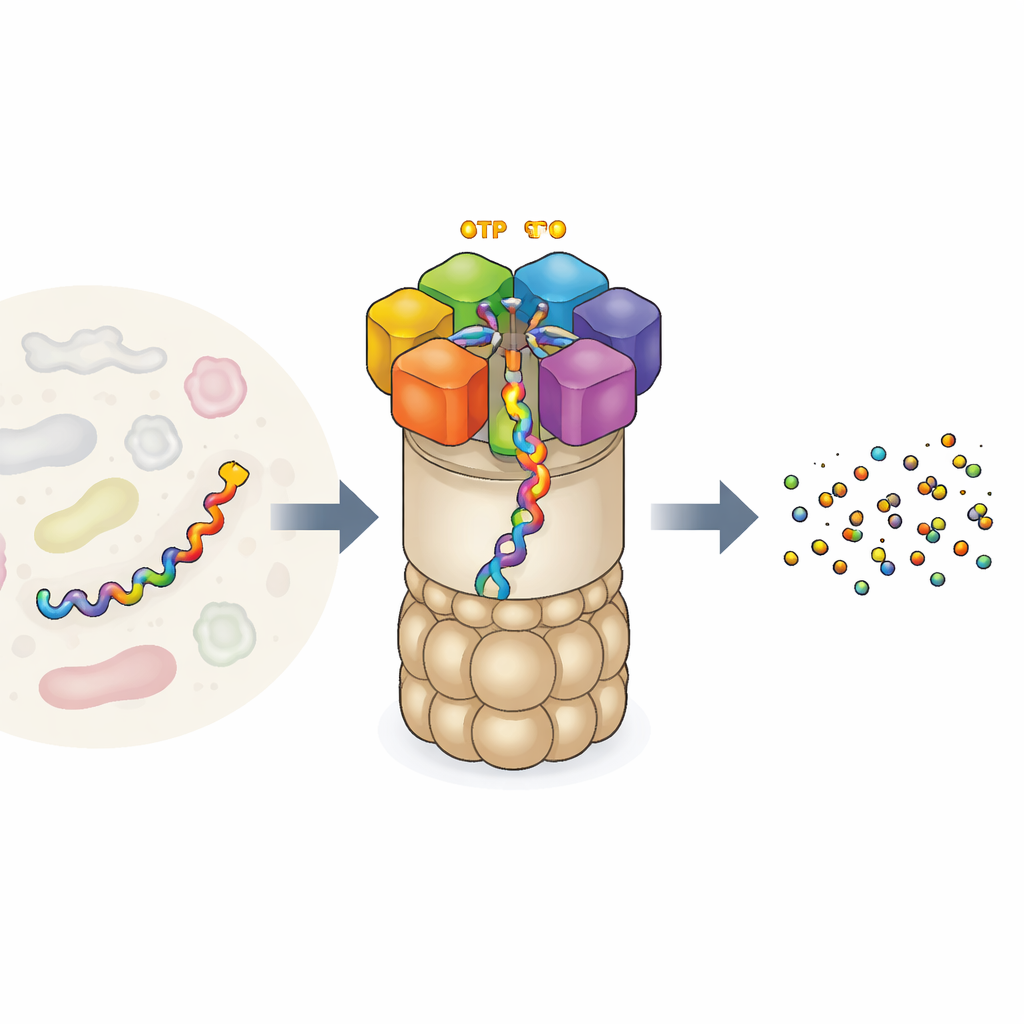
La fabbrica cellulare del riciclo proteico
Il proteasoma 26S è una delle macchine proteiche più grandi e complesse nelle nostre cellule. È costituito da un nucleo a forma di barile che taglia le proteine e da un cappuccio regolatore che riconosce quali proteine distruggere. All’ingresso si trova un anello di sei subunità motrici diverse. Ciascuna può legare ATP, la moneta energetica universale della cellula, e usa quell’energia per afferrare una catena proteica e tirarla nel nucleo per la degradazione. Questo motore non agisce a caso: esperimenti precedenti suggerivano che le sei subunità lavorino in modo coordinato «mano dopo mano», passando la proteina come scalatori su una corda. Ma gli esperimenti potevano osservare solo pochi istantanei di questa azione, lasciando aperte domande sulla sequenza completa dei movimenti e su come esattamente la combustione del carburante sia collegata al lavoro meccanico.
Simulare una prova di forza molecolare
Gli autori hanno costruito un modello probabilistico al computer che tratta il motore come un sistema che salta tra molte conformazioni possibili mentre molecole di ATP e dei suoi prodotti si legano e si staccano. Hanno definito 30 conformazioni principali dell’anello in cui una, due o tre subunità motrici perdono la presa sulla proteina, più uno stato speciale strettamente chiuso in cui tutte e sei trattengono la catena. Usando un algoritmo standard per simulare eventi chimici casuali, hanno seguito centinaia di migliaia di passaggi in cui avvengono il legame dell’ATP, la sua scissione e i cambiamenti conformazionali del motore. Da queste simulazioni hanno potuto prevedere quanto velocemente una proteina venga trascinata attraverso il sistema in diverse condizioni, come quantità variabili di ATP, della sua forma spesa ADP, e di un analogo non scindibile dell’ATP spesso impiegato negli esperimenti.
Quando troppo carburante rallenta il motore
Le simulazioni hanno riprodotto diversi risultati sperimentali sorprendenti. Man mano che i livelli di ATP aumentano da valori bassi, il motore tira le proteine più velocemente, perché il legame del carburante è il passo più lento. Ma oltre circa 1 millimolare di ATP la velocità raggiunge un picco e poi cala: l’anello trascorre più tempo in una conformazione bloccata, non traslocante, in cui tutte e sei le subunità sono occupate dall’ATP eppure la proteina non si muove. L’aggiunta di ADP o dell’analogo non scindibile dell’ATP rallenta il motore in modo costante, perché queste molecole competono con l’ATP per i siti di legame ma non possono completare la corsa meccanica. Il modello predice anche come il motore si comporta quando incontra regioni di una proteina molto strettamente ripiegate, che agiscono da ostacoli. In quei casi il motore trascorre più tempo a lottare contro la resistenza e il tasso complessivo di degradazione diminuisce, in accordo con misure su domini proteici stabilizzati artificialmente.
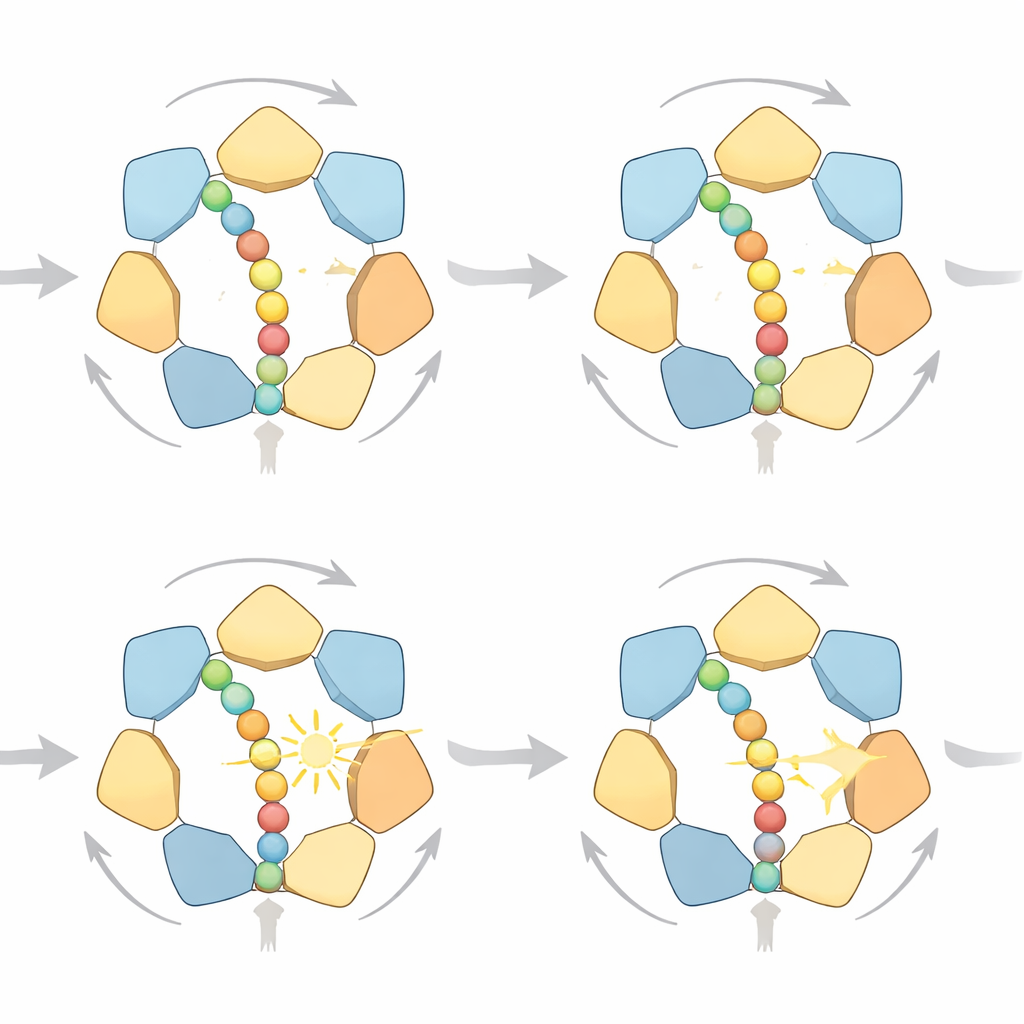
Molte modalità per compiere un passo
Esaminando in dettaglio le traiettorie simulate, i ricercatori hanno scoperto che l’anello non segue un singolo ciclo rigido. Al contrario, esistono molteplici percorsi ad alta probabilità che rispettano la stessa regola direzionale «mano dopo mano»: le subunità vicino all’uscita dell’anello rilasciano la proteina dopo la scissione dell’ATP, si spostano in cima a una scala a spirale di subunità e riafferano la catena più avanti. A volte la proteina avanza con un piccolo passo, a volte con due, a seconda di quante subunità mollano la presa insieme. Con carburante abbondante, prevalgono i movimenti a passo singolo perché sprecano meno lavoro contro forze avverse; quando il carburante scarseggia, il modello predice salti a due passi più frequenti. Le simulazioni collegano inoltre il carico meccanico allo stato chimico del motore: all’aumentare della resistenza e quando la proteina si blocca, l’ADP tende ad accumularsi in un numero maggiore di tasche di legame—esattamente quanto osservano studi strutturali ad alta risoluzione.
Uso dell’energia e regole progettuali condivise
Il modello permette agli autori di mappare come l’energia del motore aumenta quando l’ATP viene scisso e diminuisce quando quell’energia viene convertita in moto. Calcolano una curva di efficienza che mostra che il motore funziona meglio a una forza opposta intermedia: troppo poca resistenza e consuma ATP inutilmente; troppa e rallenta quasi fino a fermarsi. Quando il gruppo ha confrontato le loro previsioni con dati provenienti da macchine distruttrici di proteine correlate in batteri e lievito, ha trovato tendenze molto simili riguardo a come un analogo non scindibile dell’ATP rallenti questi motori. Questo suggerisce che molti membri della stessa famiglia di enzimi ad anello condividono probabilmente un meccanismo comune e conservato per tirare le proteine.
Perché questo è importante per la salute e la malattia
Trasformando istantanee strutturali sparse e misure biochimiche in un unico quadro verificabile, questo lavoro mostra in dettaglio quantitativo come un piccolo motore molecolare traduca carburante chimico in forza per riciclare le proteine della cellula. Il modello non solo spiega una vasta gamma di esperimenti esistenti, ma fa anche previsioni su come variazioni nei livelli di carburante, nel carico meccanico o in mutazioni del motore potrebbero alterare la distruzione proteica. Poiché macchine simili operano in tutte le forme di vita e sono centrali in condizioni che vanno dalla neurodegenerazione al cancro, comprendere il loro funzionamento a questo livello potrebbe in ultima analisi guidare la progettazione di farmaci che modulino, potenzino o blocchino selettivamente questi trituratori microscopici.
Citazione: Wu, D., Ouyang, Q., Wang, H. et al. Nonequilibrium chemomechanical transduction of ATP-driven protein unfolding in the 26S proteasome. npj Biol. Phys. Mech. 3, 4 (2026). https://doi.org/10.1038/s44341-026-00034-w
Parole chiave: proteasoma, motore AAA+ ATPasi, degradazione proteica, macchine molecolari, accoppiamento chemomeccanico