Clear Sky Science · it
Rilevazione proteica ultrasensibile non enzimatica mediante immunoassay di prossimità con microscopia di assorbimento su risonatori fotonici
Perché è importante rilevare tracce minime di proteine
I medici e i ricercatori si affidano sempre più alle proteine nel sangue per segnalare tumori, malattie cardiache, infezioni o infiammazioni dannose molto prima che i sintomi diventino gravi. Ma molti di questi segni molecolari compaiono a livelli talmente bassi che i test di laboratorio standard faticano a rilevarli rapidamente o a basso costo. Questo studio presenta un nuovo metodo di analisi, chiamato PINATA, in grado di individuare quantità estremamente piccole di una proteina legata all’infiammazione utilizzando attrezzature semplici e passaggi a temperatura ambiente, aprendo la strada a diagnostiche più accessibili e sensibili.
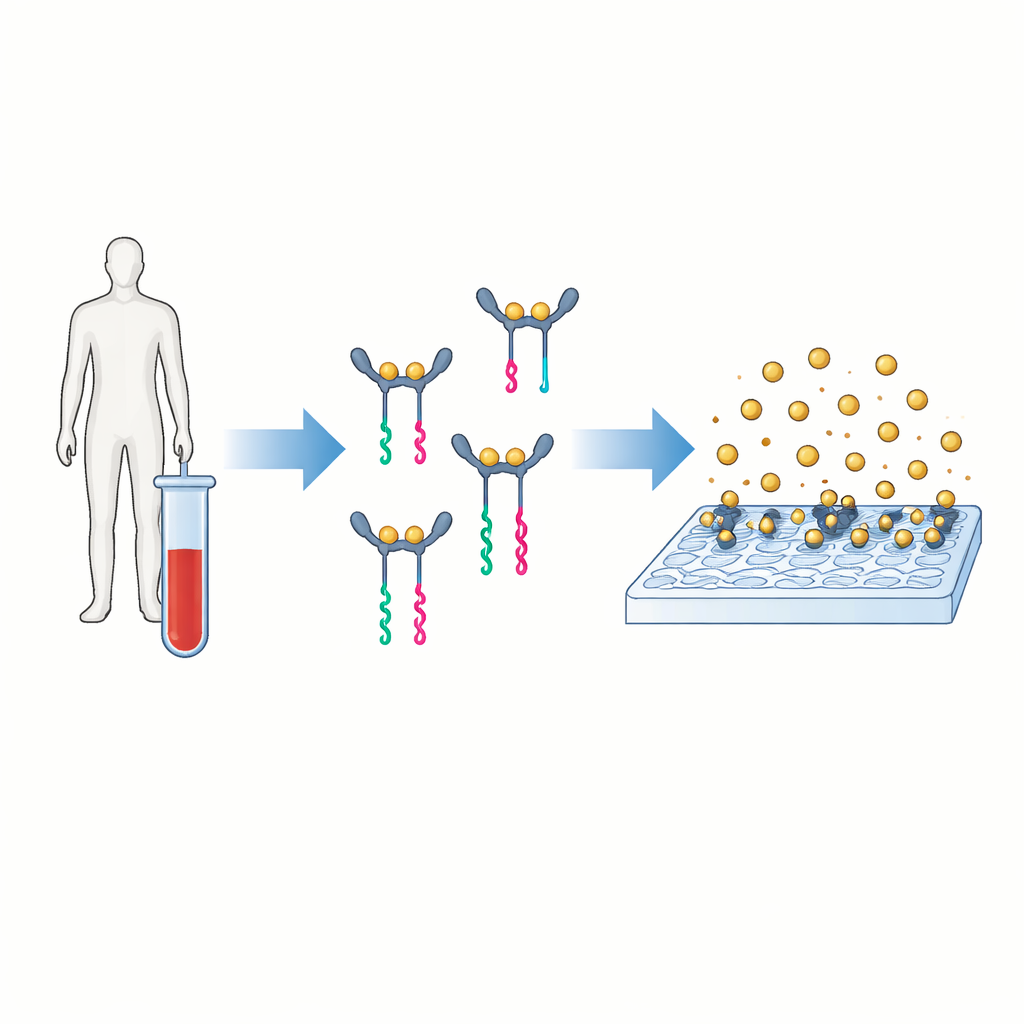
Un nuovo modo di trasformare le proteine in segnali leggibili
L’idea centrale di PINATA è tradurre la presenza di una proteina in un breve frammento di DNA facile da amplificare e contare. Gli autori si concentrano sull’interleuchina‑6, una molecola di segnalazione nel sangue che aumenta in condizioni che vanno dall’infezione al cancro. Nei test convenzionali, due anticorpi si legano alla proteina e portano un enzima che produce un segnale colorato o fluorescente. PINATA conserva il concetto di due anticorpi che riconoscono la stessa proteina, ma al posto degli enzimi aggancia brevi filamenti di DNA a ciascun anticorpo. Quando entrambi gli anticorpi si legano alla stessa proteina e si avvicinano, i loro frammenti di DNA cooperano per rilasciare un pezzo separato di DNA chiamato reporter. Ogni molecola proteica può così innescare il rilascio di molti reporter di DNA identici.
Usare le “regole del traffico” del DNA al posto degli enzimi
Al cuore del metodo ci sono circuiti di DNA progettati con cura che si comportano come sistemi di traffico molecolare, dirigendo quando i filamenti possono legarsi, separarsi o scambiarsi partner. Questi circuiti sono costruiti in modo che, a meno che una proteina non porti i due pezzi di DNA legati agli anticorpi l’uno vicino all’altro, il DNA reporter rimanga bloccato e non venga generato alcun segnale. Quando la proteina è presente, la sua azione di ponte libera il reporter. Questo reporter liberato partecipa quindi a un processo di amplificazione secondario su una superficie preparata. Lì, prende ripetutamente parte a reazioni di scambio di filamenti che permettono a una singola molecola reporter di reclutare numerosi nanoparticelle d’oro sulla superficie, creando un forte segnale digitale senza l’uso di enzimi o cicli di temperatura.
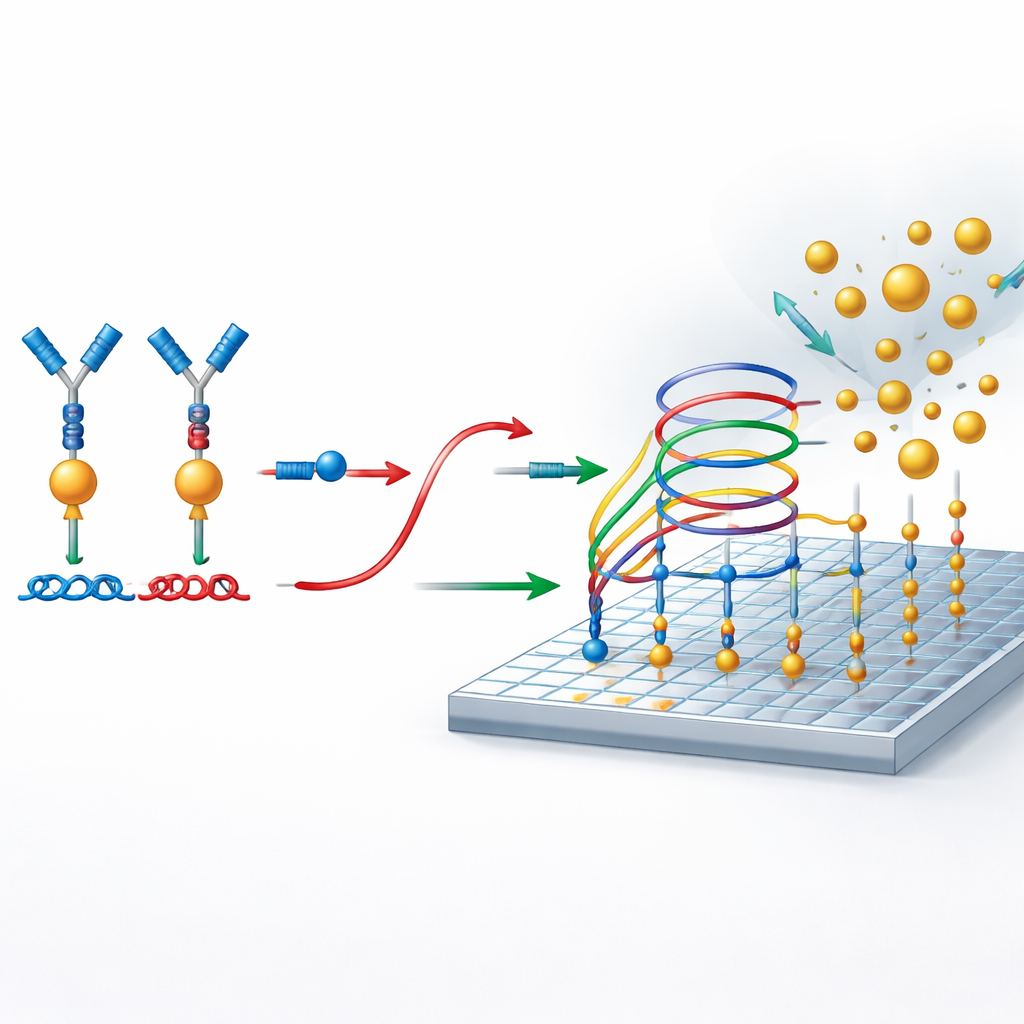
Contare singole nanoparticelle come eventi sì-o-no
Per leggere il risultato, i ricercatori utilizzano la microscopia di assorbimento su risonatori fotonici, o PRAM. La superficie sensibile è un materiale appositamente patternato che riflette fortemente la luce a un particolare colore. Quando nanoparticelle d’oro atterrano su questa superficie, assorbono quella luce e appaiono come punti scuri nell’immagine al microscopio. Poiché il sistema è progettato in modo che le nanoparticelle si leghino solo quando è presente il DNA reporter, ogni punto scuro rappresenta un evento di rilevazione riuscito ricondotto a una molecola proteica. Un semplice e poco costoso apparato ottico e un software di elaborazione delle immagini vengono quindi utilizzati per contare questi punti sulla superficie, trasformando il numero di nanoparticelle in una misura precisa della concentrazione proteica.
Quanto è sensibile e selettivo il test?
Con questo approccio, il team dimostra di poter rilevare l’interleuchina‑6 a livelli bassissimi, fino a 37 femtogrammi per millilitro — approssimativamente alcune decine di molecole in una goccia — su un intervallo dinamico che copre sei ordini di grandezza. Il saggio funziona in un protocollo semplice in due fasi della durata di 90 minuti eseguito interamente a temperatura ambiente. Gli autori dimostrano anche che il test rimane accurato anche quando l’interleuchina‑6 è mescolata in campioni complessi come siero e plasma umano, che tipicamente interferiscono con misurazioni sensibili. Confermano inoltre che gli anticorpi rivolti contro l’interleuchina‑6 non rispondono ad altre proteine correlate, sottolineando la selettività del saggio.
Cosa potrebbe significare per la diagnostica futura
Per un non‑specialista, il punto chiave è che PINATA offre un modo per rilevare proteine correlate a malattie a livelli estremamente bassi utilizzando uno strumento ottico compatto invece di apparecchiature di laboratorio ingombranti e costose. Combinando circuiti di DNA intelligenti con il conteggio digitale di nanoparticelle, il metodo evita enzimi fragili e passaggi di riscaldamento, pur raggiungendo o superando la sensibilità di molti test proteici avanzati. Con ulteriore sviluppo e adattamento ad altri bersagli, questa strategia potrebbe consentire diagnosi più precoci, monitoraggi più frequenti e test point‑of‑care per un’ampia gamma di condizioni in cui piccole variazioni nei livelli proteici hanno grande rilevanza clinica.
Citazione: Shepherd, S., Bhaskar, S., Xu, H. et al. Ultrasensitive non-enzymatic protein detection using proximity immunoassay with photonic resonator absorption microscopy. npj Biosensing 3, 21 (2026). https://doi.org/10.1038/s44328-026-00090-1
Parole chiave: rilevazione di biomarcatori proteici, diagnostica ultrasensibile, sostituzione di filamenti di DNA, saggio per interleuchina‑6, biosensori digitali