Clear Sky Science · it
Vescicole extracellulari neuronali e astrogliali isolate nanomagneticamente su microfluidica per differenziare la malattia a corpi di Lewy e l’Alzheimer
Perché è importante per famiglie e medici
La demenza è un termine ombrello che comprende diverse malattie cerebrali con sintomi simili ma cause sottostanti molto diverse. Due delle più comuni, la malattia di Alzheimer e la malattia a corpi di Lewy, possono apparire quasi identiche in clinica, ma rispondono diversamente ai farmaci e comportano rischi differenti. Oggi, l’unico modo per sapere con certezza quale malattia avesse una persona è esaminare il cervello dopo la morte. Questo studio descrive un nuovo tipo di analisi del sangue che legge minuscoli messaggi rilasciati dalle cellule cerebrali, con l’obiettivo di distinguere queste due demenze mentre le persone sono ancora in vita.
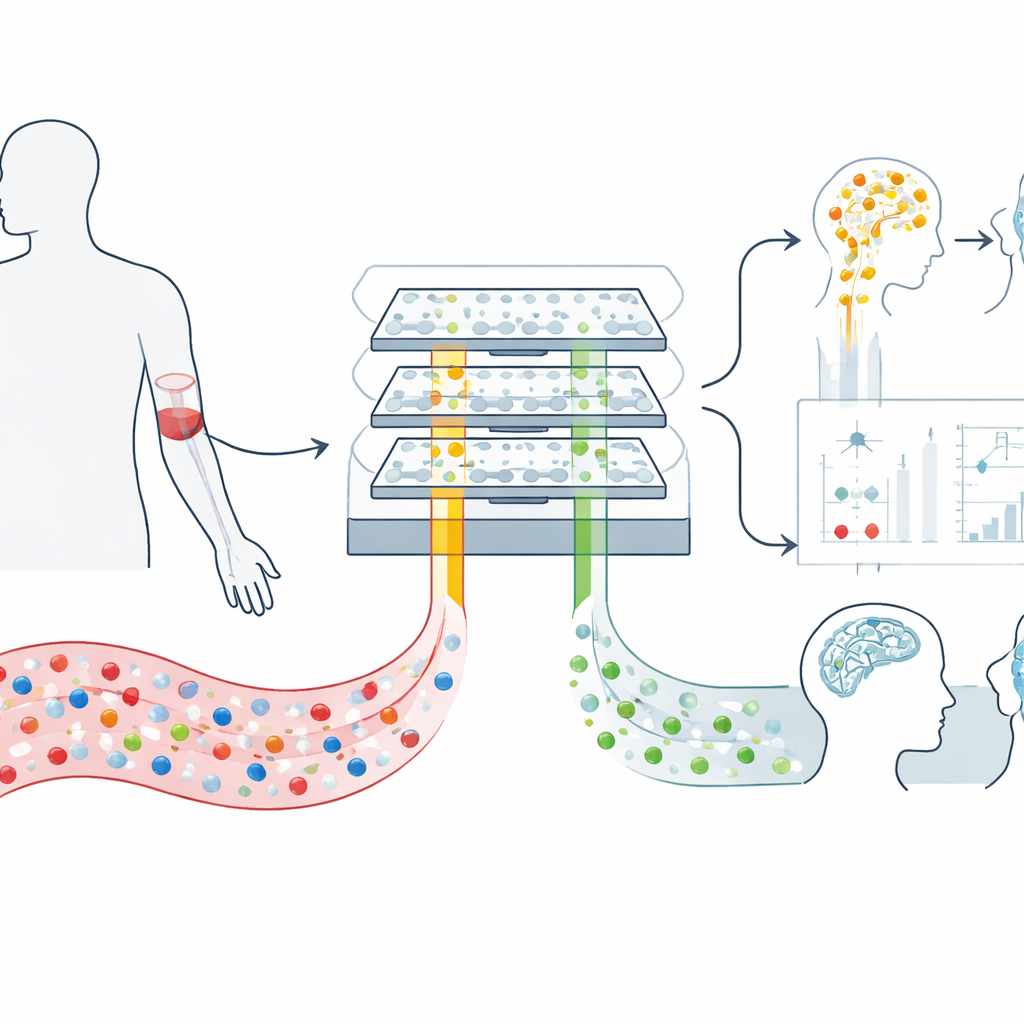
Piccoli pacchetti che viaggiano dal cervello al sangue
I nostri cervelli rilasciano costantemente bolle microscopiche chiamate vescicole extracellulari nel flusso sanguigno. Queste vescicole sono come buste imbottite inviate dai neuroni e dalle loro cellule di supporto, che trasportano frammenti di materiale genetico e proteine che riflettono ciò che sta avvenendo all’interno del cervello. Poiché possono attraversare la barriera emato-encefalica e sopravvivere in circolo, offrono una rara finestra minimamente invasiva sulla biologia cerebrale. La sfida è che un millilitro di sangue contiene centinaia di miliardi di vescicole provenienti da tutto il corpo, quindi quelle di origine cerebrale sono di gran lunga in minoranza e difficili da isolare con i metodi di laboratorio standard.
Un chip magnetico che separa i segnali cerebrali
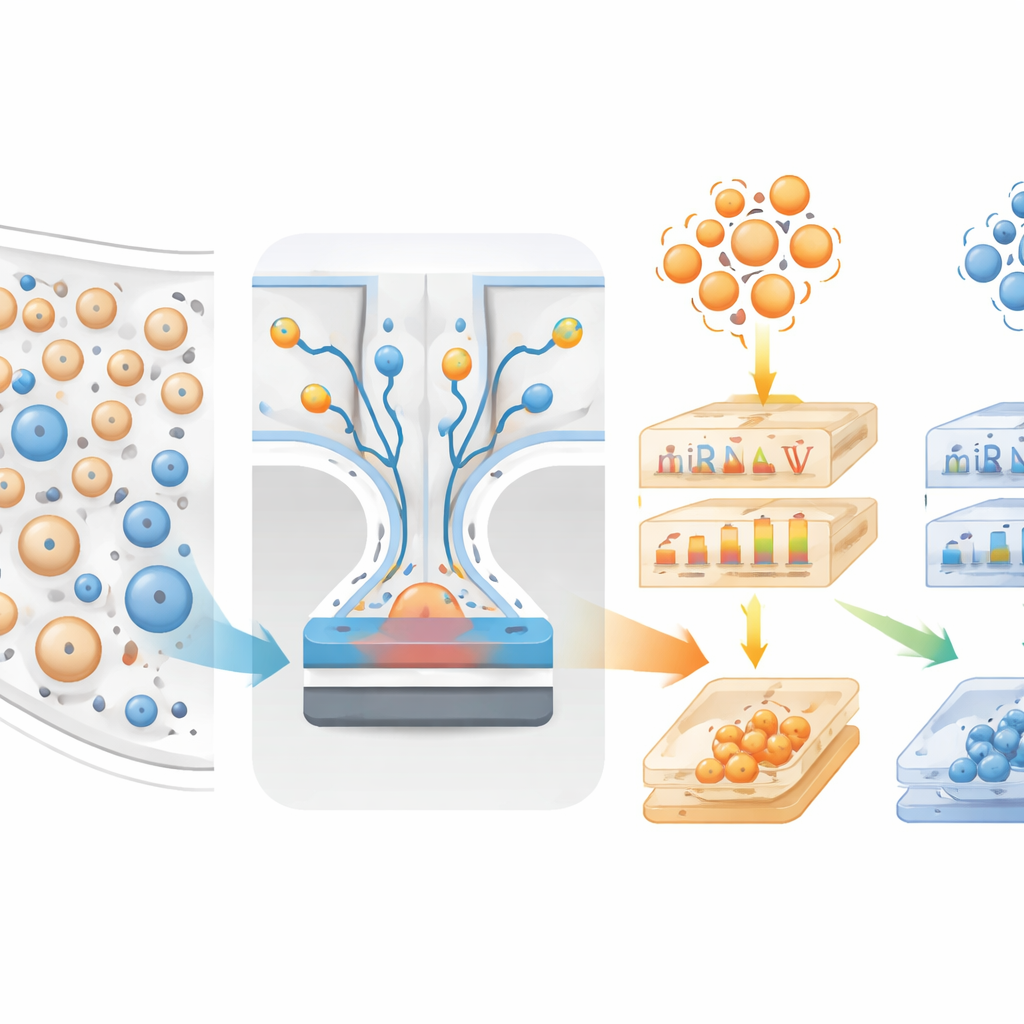
Per affrontare questo problema, i ricercatori hanno costruito un dispositivo microfluidico chiamato mTENPO che combina un chip delle dimensioni di una carta di credito con un magnete potente. Prima che un campione di sangue entri nel chip, le vescicole vengono marcate con nanoparticelle magnetiche usando anticorpi che si legano a proteine di superficie tipicamente presenti sulle vescicole neuronali (GluR2) o su quelle astrocitarie (GLAST). Quando la miscela marcata scorre attraverso milioni di pori microscopici nel chip, il campo magnetico attira le vescicole cerebrali fortemente marcate verso le pareti dei pori, trattenendole mentre il resto defluisce. In questo modo il team può arricchire separatamente due popolazioni di vescicole—quelle prevalentemente neuronali e quelle prevalentemente astrocitarie—direttamente da un piccolo campione di plasma.
Leggere le impronte molecolari
Da 137 volontari la cui diagnosi cerebrale è stata confermata dopo la morte, il team ha isolato questi due tipi di vescicole e ha inoltre misurato proteine plasmatiche classiche dell’Alzheimer come diverse forme di beta-amiloide e tau. Hanno quindi sequenziato piccoli RNA regolatori (miRNA) all’interno delle vescicole e hanno analizzato quali variassero tra persone con malattia a corpi di Lewy pura, Alzheimer puro, patologie miste o assenza di demenza. Molti miRNA presenti nelle vescicole neuronali e astrogliali, insieme a diverse proteine tau fosforilate nel plasma, hanno mostrato schemi distinti tra i gruppi Lewy e Alzheimer. Quando i ricercatori hanno mappato i geni bersaglio di questi miRNA, hanno trovato forti collegamenti con vie coinvolte nella sopravvivenza cellulare, nell’infiammazione e nella gestione delle proteine—processi già implicati nella neurodegenerazione.
Costruire un test del sangue combinato e potente
Poiché nessun singolo marcatore separava nettamente le malattie, il team ha utilizzato strumenti di machine learning per assemblare un pannello compatto delle evidenze più informative tratte da tutti e tre i compartimenti: vescicole neuronali, vescicole astrogliali e proteine plasmatiche. Il pannello risultante a 15 caratteristiche includeva 14 specifici miRNA delle vescicole più due proteine tau fosforilate. Testato con validazione incrociata ripetuta per ridurre l’overfitting, questo pannello multimarker ha distinto la malattia a corpi di Lewy dall’Alzheimer con circa il 95% di accuratezza e un’area sotto la curva di 0,96—sostanzialmente migliore rispetto a qualsiasi singola misura. Le persone con cervelli che mostravano miscele di patologie tendevano ad avere livelli di marcatori intermedi, suggerendo che tali pannelli potrebbero un giorno aiutare a riconoscere malattie miste invece di imporre una etichetta dicotomica.
Dal proof of concept all’uso clinico futuro
Lo studio è una dimostrazione iniziale ma importante che le vescicole delle cellule cerebrali presenti nel sangue possono trasportare informazioni sufficientemente dettagliate da separare i principali tipi di demenza. Il lavoro deve ancora essere confermato in gruppi più numerosi e diversificati e in pazienti seguiti nel tempo, e gli autori sottolineano i limiti attuali nell’identificare con precisione la cellula di origine di ogni singola vescicola. Tuttavia, la combinazione di un chip magnetico scalabile e di un pannello multimarker scelto con cura offre una tabella di marcia per futuri test del sangue che potrebbero guidare le scelte terapeutiche, migliorare gli studi clinici e fornire alle famiglie risposte molto più chiare sulla specifica malattia alla base della demenza di una persona cara.
Citazione: Yang, S.J., Lin, A.A., Shen, H. et al. Microfluidic nanomagnetically isolated neuron- and astrocyte-derived extracellular vesicles to differentiate Lewy body and Alzheimer’s disease. npj Biosensing 3, 19 (2026). https://doi.org/10.1038/s44328-026-00086-x
Parole chiave: vescicole extracellulari, malattia a corpi di Lewy, malattia di Alzheimer, biomarcatori nel sangue, diagnostica microfluidica