Clear Sky Science · it
Rilevazione multiplex di citochine al punto di cura tramite una matrice di elettrodi HexaPie per l’endotipizzazione dell’asma
Perché testare l’asma con la saliva potrebbe cambiare la cura a domicilio
L’asma colpisce centinaia di milioni di persone, eppure i medici faticano ancora ad abbinare a ciascun paziente la terapia più adatta. Questo studio presenta un piccolo sensore elettronico, chiamato HexaPie, che legge segnali immunitari da un semplice campione di saliva anziché dal sangue. Misurando contemporaneamente più molecole legate all’infiammazione, potrebbe un giorno permettere alle persone di monitorare l’asma — e altri problemi immunitari — in modo rapido e indolore a casa o in ambulatorio. 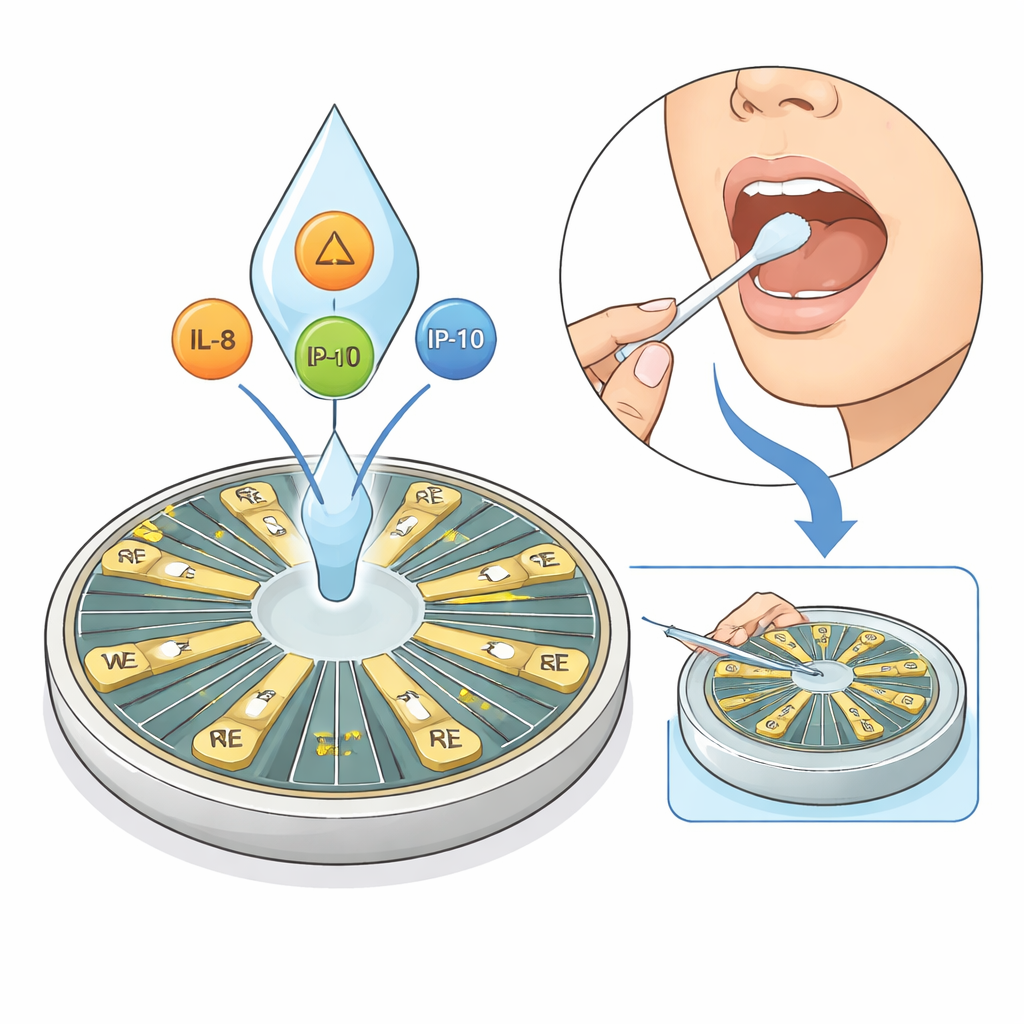
Un nuovo modo di ascoltare il sistema immunitario
L’asma non è una singola malattia, ma una raccolta di diversi “tipi” guidati da percorsi immunitari distinti. I test tradizionali spesso si concentrano su un marcatore alla volta e di solito richiedono prelievi di sangue e macchine di laboratorio centralizzate, che sono lente e scomode per controlli frequenti. Il sistema HexaPie mira a risolvere questo problema individuando tre messaggeri immunitari chiave nella saliva — IL‑8, IL‑10 e IP‑10 — che insieme delineano un quadro più ampio dell’infiammazione delle vie aeree, comprese le forme non eosinofiliche e difficili da trattare. Poiché la raccolta della saliva è non invasiva e semplice, è particolarmente adatta a monitoraggi ripetuti al di fuori dei grandi ospedali.
Una piccola matrice aurea che rileva senza reagenti aggiunti
HexaPie è costruito su una scheda a circuito stampato personalizzata che ospita sei coppie di minuscoli elettrodi d’oro disposti come fette di una torta. Ogni elettrodo attivo è rivestito con un anticorpo diverso che si lega specificamente a una delle citochine bersaglio, mentre l’elettrodo di riferimento accoppiato rimane nudo. Invece di usare coloranti o reagenti redox, il dispositivo si affida a un metodo elettrico senza marcatori: quando le citochine nella saliva si legano ai loro anticorpi, riorganizzano sottilmente particelle cariche e molecole d’acqua sulla superficie metallica. Questo modifica lo strato elettrico doppio — una regione sottile proprio all’interfaccia — e lo spostamento risultante nell’impedenza elettrica può essere letto direttamente, permettendo la misurazione simultanea di tutte e tre le citochine a partire da una singola, piccola goccia.
Mettere il progetto alla prova con simulazioni e test di laboratorio
Prima di costruire dispositivi completi, il team ha utilizzato simulazioni al computer per verificare che la geometria HexaPie distribuisse i campi elettrici e le correnti in modo controllato tra ogni elettrodo attivo e di riferimento. I modelli hanno mostrato che la tensione applicata resta ben confinata vicino alle regioni sensibili e che la corrente scorre principalmente attraverso gli spazi previsti — condizioni necessarie per letture stabili e ripetibili. In laboratorio, i ricercatori hanno quindi verificato la chimica sugli elettrodi d’oro aggiungendo ogni strato — linker, anticorpo e antigene — mentre tracciavano segnali elettrochimici standard. Man mano che più materiale biologico ricopriva la superficie, il flusso di elettroni rallentava e l’impedenza aumentava in passaggi prevedibili, confermando che gli strati di anticorpi si erano formati correttamente e potevano catturare i loro bersagli. 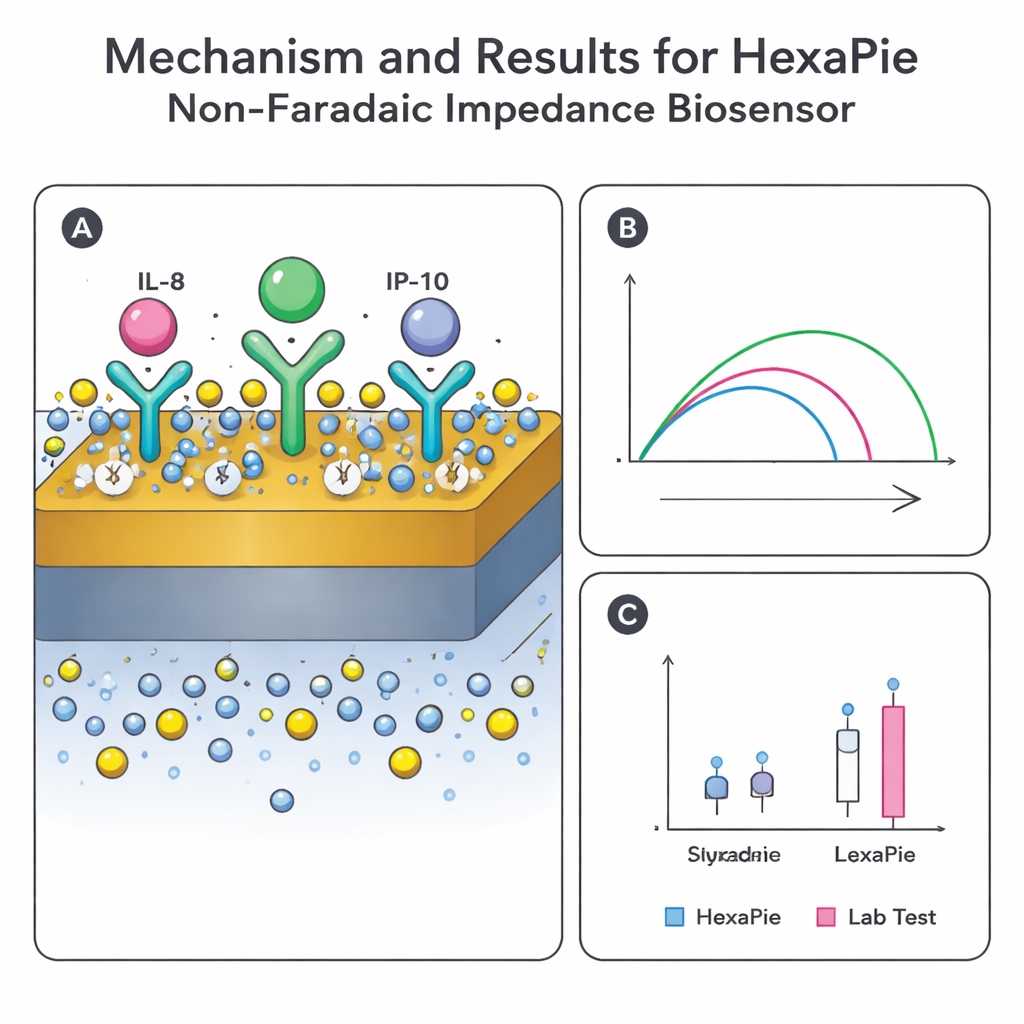
Quanto bene il sensore misura campioni di saliva reali
Per verificare se HexaPie potesse fornire numeri affidabili nella pratica, gli autori hanno aggiunto quantità note delle tre citochine in saliva umana poolata e hanno misurato i corrispondenti cambiamenti di impedenza. I segnali mutate in modo ordinato e dipendente dalla concentrazione, e adattando i dati il team ha costruito curve di calibrazione che convertono le letture elettriche in livelli di citochine. Il dispositivo ha raggiunto limiti di rilevamento bassi — fino a trilionesimi di grammo per millilitro per alcuni marker — entro gli intervalli riportati per persone con vie aeree infiammate. Le misurazioni ripetute sullo stesso chip e tra chip diversi variavano di meno del 15 percento, soddisfacendo gli standard clinici accettati. Quando i ricercatori hanno aggiunto componenti salivari comuni come albumina, acido urico e vitamina C a livelli elevati, le risposte del sensore sono rimaste sostanzialmente invariate, indicando che interferenti quotidiani difficilmente confonderebbero le letture.
Confronto con test di livello ospedaliero
La prova definitiva è stata il confronto di HexaPie con piattaforme di laboratorio consolidate. Saliva di persone con asma (durante esacerbazioni e in fasi stabili) e di soggetti sani fumatori e non fumatori è stata analizzata in parallelo usando HexaPie, un sistema immunodosaggio automatizzato (ELLA) e un test multiplex su perline (Luminex). Sebbene questo piccolo studio non abbia trovato chiare differenze tra i gruppi nei livelli di citochine — probabilmente a causa dei tempi e della dimensione del campione — i valori del nuovo sensore per IL‑8 e IP‑10 hanno corrisposto strettamente a quelli di entrambi i metodi di riferimento, con solo piccoli scostamenti medi. IL‑10, che è naturalmente scarso e difficile da misurare, ha mostrato maggiori discrepanze tra le piattaforme, sottolineando una sfida più ampia nel rilevare in modo affidabile molecole a bassa abbondanza nella saliva.
Cosa significa per la cura di tutti i giorni
Per i non specialisti, il messaggio è che HexaPie porta misurazioni immunitarie in stile di laboratorio in un dispositivo compatto, privo di reagenti, che funziona direttamente sulla saliva. Monitora in modo affidabile aumenti clinicamente significativi di tre citochine correlate all’asma senza etichette aggiuntive o procedure di campionamento complesse, e le sue letture concordano bene con i test di riferimento per due di esse. Sebbene siano necessari ulteriori lavori per perfezionare la rilevazione di IL‑10 e per convalidare il sistema su gruppi di pazienti più ampi, questa tecnologia indica un futuro in cui le persone con asma e altre malattie infiammatorie potrebbero monitorare il loro stato immunitario rapidamente e senza dolore al punto di cura, aiutando i medici a personalizzare i trattamenti sul profilo immunitario unico di ciascuno.
Citazione: Churcher, N.K.M., Rizvi, F.Z., Qureshi, A. et al. Point-of-care multiplexed detection of cytokines using a HexaPie electrode array for asthma endotyping. npj Biosensing 3, 16 (2026). https://doi.org/10.1038/s44328-026-00081-2
Parole chiave: monitoraggio dell’asma, biosensore per saliva, rilevazione di citochine, diagnostica point-of-care, impedenza elettrochimica