Clear Sky Science · it
Bioassay potenziato da plasmoni per il rilevamento e la quantificazione senza amplificazione dell'RNA di SARS-CoV-2
Perché contano test virali più rapidi e semplici
La pandemia di COVID-19 ha messo in luce quanto facciamo affidamento su test di laboratorio lenti, costosi e difficili da scalare quando milioni di persone necessitano di risposte rapide. Il lavoro qui descritto presenta un nuovo tipo di test di laboratorio in grado di individuare e contare piccole quantità di materiale genetico del coronavirus senza il consueto passaggio di amplificazione usato nella PCR. Questo approccio mira ad avvicinare l’accuratezza ospedaliera a test semplici e a basso costo che potrebbero essere impiegati più diffusamente durante future epidemie.
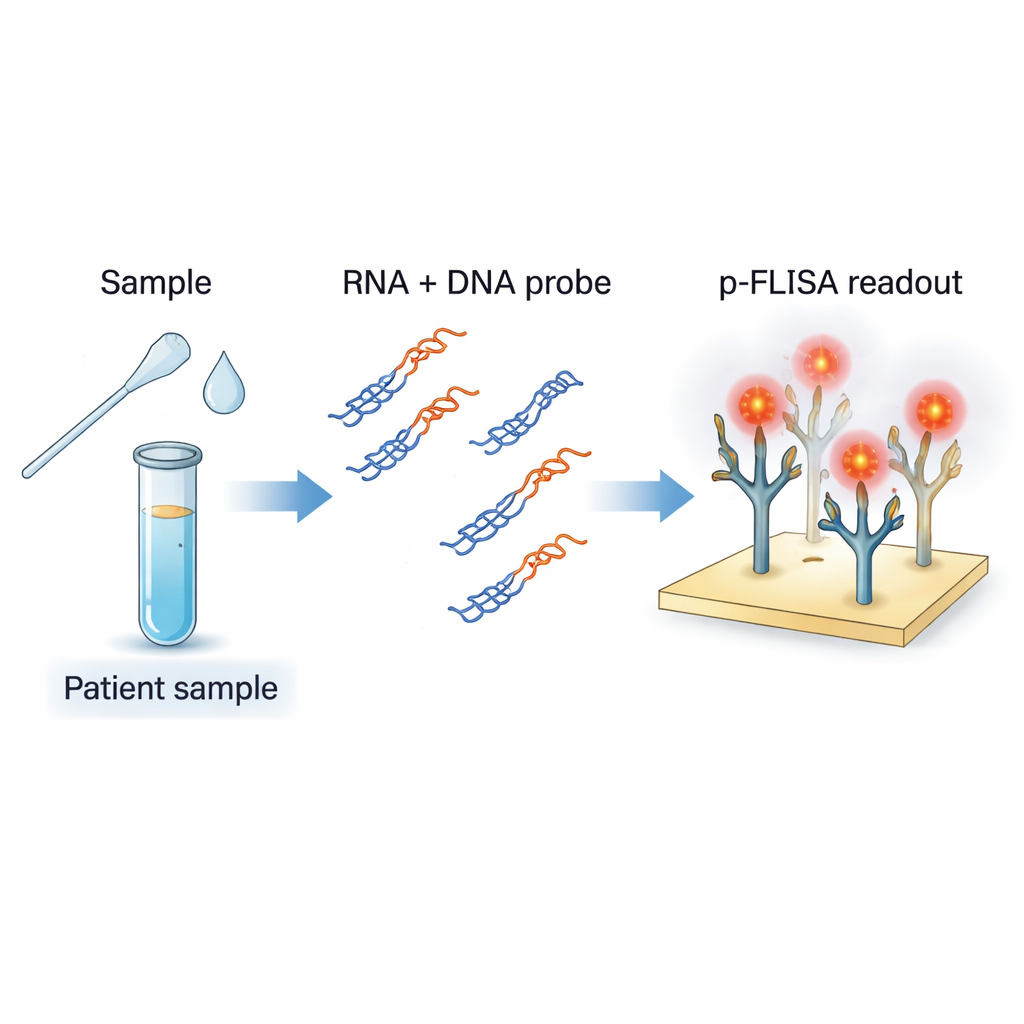
Un nuovo modo di vedere tracce genetiche virali
La diagnosi standard di COVID-19 utilizza la RT-PCR, che produce molte copie di frammenti di RNA virale affinché possano essere rilevati. Pur essendo molto sensibile, la PCR richiede apparecchiature complesse, personale qualificato e tempo, e di solito fornisce una risposta “sì o no” invece di una misura precisa della carica virale. Gli autori hanno voluto costruire un assay che funzioni più come una versione molto avanzata di un test ELISA: un formato semplice su piastra, ma tarato per rilevare direttamente l’RNA virale e quantificare la sua concentrazione. Il loro metodo mira all’RNA di SARS-CoV-2 in campioni come tamponi nasali e saliva, ma è progettato per essere facilmente adattabile ad altri virus a RNA.
Trasformare l’RNA in un bersaglio catturabile
Il gruppo usa brevi frammenti di DNA progettati per corrispondere a regioni specifiche del genoma di SARS-CoV-2. Quando vengono mescolati con l’RNA estratto da un campione del paziente e sottoposti a un lieve riscaldamento e raffreddamento, queste sonde di DNA si appaiano con qualsiasi RNA virale corrispondente per formare ibridi DNA–RNA, come una piccola cerniera con un filamento di RNA e uno di DNA. Un anticorpo speciale chiamato S9.6 fa da cattore: riconosce e si lega saldamente a questi ibridi, ma non al DNA a singolo o doppio filamento ordinario né ad RNA non correlati. Rivestendo il fondo di una piastra con S9.6, l’assay cattura selettivamente solo quegli ibridi che contengono le sequenze genetiche virali d’interesse, filtrando il resto del materiale genetico presente nel campione.
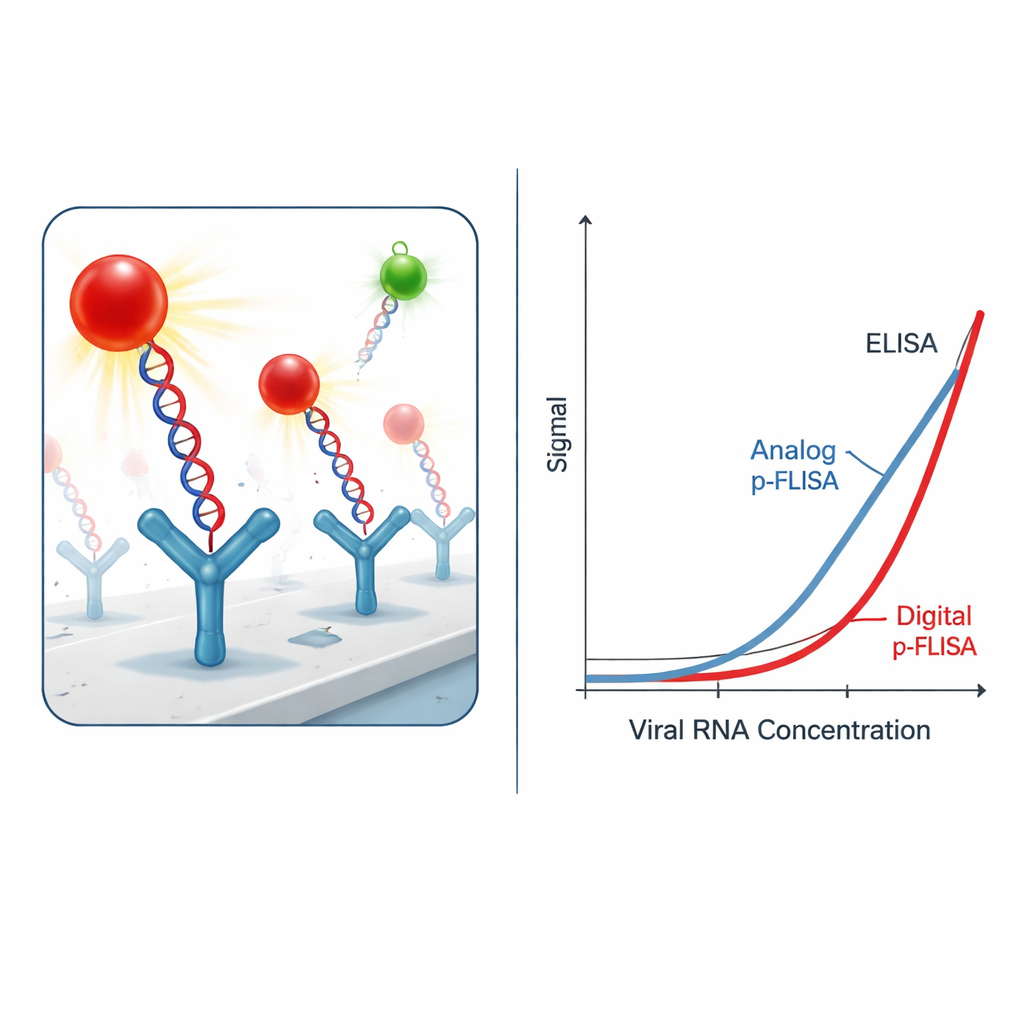
Rendere il segnale ultrabrillante
Limitarsi a catturare gli ibridi virali non è sufficiente; la sfida è distinguerli dal rumore di fondo. Invece dei coloranti fluorescenti convenzionali, i ricercatori utilizzano nanomarcatori “plasmonic-fluor” — nanoparticelle ingegnerizzate che funzionano come minuscole antenne per la luce. Ogni marcatore combina un nanorod metallico con molte molecole fluorescenti e un rivestimento che gli permette di ancorarsi a tag biotinici sul DNA o sull’anticorpo. Questi marcatori plasmonici emettono luce più di mille volte più intensa rispetto ai coloranti standard nelle stesse condizioni. In pratica, ciò significa che servono molti meno ibridi virali per produrre un bagliore rilevabile, migliorando drasticamente la sensibilità del test e abbassando la concentrazione minima di RNA virale che può misurare.
Dalla luminescenza analogica al conteggio digitale
Nella sua forma “analogica” più semplice, l’assay misura la luminosità complessiva di ciascun pozzo della piastra, molto simile a un classico test fluorescente. Anche in questa modalità, il sistema potenziato da plasmoni migliora il limite di rilevamento e il più basso livello quantificabile in modo affidabile di RNA di SARS-CoV-2 di uno-tre ordini di grandezza rispetto a un ELISA tradizionale che usa enzimi o fluorofori standard. Gli autori spingono poi l’idea oltre passando a un formato “digitale”: invece di mediare la luce sull’intero pozzo, acquisiscono l’immagine della superficie con un microscopio a fluorescenza e contano i singoli nanomarcatori brillanti usando un software di analisi immagini su misura. Questo approccio di conteggio delle singole particelle produce un ulteriore guadagno di sensibilità di dieci- trenta volte, portando complessivamente a limiti di rilevamento circa 2.300 volte migliori e a limiti di quantificazione 460 volte migliori rispetto all’ELISA.
Applicare il test a campioni reali
Per verificare se il metodo regge al di fuori di miscele controllate in laboratorio, i ricercatori hanno testato RNA estratto da tamponi nasali e saliva di pazienti con COVID-19, incluse infezioni dovute a diversi varianti virali come alpha/beta e delta, oltre a campioni di persone con altri virus respiratori. Il loro assay potenziato da plasmoni ha rilevato RNA di SARS-CoV-2 in tutti i campioni positivi alla PCR, senza segnale superiore al fondo nei campioni negativi alla PCR o in quelli contenenti altri virus, indicando eccellente sensibilità e specificità clinica comparabili alla RT-PCR. Inoltre, le concentrazioni di RNA misurate mostrano una relazione inversa con i valori di ciclo soglia (Ct) della PCR: i campioni che richiedevano meno cicli PCR (indicando una carica virale maggiore) mostravano livelli di RNA più alti con il nuovo assay, coerente con le aspettative biologiche e suggerendo che può fornire informazioni quantitative significative sulla carica virale.
Cosa potrebbe significare per future epidemie
Per i non specialisti, il messaggio chiave è che questo assay offre un modo per misurare quanto virus è presente senza il passaggio di copiatura che rende la PCR lenta e dipendente da apparecchiature complesse. Combinando un anticorpo selettivo per ibridi RNA–DNA con sorgenti di luce nanoscalari ultrabrillanti e il conteggio digitale, il metodo si avvicina alle prestazioni della PCR mantenendo un flusso di lavoro semplice su piastra. Con ulteriori validazioni e sviluppi ingegneristici, tali assay potenziati da plasmoni potrebbero essere adattati a molti bersagli di RNA e possibilmente riconfigurati in formati rapidi point-of-care, aiutando i clinici non solo a diagnosticare le infezioni ma anche a valutare lo stadio della malattia e la contagiosità a partire da una misura assoluta dell’RNA virale.
Citazione: Liu, L., Seth, A., Liu, Y. et al. Plasmon-enhanced bioassay for amplification-free detection and quantification of SARS-CoV-2 RNA. npj Biosensing 3, 13 (2026). https://doi.org/10.1038/s44328-026-00078-x
Parole chiave: rilevamento RNA di SARS-CoV-2, nanomarcatori plasmonici, immunoassay digitale, diagnostica senza amplificazione, quantificazione della carica virale