Clear Sky Science · it
Un biosensore microfluidico basato su micro-organi per il monitoraggio continuo dei livelli di glucosio in vivo
Perché questo è importante per le persone con diabete
Per le persone con diabete di tipo 1, i sistemi attuali di “pancreas artificiale” richiedono ancora attenzione costante: segnalare i pasti, gestire gli allarmi e preoccuparsi per l’ipoglicemia notturna. Questo studio esplora un tipo radicalmente diverso di sensore del glucosio che non si affida a un singolo enzima o a una formula informatica, ma prende in prestito un piccolo frammento vivente del meccanismo biologico di controllo degli zuccheri: aggregati di cellule pancreatiche chiamati isole. Permettendo a questi mini-organi di fare ciò che l’evoluzione ha ottimizzato per loro, i ricercatori mirano a costruire monitor del glucosio più intelligenti e sicuri che un giorno possano funzionare in modo più autonomo e in background.
Un micro-organo come sensore vivente
La maggior parte dei biosensori attuali rileva le sostanze chimiche usando molecole purificate o linee cellulari singole. Rispondono a una sostanza specifica e poi trasmettono il segnale grezzo a un software che cerca di interpretarlo. Gli autori sostengono che questo approccio ignora un “computer” intrinseco e potente: i micro-organi, come le isole pancreatiche, che naturalmente percepiscono molti segnali contemporaneamente e li traducono in una risposta coordinata. Ogni isola contiene diversi tipi di cellule produttrici di ormoni che comunicano continuamente fra loro. Insieme mantengono la glicemia entro un intervallo ristretto e sicuro, reagendo non solo al glucosio ma anche agli aminoacidi, agli ormoni intestinali e dello stress e alla storia recente di alti e bassi dell’organismo. Questa complessità innata, suggeriscono, potrebbe essere sfruttata per ottenere informazioni più ricche e affidabili rispetto a un semplice sensore a glucosio-ossidasi.
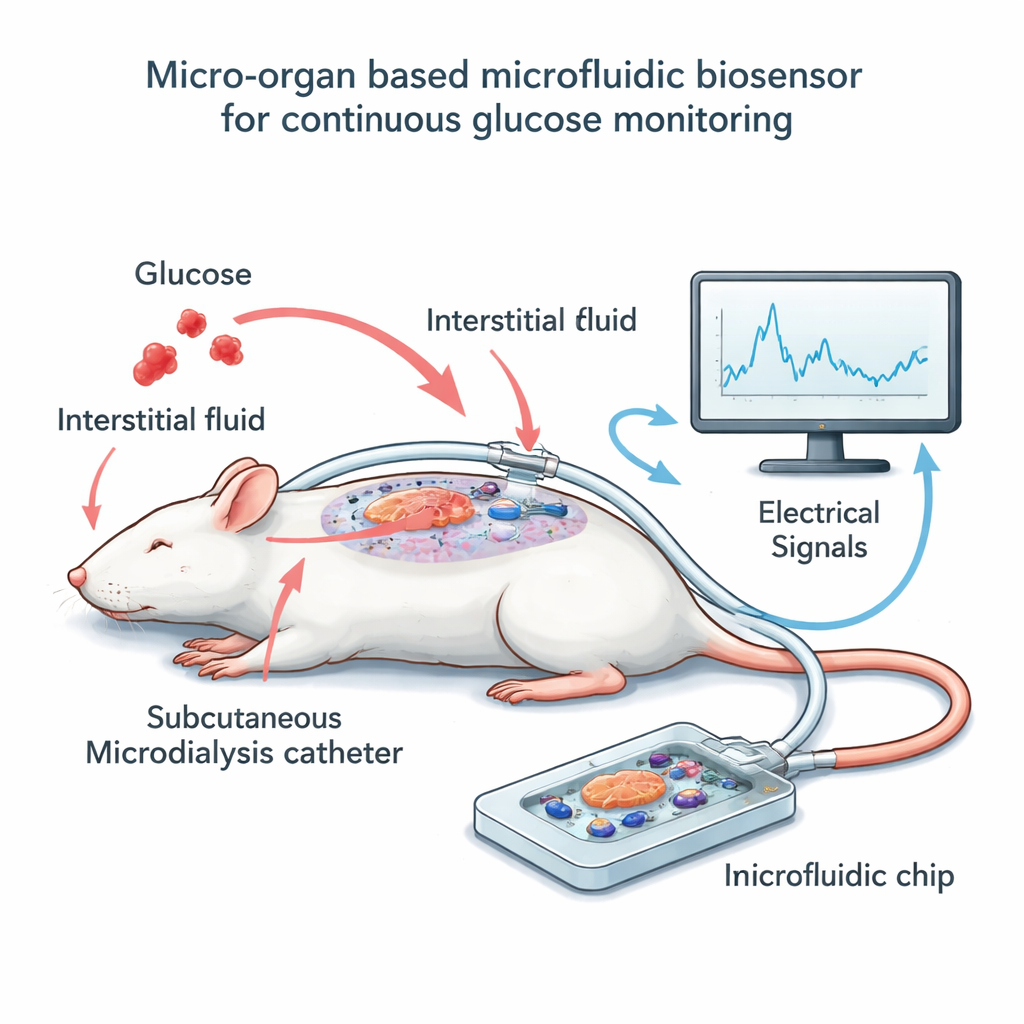
Costruire il sistema chip-catetere
Per mettere alla prova l’idea, il team ha costruito un piccolo dispositivo extracorporeo che ospita alcune decine di isole di topo sopra una griglia di microelettrodi. Invece di immergere direttamente queste cellule nel sangue, hanno usato una tecnica chiamata microdialisi: un sottile catetere flessibile è posizionato appena sotto la pelle di ratti anestetizzati e raccoglie lentamente il fluido tissutale circostante, che segue da vicino la glicemia ma con un breve ritardo. Un flusso costante e basso trasporta questo fluido attraverso un canale stretto sulle isole presenti sul chip. Quando i livelli di glucosio nel dialisato aumentano o diminuiscono, le isole modificano la loro attività elettrica, che gli elettrodi catturano come segnali lenti e ondulatori. In parallelo, i ricercatori misuravano periodicamente il glucosio nel sangue dei ratti e nel dialisato, permettendo di allineare la lettura elettrica con i livelli reali di zucchero nel tempo.
Come il sensore vivente ha risposto alle variazioni di zucchero
Innanzitutto, gli scienziati hanno verificato se le isole sugli elettrodi potessero rispondere a componenti ematici reali piuttosto che a semplici soluzioni di laboratorio. Le hanno esposte a sieri umano e di ratto con diversi livelli di glucosio e hanno osservato cambiamenti chiari e graduati sia nella frequenza sia nell’ampiezza delle loro onde elettriche. Le risposte sono state abbastanza forti da distinguere piccoli incrementi di concentrazione di zucchero nell’intervallo rilevante per il diabete. Successivamente sono passati agli esperimenti sui ratti, somministrando un’iniezione di glucosio per aumentare la glicemia e più tardi iniettando insulina per abbassarla. Tenendo conto del tempo necessario perché il glucosio passi dal sangue al fluido tissutale e attraverso il tubing, hanno riscontrato che la frequenza dei segnali elettrici lenti delle isole aumentava e diminuiva quasi in sincronia con la glicemia. L’analisi statistica su più animali ha mostrato una relazione sorprendentemente stretta e ripetibile tra la frequenza del segnale e il livello di glucosio, mentre l’ampiezza del segnale, pur informativa, è risultata un po’ più variabile.
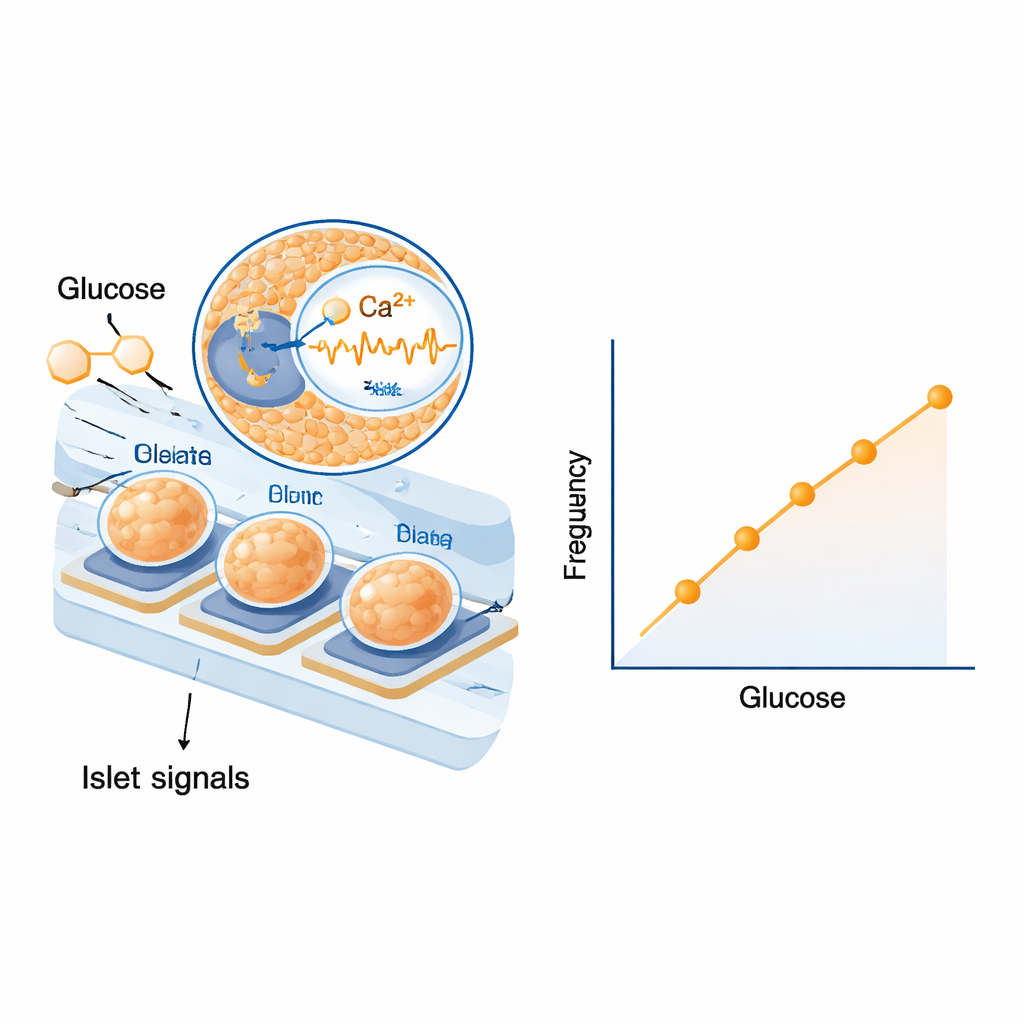
Meccanismi di sicurezza integrati dalla biologia
Un vantaggio importante dell’uso di isole intatte, anziché di una singola molecola, è che il loro comportamento include già meccanismi di sicurezza modellati dall’evoluzione. Lavori precedenti, e indizi emersi da questo studio, mostrano che le isole reagiscono più intensamente quando il glucosio diminuisce rispetto a quando aumenta—una forma di “isteresi” che aiuta a proteggere dall’ipoglicemia pericolosa. I pattern elettrici sono anche influenzati dai tipi cellulari vicini che amplificano o attenuano il rilascio di insulina a seconda delle esigenze dell’organismo. Poiché il chip si limita ad ascoltare questi segnali integrati senza aggiungere coloranti o modifiche genetiche, può registrare per giorni senza danneggiare le cellule. Gli autori segnalano sfide tecniche future, come evitare bolle d’aria, garantire prestazioni di microdialisi a lungo termine e decidere quale tipo di isole umane o derivate da cellule staminali dovrebbe essere impiegato in prospettiva. Tuttavia, simulazioni al computer usando un modello consolidato del diabete suggeriscono che un sensore basato su isole potrebbe eguagliare o persino superare i monitor del glucosio attuali in condizioni difficili.
Cosa potrebbe significare per la cura del diabete in futuro
Questo lavoro dimostra che poche isole pancreatiche mantenute vive su un piccolo chip e collegate al corpo tramite un sottile catetere possono tracciare continuamente la glicemia negli animali viventi attraverso la loro naturale attività elettrica. Per un lettore non specialista, il messaggio chiave è che invece di chiedere a un semplice sensore chimico di misurare il glucosio e poi costringere un computer a interpretare cosa significhi per l’organismo, questo approccio ascolta direttamente lo stesso tipo di tessuto vivente che normalmente decide quanto insulina rilasciare. Se perfezionati e resi pratici per l’uso umano, tali biosensori viventi potrebbero diventare il nucleo di sistemi di pancreas artificiale veramente autonomi—dispositivi che anticipano silenziosamente i bisogni del corpo e riducono l’onere quotidiano della gestione del diabete.
Citazione: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
Parole chiave: monitoraggio continuo del glucosio, pancreas artificiale, isole pancreatiche, biosensore microfluidico, diabete di tipo 1