Clear Sky Science · it
Massimizzare l’utilizzo dei fotoni nella microscopia di localizzazione spettroscopica a singola molecola usando prismi doppi a cuneo disperdenti simmetrici
Visioni più nitide del mondo minuscolo
Molti dei protagonisti più importanti in biologia — singole molecole all’interno delle nostre cellule — sono troppo piccoli per essere visti con i microscopi convenzionali. Nell’ultimo decennio, nuove tecniche «super-risolutive» hanno cambiato questa situazione, ma spesso costringono gli scienziati a scambiare nitidezza dell’immagine con informazioni sul colore o a ricorrere a esperimenti lunghi e complessi. Questo articolo presenta un accessorio ottico ingegnoso che aiuta i ricercatori a vedere molte specie molecolari contemporaneamente, in 3D, con maggiore dettaglio e meno complicazioni.
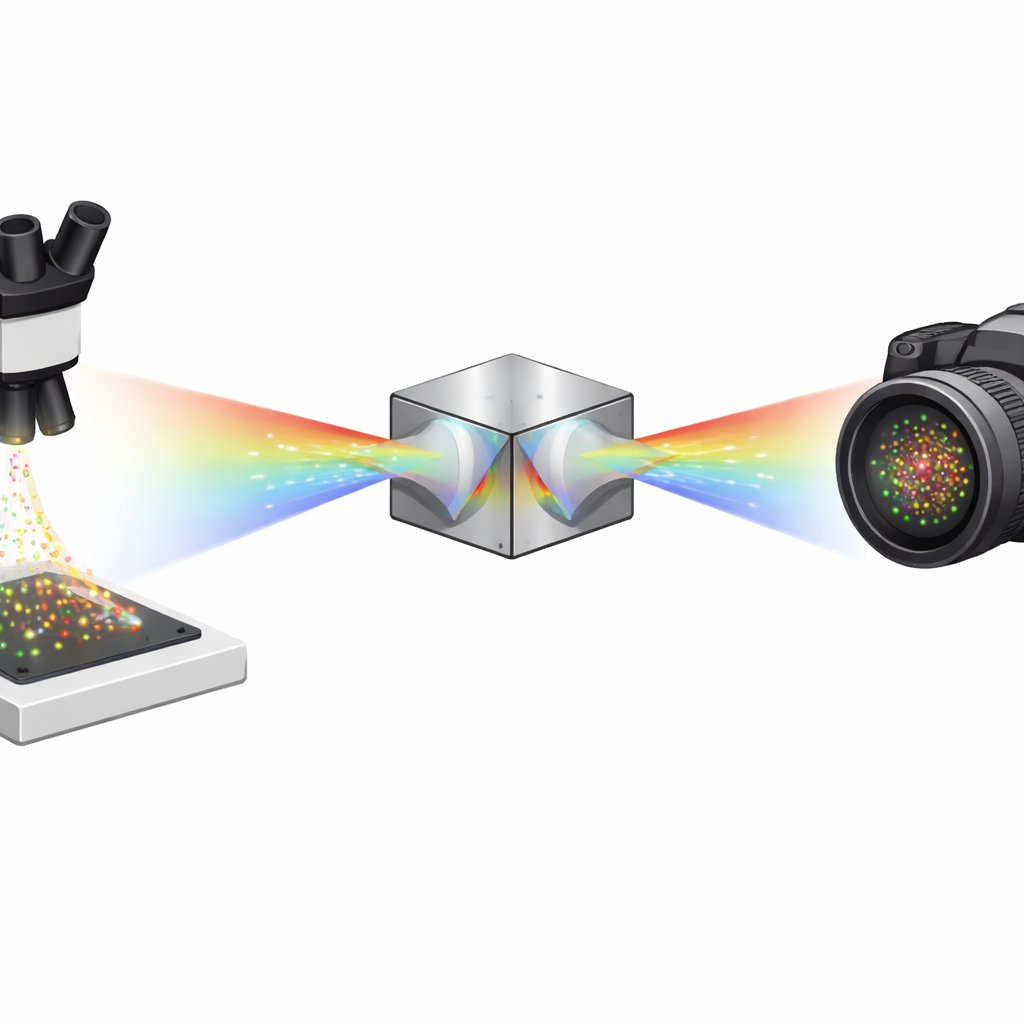
Osservare le singole molecole una alla volta
Metodi super-risolutivi come STORM e PALM funzionano facendo lampeggiare solo poche molecole fluorescenti alla volta, individuando ogni lampeggio con elevata precisione e combinando migliaia di fotogrammi per ottenere un’immagine dettagliata. La microscopia di localizzazione spettroscopica a singola molecola (sSMLM) spinge questo approccio oltre: non solo determina la posizione di ogni molecola, ma misura anche il suo spettro di emissione. Questa informazione spettrale aggiuntiva è potente perché permette di usare più coloranti dai spettri sovrapposti e distinguerli comunque. Il problema è che la sSMLM tradizionale di solito divide i preziosi fotoni tra un’immagine di posizione e un’immagine spettrale, il che sfoca il risultato finale e rende difficile rilevare molecole deboli.
Usare ogni fotone due volte
Gli autori risolvono questo problema con un modulo ottico compatto basato su due prismi doppi a cuneo identici e uno splitter di fascio. Invece di inviare i fotoni in un braccio «posizione» e in un braccio separato «colore», il loro progetto con prismi doppi a cuneo disperdenti simmetrici (SDDWP) crea due copie speculari e disperse spettralmente di ogni molecola lampeggiante sulla stessa camera. Poiché queste due immagini sono perfettamente simmetriche, un semplice calcolo può recuperare sia la posizione reale della molecola (dal punto medio tra i due spot) sia il suo spettro (da quanto sono distanti gli spot). Di fatto, tutti i fotoni raccolti contribuiscono sia alle informazioni spaziali sia a quelle spettrali, migliorando drasticamente la precisione con cui il sistema può localizzare e identificare ogni molecola.
Colori più nitidi e più chiari in tre dimensioni
Usando modelli analitici e campioni di test accuratamente calibrati, il team mostra che l’SDDWP migliora la precisione laterale (in piano) di circa il 27% e la precisione spettrale di circa il 48% rispetto al loro precedente sistema basato su prisma. Hanno poi esteso il progetto all’imaging tridimensionale con un approccio «biplano», in cui le due immagini spettrali sono leggermente fuori fuoco in direzioni opposte. Analizzando come cambia la dimensione di ciascuno spot tra i due piani, il sistema può determinare quanto una molecola si trovi sopra o sotto il piano focale, ottenendo una precisione assiale dell’ordine di 18 nanometri entro una profondità utile di circa mezzo micrometro. Nonostante la complessità aggiunta dall’imaging 3D, il nuovo progetto mantiene livelli di nitidezza spettrale prossimi a quelli 2D, permettendo una discriminazione molto fine tra coloranti i cui spettri si sovrappongono fortemente.
Separare i colori di strutture cellulari e particelle in movimento
Per dimostrare il significato pratico di tutto ciò, i ricercatori hanno immaginato cellule HeLa fissate in 3D usando un singolo laser rosso e tre coloranti nel rosso lontano che normalmente hanno spettri sovrapposti. Hanno marcato perossisomi, microtubuli e mitocondri, e mostrato che il sistema poteva separare in modo affidabile queste strutture basandosi sulle sottili differenze spettrali pur mantenendo elevato il dettaglio spaziale lungo la profondità. Hanno anche usato punti quantici spettralmente distinti come piccole etichette per tracciare molte particelle in movimento contemporaneamente in una soluzione viscosa. Trattando lo spettro di ogni particella come una «impronta» unica, la configurazione SDDWP è stata in grado di seguire correttamente centinaia di traiettorie densamente impaccate che altrimenti si sarebbero aggrovigliate quando i percorsi si incrociavano, riducendo gli errori di tracciamento a solo pochi punti percentuali anche a densità di particelle vicine ai limiti teorici.
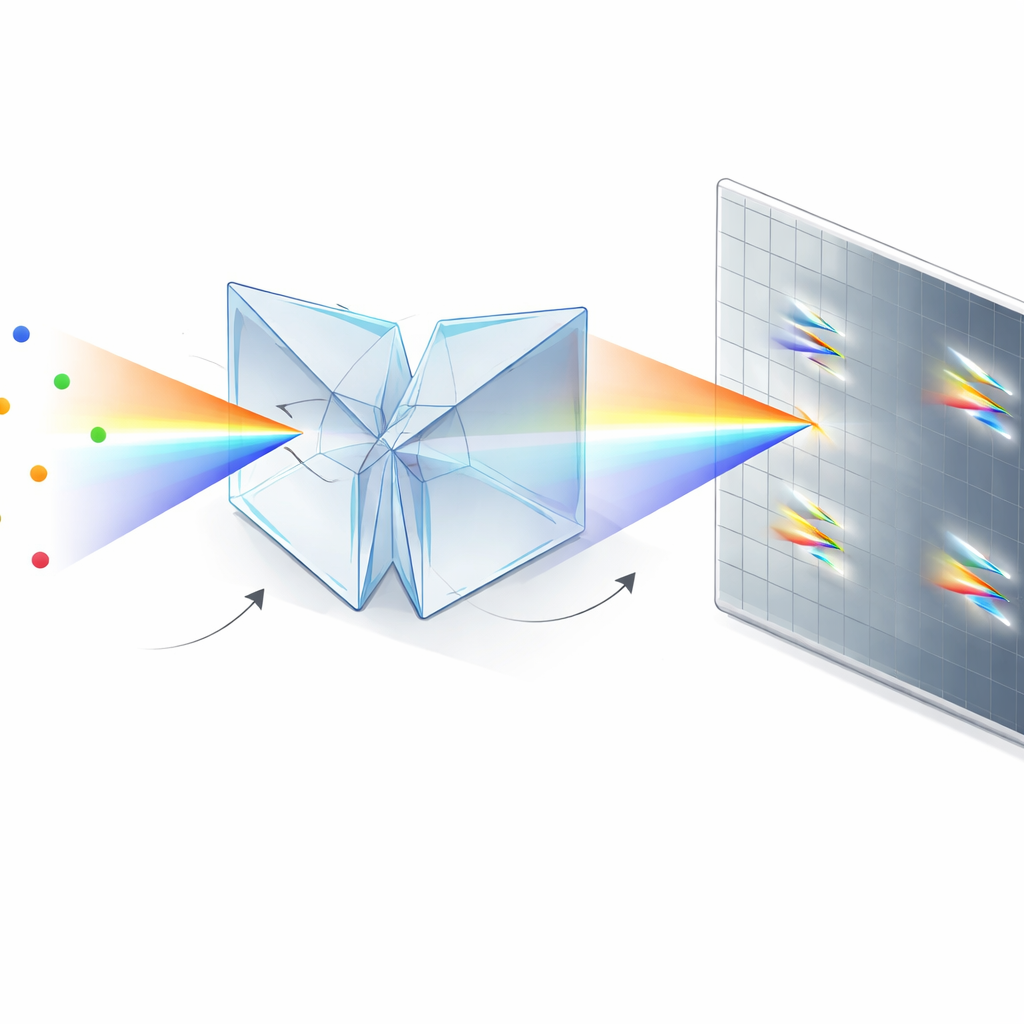
Dalla ottica complessa a un semplice accessorio
Oltre alle prestazioni, un vantaggio chiave di questo approccio è la praticità. L’unità SDDWP è un piccolo assemblato in gran parte monolitico che si avvita alla porta laterale di un microscopio a fluorescenza invertito standard e richiede solo un’allineamento modesto. Il suo design basato su prismi spreca molti meno fotoni rispetto alle reticoli di diffrazione ed è meccanicamente abbastanza stabile da restare calibrato per lunghi periodi con controlli di routine. Questo lo rende un percorso di aggiornamento realistico per molti laboratori esistenti che lavorano con singole molecole.
Cosa significa per la microscopia futura
Rivedendo il modo in cui la luce viene divisa e ricombinata, questo lavoro dimostra che è possibile ottenere sia posizioni più nitide sia informazioni cromatiche più chiare dallo stesso limitato insieme di fotoni. In termini pratici, permette agli scienziati di distinguere più tipi di molecole in ambienti affollati e tridimensionali e di tracciare molte particelle etichettate contemporaneamente, senza sacrificare la qualità dell’immagine. Man mano che la tecnica verrà adottata e adattata — potenzialmente anche per l’imaging in cellule vive con luce rossa delicata — potrebbe diventare uno strumento versatile per esplorare come gli assemblaggi molecolari complessi e gli organelli sono organizzati e come si muovono all’interno delle cellule viventi, tutto su scala nanometrica.
Citazione: Yeo, WH., Brenner, B., Shi, M. et al. Maximizing photon utilization in spectroscopic single-molecule localization microscopy using symmetrically dispersed dual-wedge prisms. npj Imaging 4, 20 (2026). https://doi.org/10.1038/s44303-026-00152-z
Parole chiave: microscopia a singola molecola, imaging a super-risoluzione, imaging spettrale, imaging cellulare 3D, tracciamento di singole particelle