Clear Sky Science · it
Tecniche di imaging avanzate per la navigazione intraoperatoria dei tumori
Vedere il cancro più chiaramente in sala operatoria
La chirurgia oncologica spesso si riduce a un delicato compromesso: rimuovere ogni ultima cellula tumorale preservando quanto più tessuto sano possibile. Questo articolo di revisione spiega come una nuova generazione di strumenti di imaging stia aiutando i chirurghi a visualizzare i tumori e i loro margini in tempo reale durante l’intervento. Per un lettore non specialista, l’appello è semplice: queste tecnologie promettono meno interventi ripetuti, rimozioni tumorali più precise e maggiori probabilità di sopravvivenza a lungo termine, fornendo ai chirurghi una “mappa” più chiara mentre operano.
Perché una migliore visione durante l’intervento è importante
Il cancro è ormai una delle principali cause di morte nel mondo, e la chirurgia resta una pietra angolare del trattamento. Eppure anche il chirurgo più abile è stato a lungo limitato da ciò che si può vedere e palpare manualmente, e dalle immagini acquisite giorni o settimane prima dell’operazione. Strumenti tradizionali come ecografia, TC, RM e PET aiutano a pianificare l’intervento, ma spesso sono ingombranti, lenti o non adatti all’uso continuo durante l’operazione. Di conseguenza, può essere difficile stabilire con precisione dove finisca il tumore e inizi il tessuto sano, aumentando il rischio di lasciare cellule tumorali o di asportare troppo tessuto normale. La revisione descrive come l’“imaging intraoperatorio” — immagini in tempo reale utilizzate direttamente in sala operatoria — stia cambiando questo panorama.
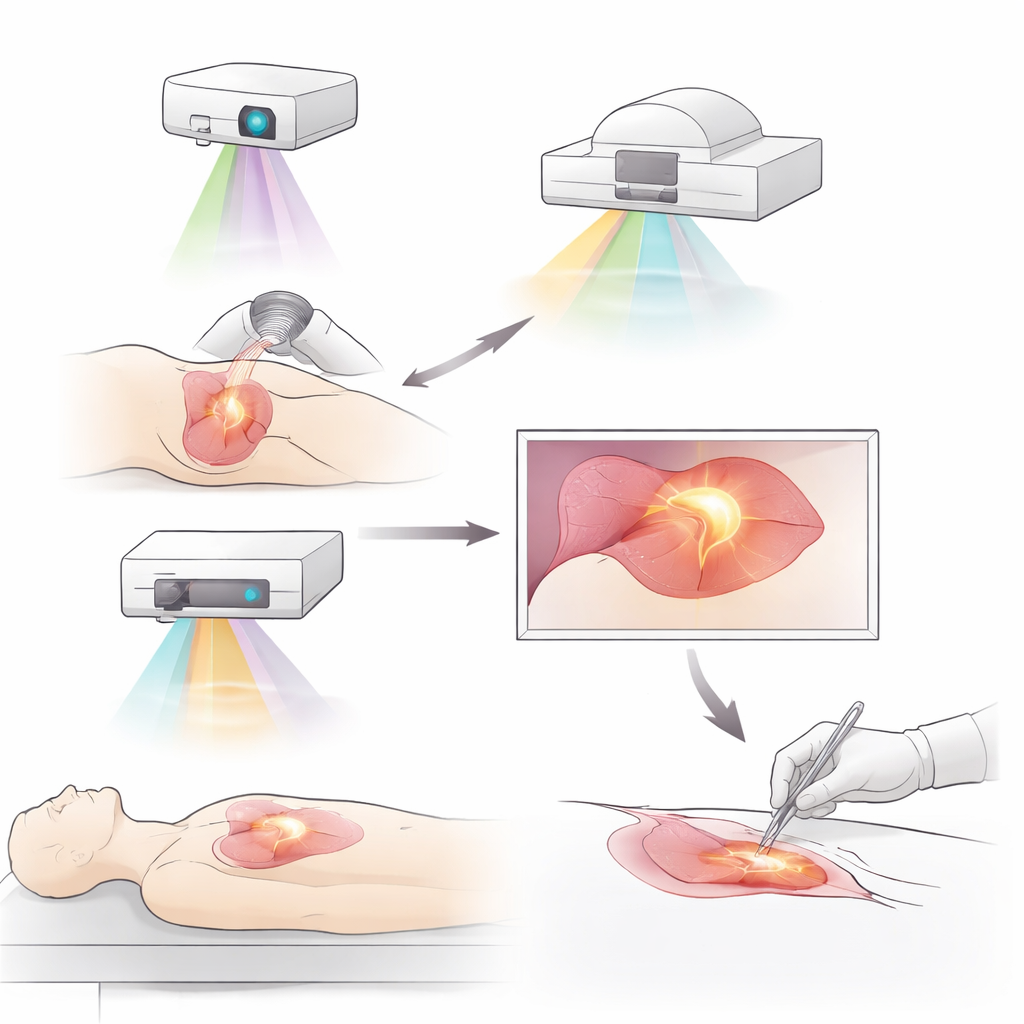
Tumori che brillano e nuovi modi per illuminarli
Un importante progresso è rappresentato dall’imaging a fluorescenza, in cui coloranti speciali o sonde molecolari fanno “brillare” i tumori sotto luce nel vicino infrarosso. Coloranti più datati e non mirati, come l’indocianina verde, hanno già aiutato i chirurghi a delineare i tumori, tracciare i vasi linfatici e individuare i linfonodi critici in tumori di mammella, fegato, polmone e stomaco. Sonde più recenti e mirate arrivano oltre, localizzandosi su molecole sovraespresse dalle cellule tumorali o dall’ambiente circostante. Esempi includono sonde che si legano a recettori per fattori di crescita, checkpoint immunitari o proteine abbondanti nel tessuto di supporto tumorale o nelle regioni ipossiche. Alcuni di questi agenti possono persino essere coniugati a farmaci antitumorali, unendo visualizzazione precisa e terapia nella stessa molecola. I primi studi clinici mostrano che tali traccianti possono rivelare depositi tumorali nascosti e ridurre la necessità di reinterventi dopo interventi conservativi al seno.
Oltre il bagliore: suono, luce e molti colori
Seppure la fluorescenza sia centrale, la revisione evidenzia diversi approcci complementari che mettono in luce aspetti differenti del tumore. L’imaging fotoacustico usa impulsi di luce per generare onde sonore all’interno dei tessuti, combinando la risoluzione dei metodi ottici con la profondità di penetrazione dell’ecografia, ed è stato in grado di rivelare metastasi molto piccole che altre scansioni mancano. L’imaging multispettrale e iperspettrale suddivide la luce in molte bande, catturando sottili differenze nell’assorbimento e nella riflessione dei tessuti; questo può distinguere il tessuto canceroso da quello normale con alta accuratezza in tumori della mammella, del collo dell’utero e gastrointestinali. I progressi nell’ecografia — comprese tecniche che misurano la rigidità dei tessuti — aggiungono informazioni sulla profondità e aiutano a mostrare fino a che punto il cancro ha infiltrato. La spettroscopia Raman, che legge l’“impronta” chimica del tessuto basandosi sul modo in cui le molecole diffondono la luce, offre identificazione senza marcatori e altamente specifica del cancro durante l’intervento, specialmente se combinata con altre modalità.
Costruire mappe 3D e combinare più viste
Un altro tema dell’articolo è la combinazione delle immagini in viste tridimensionali e multimodali che i chirurghi possano usare in modo intuitivo. Ricostruzioni tridimensionali di vasi sanguigni, canali linfatici e organi, sovrapposte a segnali fluorescenti, aiutano a pianificare resezioni segmentarie precise di fegato e polmone e guidano dissezioni linfonodali complesse. Sistemi ibridi che uniscono PET con imaging ottico o associano traccianti di medicina nucleare alla fluorescenza consentono di utilizzare la stessa sonda per la scansione preoperatoria dell’intero corpo e per la guida intraoperatoria. Piattaforme emergenti integrano ablazione laser, tomografia a coerenza ottica e robotica per localizzare e trattare automaticamente le lesioni con elevata precisione. Questi approcci mirano a fornire ai chirurghi sia la “visione d’insieme” della diffusione tumorale sia il dettaglio fine necessario per tagliare seguendo margini sicuri e puliti.
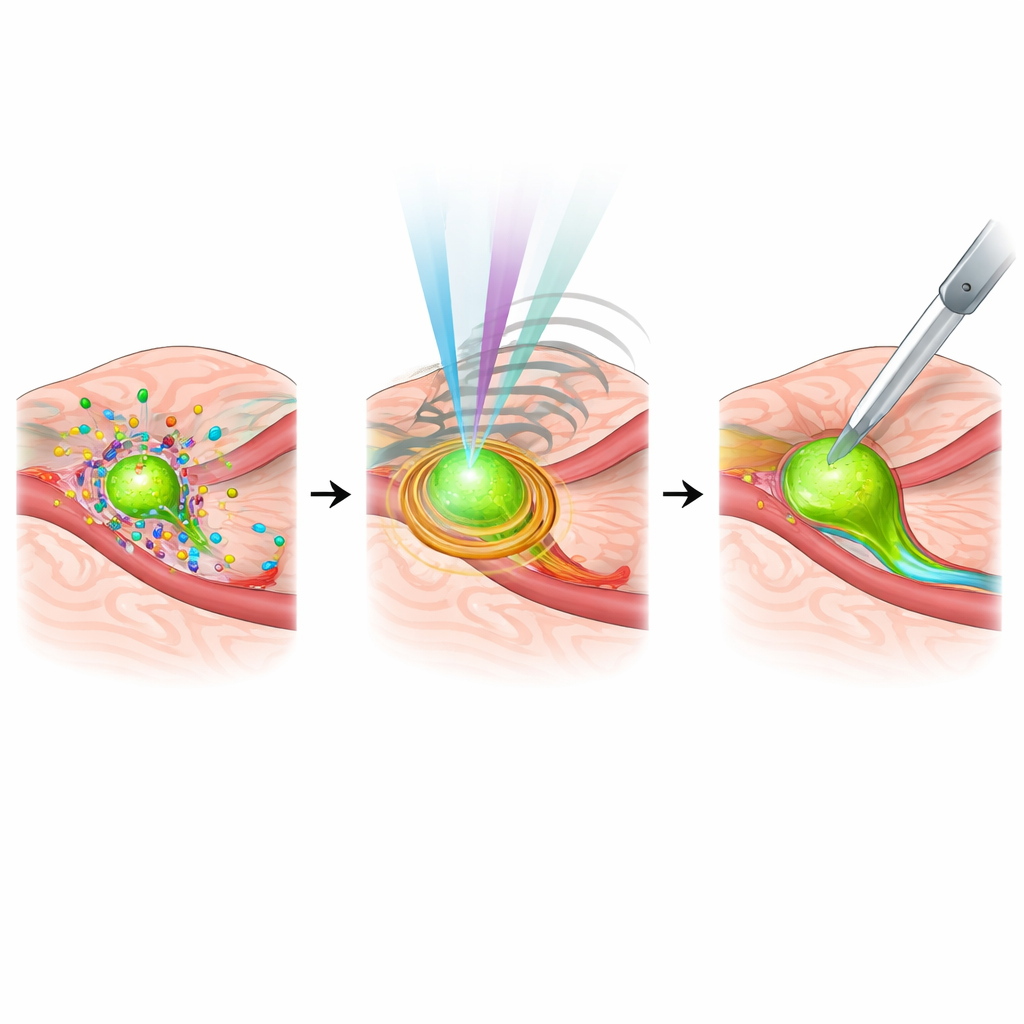
Sistemi più intelligenti, bersagli personalizzati e ostacoli ancora da superare
La revisione guarda anche al ruolo dell’intelligenza artificiale e della medicina personalizzata. Modelli di machine learning stanno già aiutando a distinguere in tempo reale tessuto canceroso da tessuto normale, riconoscere strutture anatomiche critiche e persino prevedere la diffusione ai linfonodi durante la chirurgia pancreatica, riducendo potenzialmente la dipendenza dall’esame patologico rapido. Allo stesso tempo, le sonde di imaging vengono riprogettate per corrispondere alle firme molecolari uniche del tumore di ciascun paziente, collegando le immagini intraoperatorie ai profili genetici e molecolari. Restano tuttavia ostacoli: molti sistemi sono costosi, complessi e difficili da integrare nei flussi di lavoro di routine; alcuni richiedono agenti di contrasto specializzati con profili di sicurezza attentamente gestiti; e gli standard per integrare tutti questi dati nei sistemi di navigazione sono ancora in evoluzione.
Cosa significa questo per i pazienti
In termini accessibili, la conclusione dell’articolo è che i chirurghi stanno ottenendo qualcosa che non hanno mai veramente avuto prima: la capacità di vedere il cancro vivo con grande chiarezza mentre operano. Illuminando i tumori, leggendo la loro chimica, mappandoli in 3D e combinando più tipi di immagini — spesso coadiuvati dall’IA — questi strumenti possono contribuire a garantire che venga rimossa più massa tumorale e che venga preservato più tessuto sano. Sebbene costi, formazione e lacune tecnologiche debbano essere affrontati prima che tali sistemi siano ampiamente disponibili, la direzione è chiara. L’imaging intraoperatorio avanzato è destinato a diventare una componente chiave della chirurgia oncologica standard, offrendo ai pazienti interventi più precisi, meno recidive e maggiori possibilità di controllo a lungo termine.
Citazione: Li, K., Zhang, Y., Yang, H. et al. Advanced imaging techniques for tumor intraoperative navigation imaging. npj Imaging 4, 18 (2026). https://doi.org/10.1038/s44303-026-00150-1
Parole chiave: imaging intraoperatorio, chirurgia guidata da fluorescenza, rilevamento dei margini tumorali, imaging multimodale del cancro, imaging fotoacustico