Clear Sky Science · it
Imaging multimodale correlativa per la mappatura spaziale su scala microscopica delle interazioni tra collagene e attività genica nei tessuti umani
Perché osservare l'interno dei muscoli è importante
Le malattie che cicatrizzano lentamente i nostri organi, come la distrofia muscolare di Duchenne (DMD), si sviluppano a scale troppo piccole per l'occhio nudo. L'attività genica avviene all'interno di singole cellule, mentre il tessuto di supporto intorno a esse è costituito da sottili fibre proteiche. Finora, gli scienziati raramente hanno potuto osservare questi due mondi insieme nella stessa sezione di tessuto umano. Questo studio introduce un modo per farlo, rivelando come i messaggi dei geni e l'impalcatura strutturale del corpo interagiscono a livello microscopico.
Due “fotocamere” sulla stessa porzione di tessuto
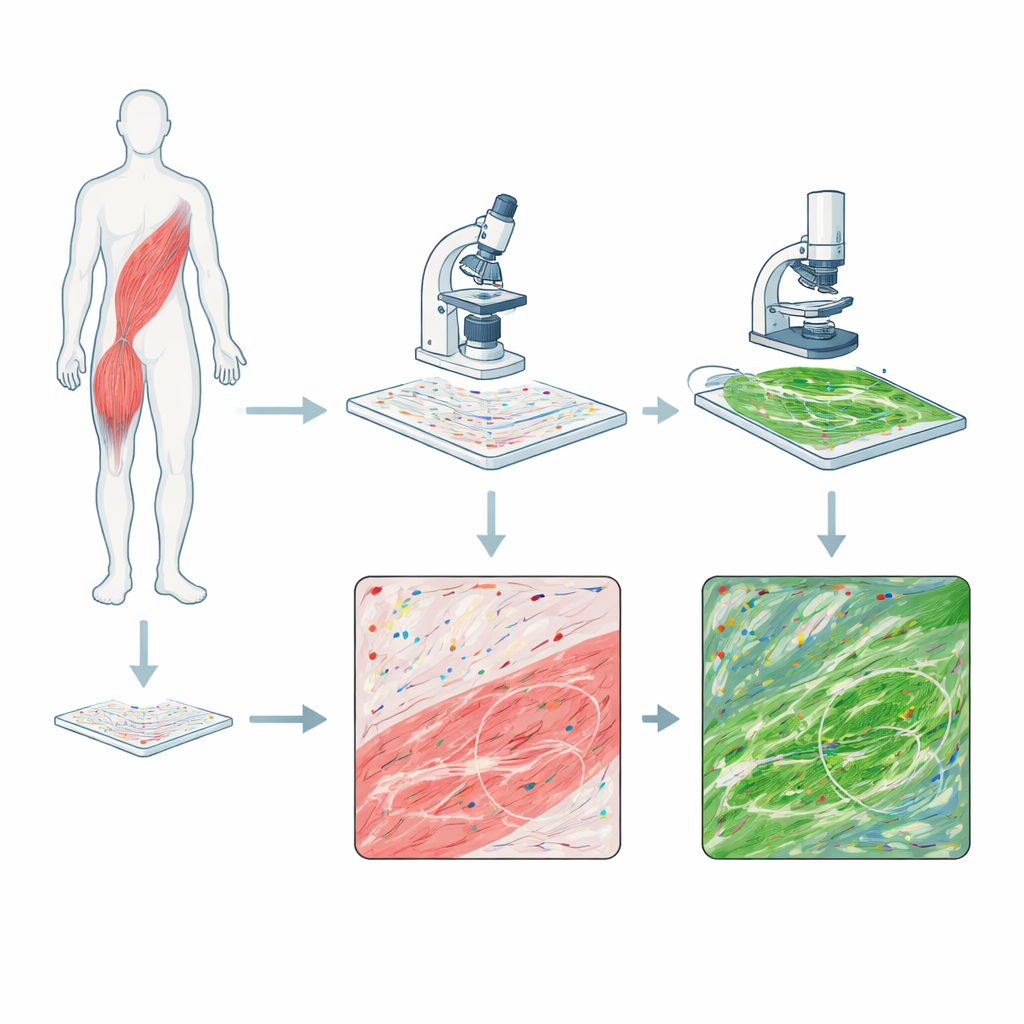
I ricercatori hanno combinato due potenti metodi di imaging su sezioni singole di biopsie del muscolo scheletrico umano provenienti da persone con DMD e da un volontario sano. Un metodo, chiamato RNAscope, colora singole molecole di RNA—le copie operative dei geni—come puntini colorati, mostrando dove sono presenti specifici messaggi genetici. Il secondo metodo, la microscopia multiphotonica, usa luce laser per far brillare le fibre di collagene nel tessuto senza aggiungere coloranti, catturando l'architettura del tessuto connettivo che si ispessisce durante la cicatrizzazione e la fibrosi. Fotografando prima i segnali di RNA e poi quelli del collagene sulla stessa vetrino, hanno potuto allineare le due immagini in modo che ogni puntino di attività genica potesse essere confrontato con la rete di fibre circostante, pixel per pixel.
Quello che le singole viste già ci dicono
L'osservazione separata di ciascun metodo di imaging ha già evidenziato chiare differenze tra muscolo malato e sano. RNAscope ha mostrato che i muscoli dei pazienti con DMD contenevano meno trascritti di distrofina—i messaggi RNA necessari per produrre la proteina distrofina assente—rispetto al campione sano. I segnali residui differivano anche per dimensione a seconda della porzione del gene bersagliata, suggerendo differenze nel modo in cui il lungo messaggio della distrofina viene processato. Nel frattempo, le immagini multiphotoniche hanno mostrato che i muscoli DMD erano pieni di fibre di collagene lunghe e dense, un segno visivo di cicatrizzazione fibrotica, mentre il muscolo sano presentava fibre meno numerose e più uniformemente distribuite. Questi risultati corrispondono all'esperienza clinica: nella DMD, il tessuto muscolare viene gradualmente sostituito da grasso e cicatrice.
Allargando lo sguardo: pattern ampi attraverso il tessuto
Dopo aver registrato digitalmente i due tipi di immagine, il gruppo ha diviso ogni sezione di tessuto in una griglia, trattando ogni quadrato come un piccolo quartiere. In ogni casella hanno misurato sia le caratteristiche del collagene—lunghezza delle fibre, orientamento e quanto le fibre fossero tortuose o dritte—sia la densità locale di puntini di RNA di distrofina. Questa vista a «mappa di calore» ha rivelato variazioni a macchie, da regione a regione, sia nell'attività genica sia nella struttura del collagene all'interno del muscolo DMD. Tuttavia, quando queste misure sono state confrontate con test statistici, l'abbondanza di trascritti e le proprietà del collagene non hanno mostrato quasi nessuna relazione coerente a questa scala grossolana. In altre parole, mediando su regioni relativamente ampie, le aree ricche di RNA di distrofina non erano in modo affidabile più o meno fibrotiche rispetto alle aree con meno segnali di RNA.
Avvicinandosi: relazioni alla scala cellulare
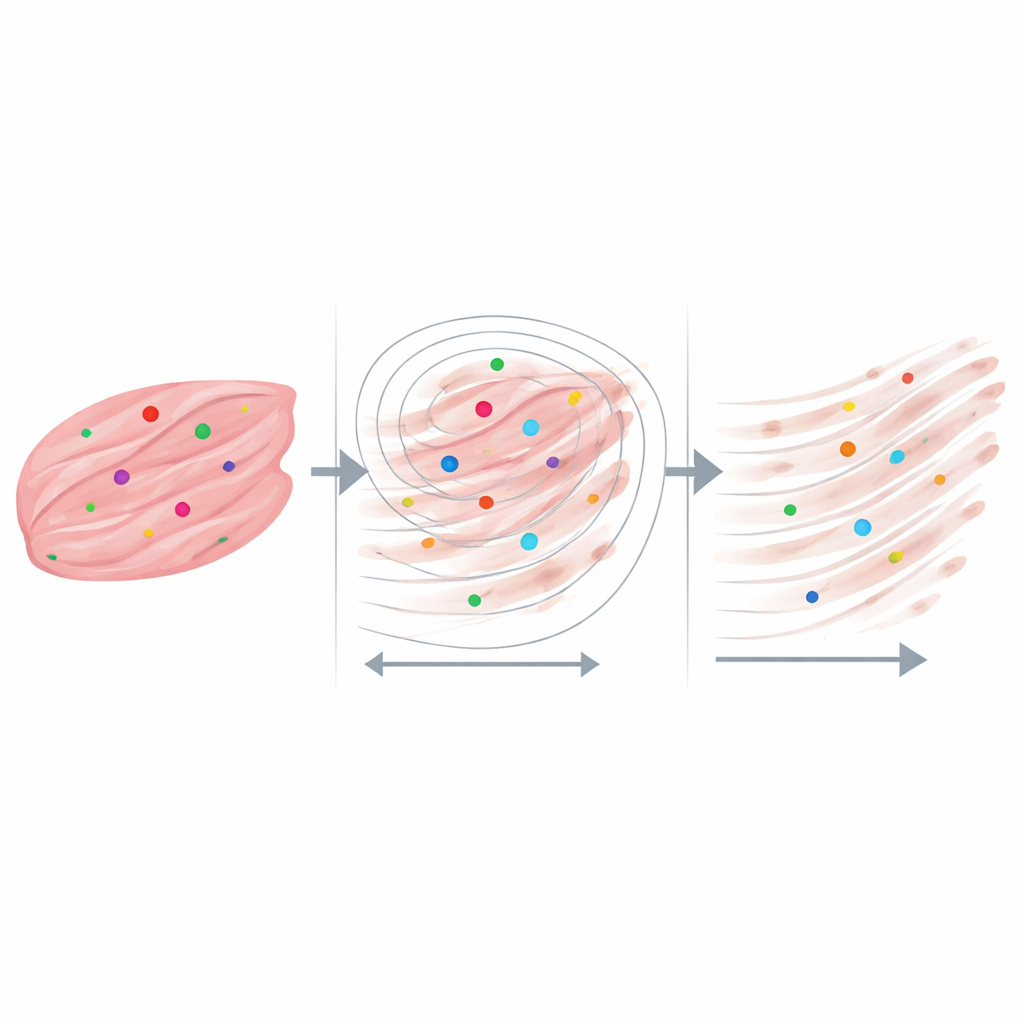
I risultati più rivelatori sono emersi quando gli scienziati si sono concentrati su quartieri misurati in poche decine di micrometri—all'incirca la dimensione delle singole fibre muscolari e del loro immediato intorno. Per ogni puntino di RNA, hanno tracciato una serie di cerchi concentrici crescenti e hanno valutato quante fibre di collagene si trovassero all'interno e quanto fossero lunghe quelle fibre. Sia nei tessuti DMD sia in quelli sani, le fibre di collagene risultavano più lunghe proprio accanto ai segnali di RNA di distrofina e diventavano progressivamente più corte all'aumentare della distanza. Nei campioni maggiormente cicatrizzati, i puntini di trascritto avevano quasi sempre collagene nelle immediate vicinanze, anche a distanze molto piccole, mentre nel campione sano molti puntini di RNA si trovavano in regioni con poco o nessun collagene vicino. Analisi di controllo con punti collocati casualmente e impostazioni leggermente modificate dell'elaborazione delle immagini hanno mostrato che questo schema non può essere spiegato semplicemente dal caso o da particolarità del software.
Cosa potrebbe significare per le malattie muscolari e oltre
Questi risultati suggeriscono che legami importanti tra i messaggi genici e la struttura tissutale possono essere nascosti quando si guardano solo grandi medie, ma diventano visibili se esaminati a livello cellulare. In questo studio pilota, le regioni ricche di specifici trascritti di distrofina tendevano a trovarsi vicino a fibre di collagene più lunghe e dense, lasciando intendere che l'attività genica locale e il rimodellamento fibrotico possano influenzarsi reciprocamente all'interno di microambienti ristretti del muscolo. Gli autori precisano che il gruppo di pazienti è piccolo e il lavoro non è ancora un test clinico. Piuttosto, presentano una piattaforma flessibile che può essere estesa ad altri geni, tipi di tessuto e metodi di imaging. Collegando dove i geni sono attivi e come è costruita l'impalcatura tissutale, questo approccio apre la strada alla scoperta di nuovi biomarcatori spaziali di fibrosi, rigenerazione e risposte alle emergenti terapie a base di RNA.
Citazione: Scodellaro, R., Mietto, M., Ferlini, A. et al. Correlative multimodal imaging for microscale spatial mapping of collagen-gene activity interactions in human tissues. npj Imaging 4, 17 (2026). https://doi.org/10.1038/s44303-026-00149-8
Parole chiave: imaging multimodale, distrofia muscolare di Duchenne, fibrosi da collagene, espressione genica spaziale, biopsia del muscolo scheletrico