Clear Sky Science · it
Una strategia di radiomarcatura in un unico passaggio per PET, SPECT e radionuclidi terapeutici usando nanoparticelle come chelante universale
Perché le particelle radioattive microscopiche contano
La medicina oncologica moderna si affida sempre più alla capacità di visualizzare e trattare i tumori con farmaci radioattivi che li rendono visibili nelle scansioni e, in alcuni casi, li distruggono dall’interno. Tuttavia, la creazione di ogni nuovo medicinale radioattivo è lenta e complessa, perché la maggior parte dei progetti deve essere costruita su misura attorno a un metallo radioattivo specifico. Questo studio esplora un approccio molto diverso: usare un unico tipo di nanoparticella a base di ferro come una “presa universale” in grado di ospitare molti isotopi medici diversi per imaging e terapia, accelerando potenzialmente la realizzazione e la messa a punto di questi farmaci.
Da molte chiavi a una sola serratura
I farmaci radioattivi odierni si basano solitamente su artigli chimici chiamati chelanti che afferrano atomi metallici e li collegano ad anticorpi o altri vettori mirati. Ogni metallo radioattivo tende a richiedere il proprio chelante e la propria ricetta—condizioni come temperatura, acidità e tempi di reazione variano. Per alcuni metalli di grande interesse medico, in particolare quelli usati per potenti terapie con particelle alfa, non esiste ancora un chelante ideale. Gli autori sostengono che questo approccio metallo‑per‑metallo sia diventato un collo di bottiglia: la lista di isotopi utili continua a crescere, ma la chimica per gestirli in sicurezza non riesce a stare al passo.
Nanoparticelle come presa universale
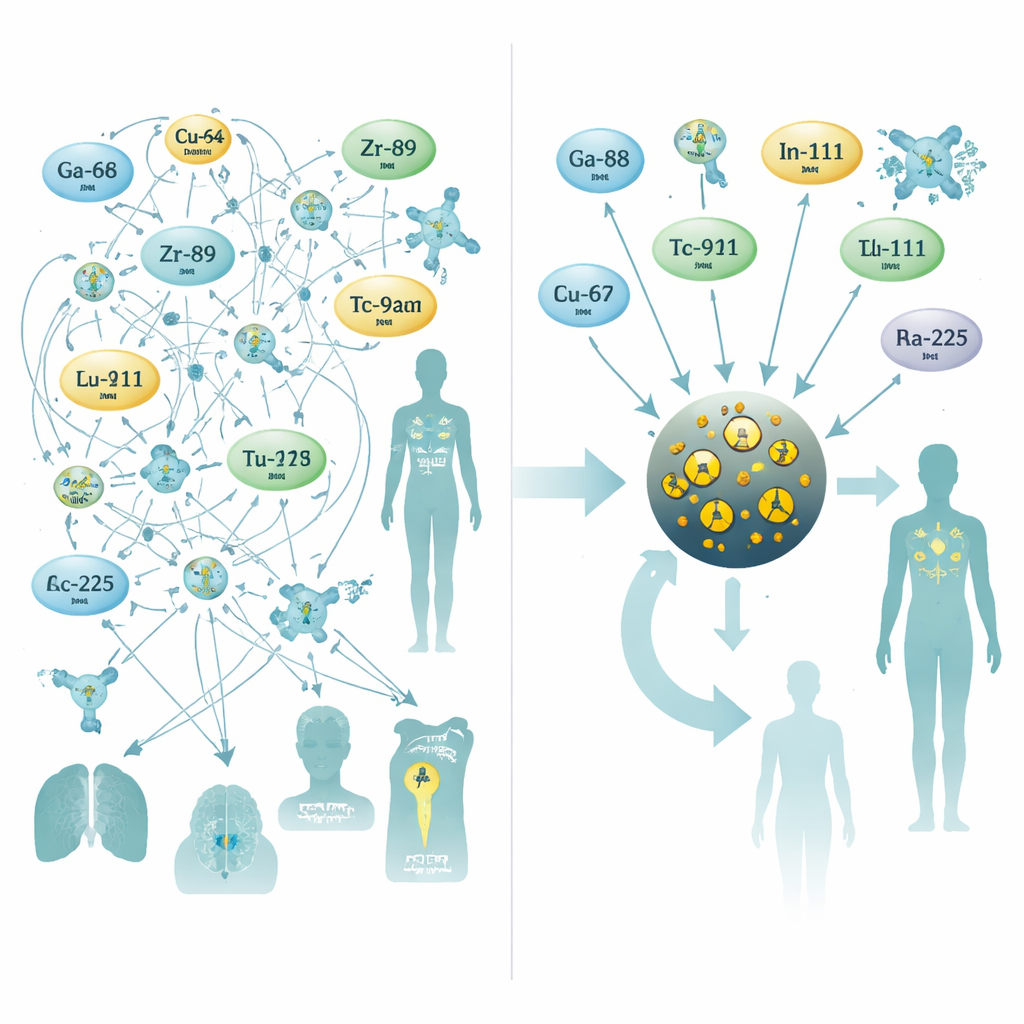
Per affrontare il problema i ricercatori hanno utilizzato nanoparticelle di ossido di ferro di dimensioni molto piccole, un materiale già studiato come mezzo di contrasto per la risonanza magnetica. Hanno progettato particelle con un nucleo di ossido di ferro di circa tre nanometri, rivestite da una pellicola di molecole di citrato che le mantiene stabili nel flusso sanguigno. Durante un unico passaggio di sintesi assistita da microonde della durata di 10 minuti, hanno drogato il nucleo con uno dei dieci diversi metalli radioattivi comunemente impiegati per PET, SPECT o radioterapia interna. Questo processo in una sola fase ha prodotto particelle di dimensioni costanti con rese elevate e, cosa cruciale, eccellente stabilità nel siero umano—anche per isotopi terapeutici difficili come il radio‑223 e l’attinio‑225, i cui prodotti di decadimento spesso sfuggono ai chelanti tradizionali.
Imaging di coaguli e tumori cerebrali
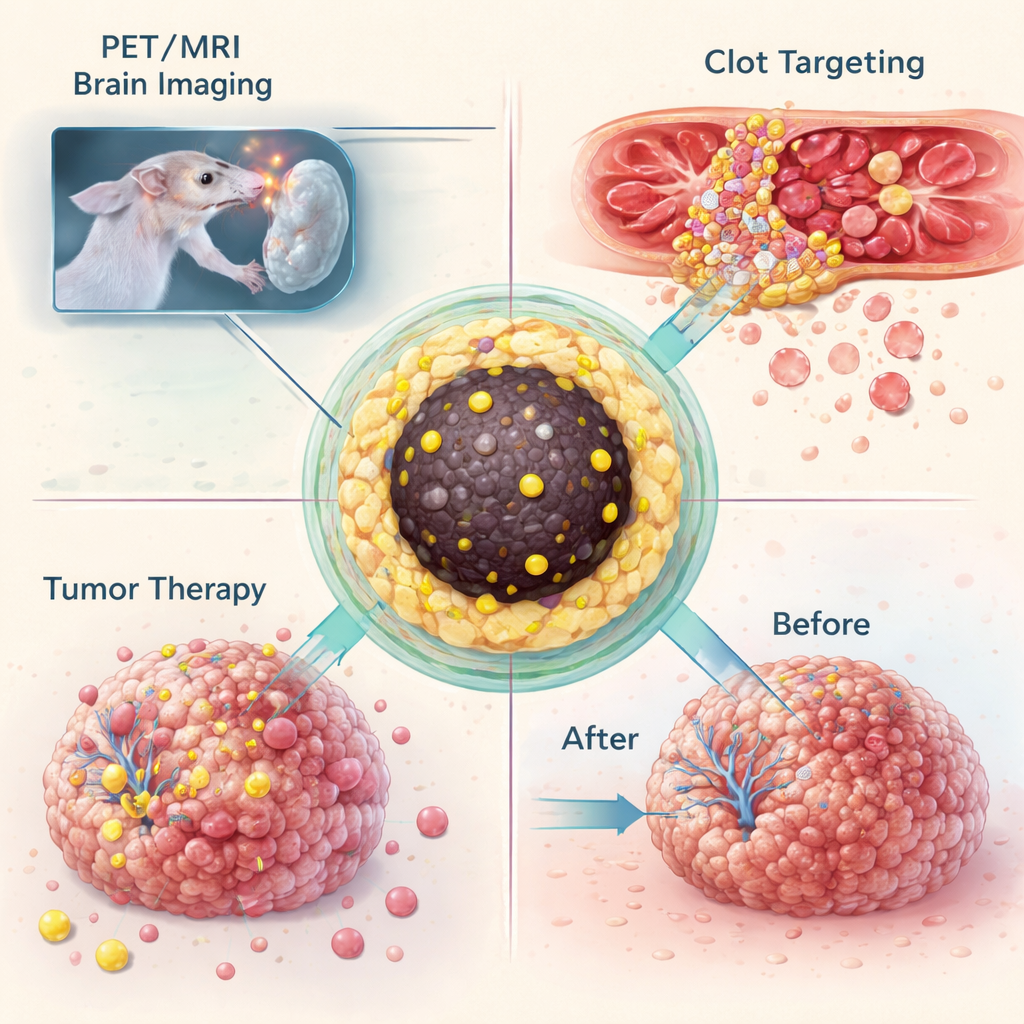
Dopo aver mostrato di poter intrappolare molti isotopi diversi nello stesso progetto di nanoparticella, il team ha testato cosa possono fare questi “nanotraccianti” in animali vivi. In un modello murino di glioblastoma, un tumore cerebrale letale, particelle marcate con gallio‑68 sono state iniettate in circolo e immaginate con PET combinata a MRI. Le particelle si sono accumulate nei tumori sufficientemente grandi da compromettere la barriera emato‑encefalica, permettendo alla stessa formulazione di fornire sia un contrasto MRI brillante sia un segnale PET sensibile. In un esperimento separato, le particelle sono state modificate chimicamente per potersi legare tramite una reazione click altamente selettiva a un anticorpo che riconosce piastrine attivate all’interno dei coaguli. In topi con lesione della carotide, questa strategia a due passi di “pretargeting” ha prodotto segnali PET chiari nel sito del coagulo, mentre gli animali di controllo non mostravano alcun hotspot.
Dalla diagnosi al trattamento e a una clearance più sicura
La stessa piattaforma è stata impiegata anche per la somministrazione di terapie. Quando nanoparticelle caricate con lutetio‑177 sono state iniettate direttamente nei tumori da glioblastoma nei topi, le particelle sono rimaste per lo più confinate alla massa tumorale per almeno due settimane. In quel periodo, i tumori non trattati sono cresciuti fino a raggiungere diverse volte la dimensione iniziale, mentre i tumori trattati hanno smesso di crescere, suggerendo che la dose di radiazione localizzata fosse sufficiente a fermare la progressione. Poiché trattamenti ripetuti potrebbero sovraccaricare fegato e milza di ferro, il team ha poi modificato le condizioni di sintesi per ottenere particelle ancora più piccole—intorno a quattro‑cinque nanometri—sufficientemente piccole da poter essere filtrate dai reni. Queste particelle ridotte mantenevano comunque saldamente il loro carico radioattivo ma venivano escrete rapidamente nella vescica, riducendo l’accumulo a lungo termine negli organi principali.
Cosa potrebbe significare per la cura del cancro in futuro
Per i non specialisti, il messaggio chiave è che i ricercatori hanno costruito una piattaforma di nanoparticelle unica e flessibile che può essere abbinata a molti metalli radioattivi diversi senza dover reinventare la chimica ogni volta. Nei modelli animali, la stessa particella di base può aiutare a individuare tumori cerebrali, evidenziare coaguli di sangue, somministrare radiazione direttamente nei tumori e persino essere adattata per uscire dall’organismo attraverso i reni. Pur richiedendo ulteriori studi prima di arrivare ai pazienti, questo approccio offre una strada promettente per progettare famiglie di agenti diagnostici e terapeutici con comportamento corporeo coerente, che differiscono solo per il tipo di radiazione che trasportano. Tale coerenza potrebbe semplificare lo sviluppo, migliorare i test di sicurezza e in ultima analisi rendere gli strumenti avanzati della medicina nucleare più accessibili su larga scala.
Citazione: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
Parole chiave: radiotheranostics, nanoparticelle, imaging PET, glioblastoma, radioterapia mirata