Clear Sky Science · it
Sinucleinopatia accelerata e localizzata in un modello murino ibrido: implicazioni per studi con tomografia a emissione di positroni
Perché questa ricerca è importante
La malattia di Parkinson è più nota per i tremori e i problemi di movimento, ma nel cervello comincia con piccole alterazioni difficili da osservare. I medici hanno bisogno con urgenza di metodi per individuare questi cambiamenti in fase precoce e per testare rapidamente nuovi farmaci. Questo studio descrive un modello murino perfezionato che riproduce caratteristiche chiave del danno cerebrale simile al Parkinson in poche settimane e in una regione cerebrale molto specifica, pensato appositamente per l’uso con scansioni cerebrali avanzate chiamate imaging PET. 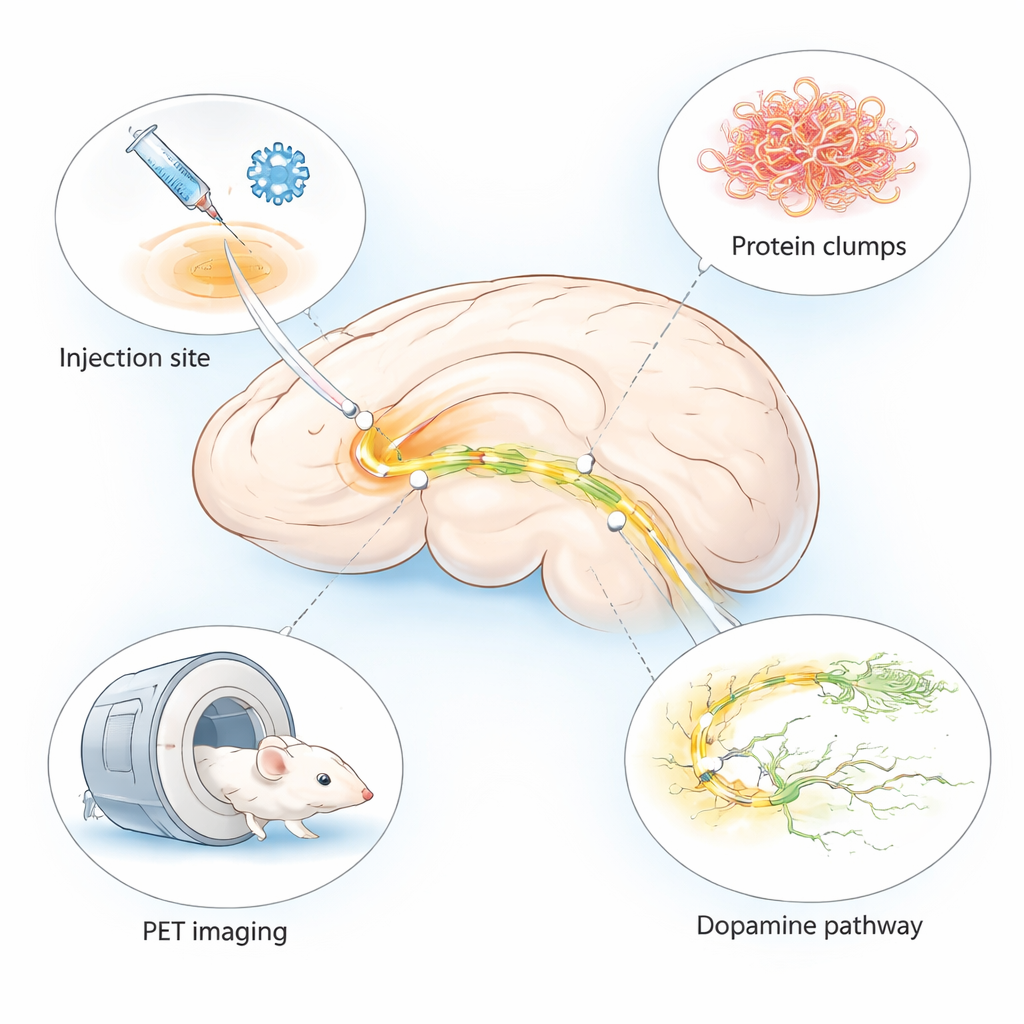
Costruire un modello di malattia più veloce e mirato
Molti modelli animali esistenti della malattia di Parkinson impiegano mesi per sviluppare sintomi o non mostrano l’intera gamma di cambiamenti cerebrali osservati nei pazienti. Gli autori hanno combinato due approcci consolidati in un unico modello “ibrido”. Hanno iniettato un virus innocuo che induce le cellule cerebrali a produrre alfa‑sinucleina umana — una proteina che tende ad aggregarsi nel Parkinson — insieme a fibrille preformate, che fungono da semi che innescano ulteriori aggregazioni. Entrambi sono stati somministrati in una piccola regione legata al movimento chiamata substantia nigra da un lato del cervello del topo. Questo disegno produce alterazioni locali ma intense simili alla malattia sul lato iniettato, mentre l’altro lato rimane relativamente sano per il confronto.
Monitorare gli aggregati proteici e la morte dei neuroni
Entro appena due settimane dall’iniezione, i topi hanno mostrato alti livelli di alfa‑sinucleina umana e della sua forma anomala fosforilata nell’area cerebrale bersaglio. Al microscopio, i ricercatori hanno osservato strutture somiglianti ai corpi di Lewy e ai neuriti di Lewy, che sono segni distintivi della malattia di Parkinson. Nelle settimane successive questi depositi anomali sono aumentati. Contemporaneamente, i neuroni che producono il messaggero chimico dopamina — cruciale per movimenti fluidi — hanno cominciato a scomparire. I marcatori di queste cellule sono scesi a circa il 60 percento del livello osservato sul lato intatto entro la quinta settimana, confermando una perdita progressiva e netta del sistema dopaminergico.
Infiammazione, sinapsi in declino e centrali energetiche esauste
Le cellule immunitarie del cervello, chiamate microglia, si sono inoltre attivate in uno stato altamente infiammatorio attorno alla regione danneggiata. Le colorazioni per diverse proteine legate all’infiammazione erano molto più intense vicino ai depositi di alfa‑sinucleina rispetto al lato opposto del cervello. In una fase successiva, il gruppo ha rilevato una perdita di sinapsi — i minuscoli punti di contatto dove i neuroni comunicano — e segni che i mitocondri, le centrali energetiche delle cellule, non funzionavano correttamente. Nel loro insieme, questi risultati mostrano che il modello non genera solo aggregati proteici; cattura anche la reazione a catena di infiammazione, deterioramento delle connessioni e problemi energetici che contribuiscono alla morte neuronale nella malattia di Parkinson. 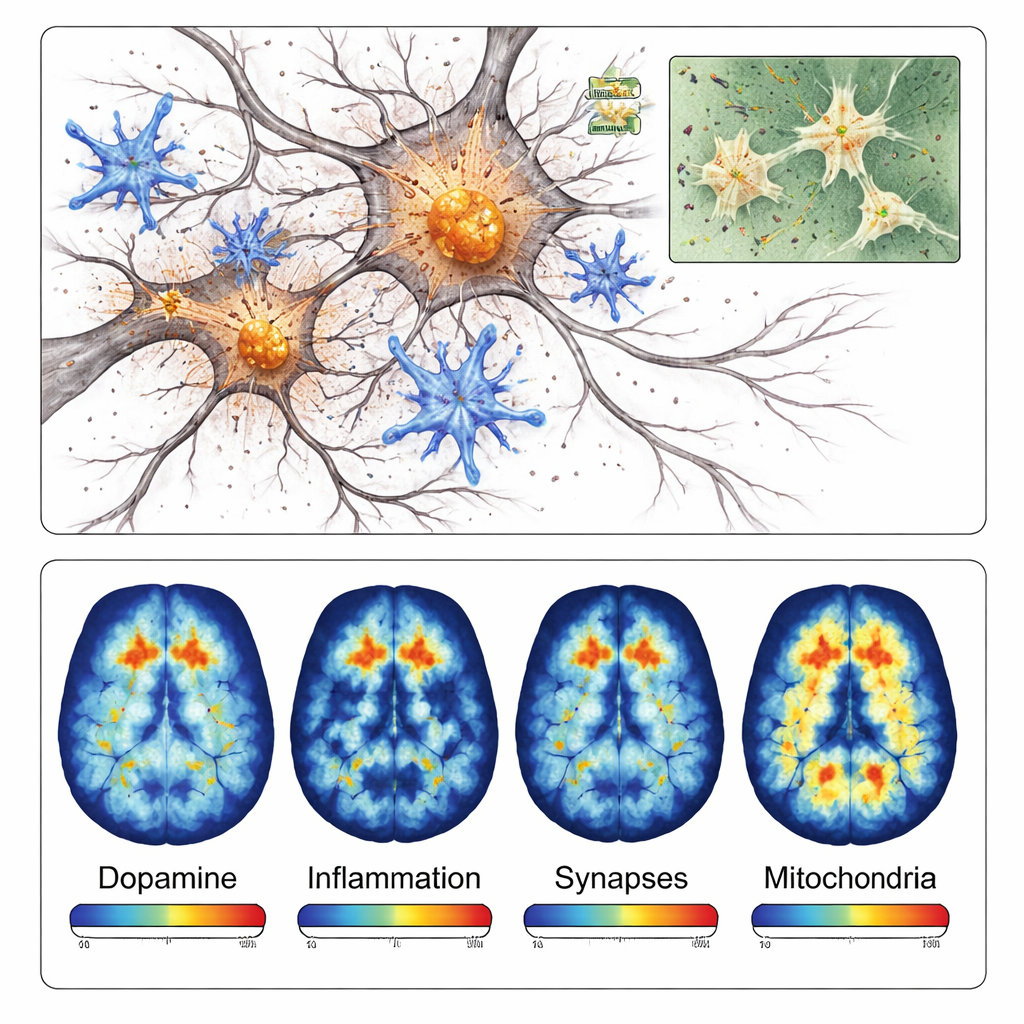
Mettere i tomografi PET al lavoro
Poiché questo modello è localizzato e si sviluppa rapidamente, è particolarmente adatto alla tomografia a emissione di positroni (PET), una tecnica di scansione che può misurare molecole specifiche nei cervelli viventi. I ricercatori hanno testato quattro diversi traccianti PET che si legano alle terminazioni nervose dopaminergiche, alle microglia infiammatorie, a proteine sinaptiche e a enzimi mitocondriali. In ogni caso, le scansioni PET hanno mostrato segnali più bassi o più alti sul lato iniettato in modi coerenti con i riscontri microscopici. Per esempio, il tracciante diretto alle vie dopaminergiche ha mostrato circa il 40 percento in meno di segnale sul lato danneggiato, mentre il tracciante per l’infiammazione ha mostrato oltre il 40 percento di segnale in più nella regione interessata.
Cosa significa per i pazienti e i trattamenti futuri
Questo nuovo modello murino riunisce, in un arco di tempo breve, molte delle modifiche chiave che si verificano nell’arco di anni nei cervelli delle persone con malattia di Parkinson. Poiché il danno è confinato a un’area piccola e ben definita e può essere seguito con scansioni PET, i ricercatori possono testare in modo più efficiente nuovi traccianti di imaging e potenziali terapie. Pur sapendo che nessun topo può riprodurre completamente la condizione umana, questo approccio offre uno strumento potente e pratico per colmare il divario tra il lavoro di laboratorio di base e gli studi sull’uomo, aiutando in ultima analisi a perfezionare la diagnosi e ad accelerare la ricerca di trattamenti migliori.
Citazione: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
Parole chiave: Malattia di Parkinson, alfa-sinucleina, sinucleinopatia, imaging PET, modello murino