Clear Sky Science · it
Modelli a equazioni differenziali ordinarie della dinamica di replicazione di SARS-CoV-2 ed efficacia degli antivirali
Perché i numeri contano per un nuovo virus
Quando è emerso il COVID-19, i medici potevano osservare gli effetti del virus sui pazienti, ma non potevano prevedere con facilità chi sarebbe diventato gravemente malato né quando un farmaco avrebbe dato il massimo beneficio. Questo articolo di revisione esamina come i ricercatori hanno trasformato le misurazioni virali provenienti da pazienti, animali e colture cellulari in “film” matematici dell’infezione all’interno del corpo. Questi modelli usano equazioni per seguire la crescita del virus, la reazione delle nostre cellule e del sistema immunitario e il modo in cui antivirali e vaccini possono far pendere la bilancia a nostro favore.
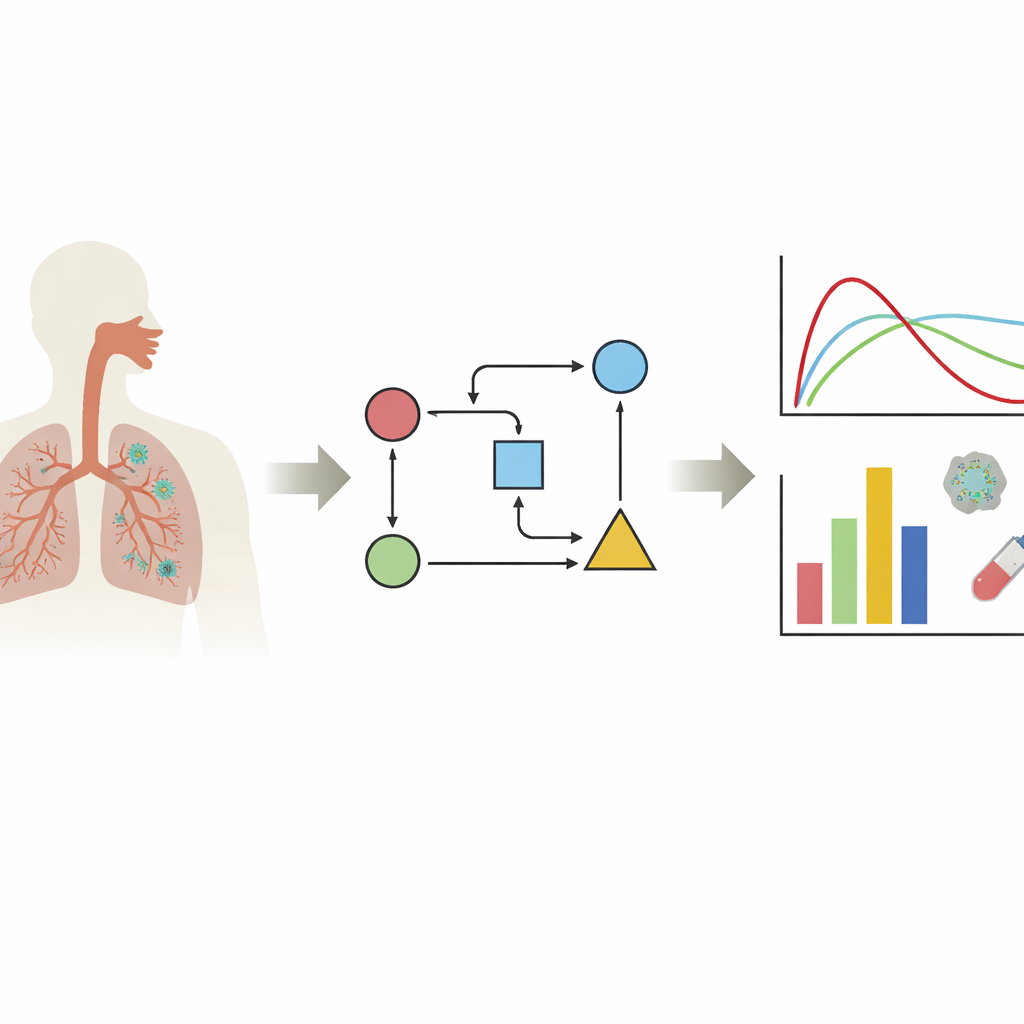
Seguire il virus all’interno del corpo
Gli autori si concentrano su una famiglia di modelli chiamati modelli a cellule bersaglio limitate. In termini semplici, questi modelli tracciano tre attori principali: le cellule sane suscettibili all’infezione, le cellule già infette e le particelle virali libere. Inserendo nei modelli dati reali sui livelli virali, i ricercatori possono stimare caratteristiche nascoste dell’infezione: quanto rapidamente il virus infetta le cellule, quanto a lungo una cellula infetta produce virus e quanto velocemente il virus viene eliminato. La revisione mostra che la maggior parte dei lavori si concentra sui tessuti più rilevanti per il COVID-19—naso e vie aeree superiori e inferiori—mentre sono pochi i modelli che esaminano altri organi. Un messaggio chiave è che il comportamento del virus può apparire molto diverso a seconda del tessuto studiato, della variante virale e della linea cellulare di laboratorio utilizzata, quindi non esiste una curva d’infezione “tipica” unica.
Cosa impariamo sul sistema immunitario
Molti modelli aggiungono livelli che rappresentano le prime difese del sistema immunitario e la sua risposta più lenta e mirata. Studi focalizzati sulla prima linea di difesa suggeriscono che un’attività rapida e ben temporizzata delle cellule del sistema innato e delle molecole di segnalazione può attenuare l’infezione, ma raramente la elimina da sola. Altri lavori evidenziano il ruolo cruciale delle cellule T e degli anticorpi nel mettere infine il virus sotto controllo. I modelli catturano anche un lato oscuro: se la risposta immune mirata è tardiva o mal orientata, gli stessi strumenti che dovrebbero proteggerci possono alimentare dannose “tempeste di citochine”, in cui segnali infiammatori in eccesso danneggiano i tessuti sani. In queste simulazioni, il sottile equilibrio tra attività immune utile e dannosa spesso decide se la malattia rimane lieve o diventa pericolosa per la vita.
Quando farmaci e vaccini funzionano meglio
Poiché le equazioni possono essere eseguite ripetutamente con assunzioni diverse, sono strumenti potenti per testare strategie terapeutiche al computer prima di provarle sull’uomo. In molti studi, i modelli coincidono su un punto centrale: gli antivirali funzionano meglio se somministrati molto precocemente, prima che il virus abbia raggiunto il picco e infettato la maggior parte delle cellule disponibili. I trattamenti che bloccano la replicazione del materiale genetico virale risultano particolarmente promettenti, soprattutto se combinati con altri farmaci che agiscono mediante meccanismi diversi. Il trattamento tardivo, al contrario, tende ad avere scarso impatto nelle simulazioni a meno che non vengano usati insieme diversi farmaci potenti. La vaccinazione è costantemente prevista come superiore ai soli farmaci, principalmente perché prepara il sistema immunitario a riconoscere rapidamente il virus e a limitare il periodo di alti livelli virali.
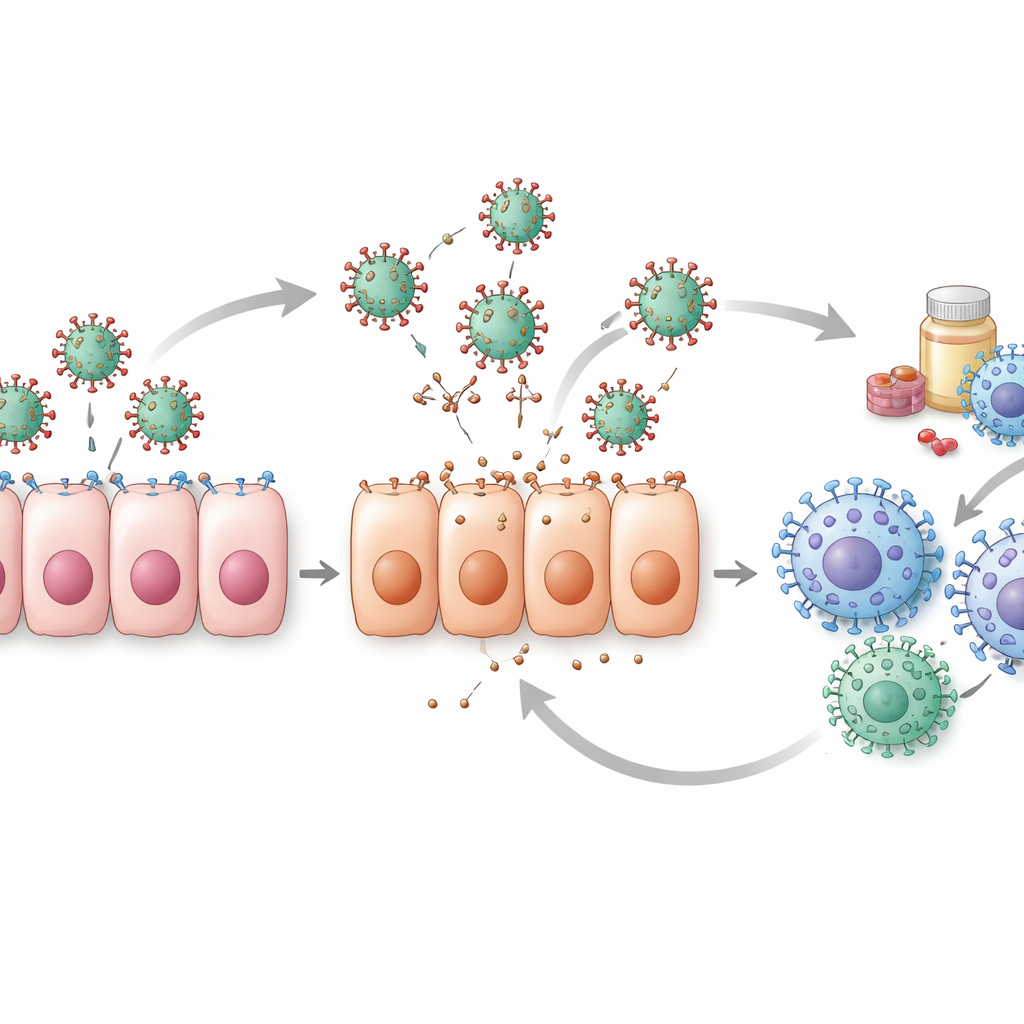
Sfide nascoste nei dati
La revisione mette anche in luce le debolezze dietro i numeri. La maggior parte dei set di dati clinici parte solo dopo che le persone si sentono già malate, il che significa che i modelli spesso perdono i primi giorni cruciali di infezione quando i livelli virali aumentano più rapidamente. In assenza di quelle misurazioni precoci, diverse combinazioni di parametri del modello possono spiegare gli stessi dati, rendendo difficile stabilire quale spiegazione sia corretta. Solo una minoranza di studi esegue controlli rigorosi per verificare se le stime dei parametri siano davvero uniche e affidabili. Studi su animali e esperimenti in colture cellulari aiutano a colmare alcune lacune, specialmente per i punti temporali iniziali, ma le differenze tra specie e sistemi di laboratorio ne limitano l’applicabilità diretta agli esseri umani.
Cosa significa per il futuro
Per un non specialista, la sintesi è che modelli matematici costruiti con cura hanno notevolmente migliorato la nostra comprensione di come SARS-CoV-2 si comporta all’interno del corpo e di come tempistica, combinazioni di farmaci e vaccinazione pregresse influenzino gli esiti. I modelli concordano in larga misura sul fatto che un intervento precoce e forte—specialmente tramite vaccinazione e antivirali somministrati tempestivamente—offre al sistema immunitario la migliore possibilità di avere la meglio, mentre risposte ritardate, sia del corpo sia del trattamento, sono associate a malattie più severe. Allo stesso tempo, gli autori sottolineano che questi strumenti valgono tanto quanto i dati che li alimentano. Per prepararsi a future varianti o a nuovi virus, raccomandano campionamenti clinici più ricchi e precoci e misurazioni immunitarie più ampie, in modo che i “numeri dietro l’infezione” possano guidare decisioni più rapide e accurate durante focolai reali.
Citazione: Kapischke, T., Herrmann, S.T., Bertzbach, L.D. et al. Ordinary differential equation models of SARS-CoV-2 replication dynamics and antiviral drug efficacies. npj Viruses 4, 17 (2026). https://doi.org/10.1038/s44298-026-00183-8
Parole chiave: Dinamica virale di SARS-CoV-2, modellizzazione intra-ospite, tempistica della terapia antivirale, risposta immunitaria, vaccinazione COVID-19