Clear Sky Science · it
Riconsiderare il virus Ravn come l'ortomarburgvirus meno noto
Perché un virus poco conosciuto conta
La maggior parte delle persone ha sentito parlare di Ebola, ma molti meno sanno che un gruppo di virus strettamente imparentati, compreso il virus Marburg e il suo più silenzioso parente il virus Ravn, può causare malattie altrettanto letali. Questo articolo di revisione esamina in profondità il virus Ravn: da dove proviene, come circola nei pipistrelli, come provoca malattia nelle persone e cosa stanno facendo gli scienziati per prevenire futuri focolai. Capire questa minaccia meno nota aiuta i responsabili della sanità pubblica e i ricercatori a prepararsi alle epidemie emergenti prima che sfuggano al controllo.
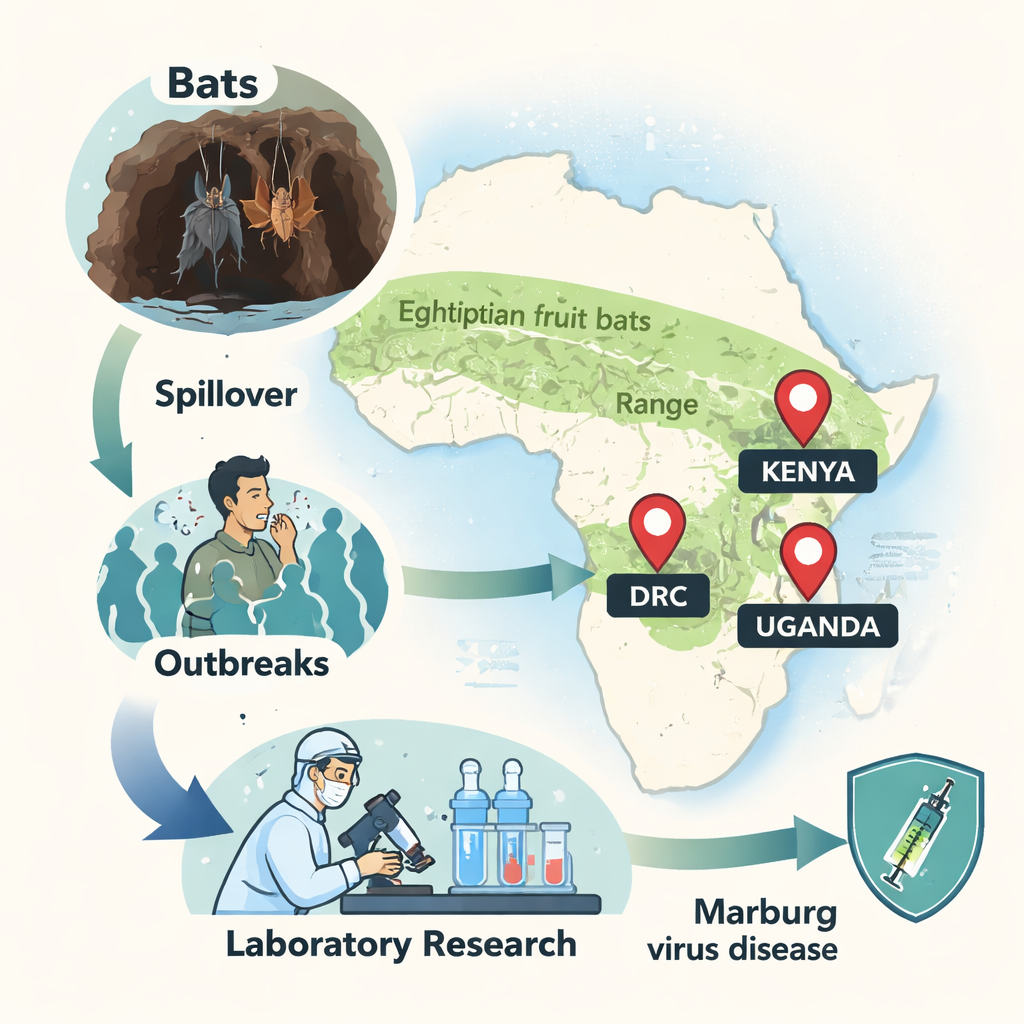
Due parenti mortali, non proprio gemelli
La malattia da virus Marburg è una patologia grave che può provocare febbre, insufficienza d’organo, shock e talvolta emorragie, con tassi di mortalità medi attorno a due terzi dei casi umani documentati. Il virus Ravn appartiene allo stesso gruppo di specie del virus Marburg e provoca una forma molto simile di febbre emorragica nell’uomo, ma il suo patrimonio genetico differisce per poco più di un quinto dei suoi componenti. Può sembrare una differenza piccola, eppure per i virus è un divario significativo che può modificare la modalità di diffusione, il modo in cui il nostro sistema immunitario li riconosce e l’efficacia dei vaccini. Analisi genetiche suggeriscono che i virus Marburg e Ravn si separarono da un antenato comune circa 700 anni fa e hanno seguito percorsi evolutivi distinti da allora.
Focolai ricondotti a grotte e miniere
Dalla prima epidemia riconosciuta di Marburg tra lavoratori di laboratorio in Europa nel 1967, si sono verificati 19 focolai documentati di malattia da virus Marburg in 15 paesi in Africa e oltre, tra cui solo tre con infezioni confermate da virus Ravn. La maggior parte degli eventi è stata ricondotta a grotte o miniere profonde dove le persone trascorrono tempo vicino a grandi colonie di pipistrelli frugivori. Il primo caso noto di Ravn, segnalato in una turista adolescente in Kenya nel 1987, seguì la visita a una grotta piena di pipistrelli. Focolai successivi nella Repubblica Democratica del Congo e in Uganda hanno nuovamente indicato miniere sotterranee, dove molti minatori infetti hanno portato il virus nelle loro famiglie e tra gli operatori sanitari. Tracciamenti genetici attenti hanno mostrato che più lignaggi virali distinti—sia Marburg che Ravn—spesso trasbordano dai pipistrelli agli esseri umani nello stesso luogo e nella stessa stagione, suggerendo salti ripetuti dalla fauna selvatica piuttosto che una singola catena di trasmissione.
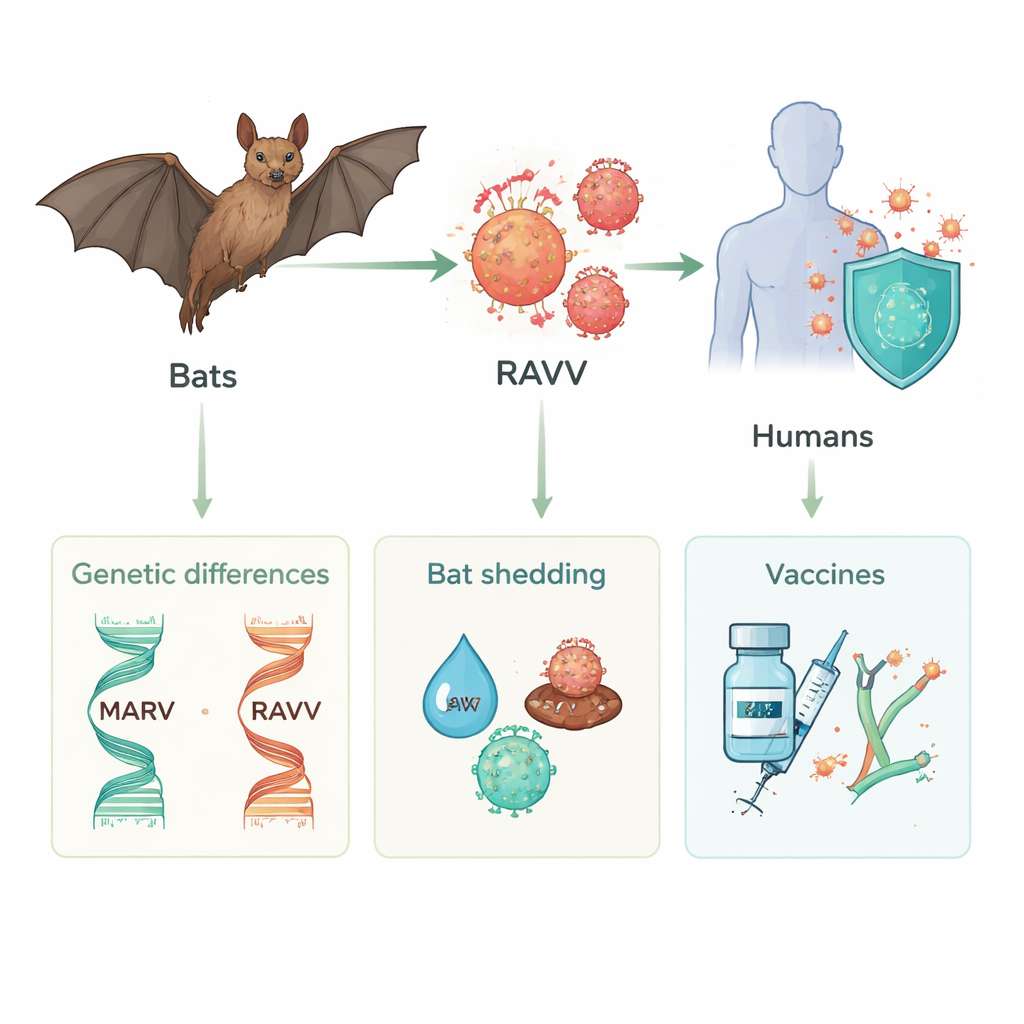
I pipistrelli frugivori come serbatoi nascosti
Studi ecologici e di laboratorio convergono su una conclusione principale: il pipistrello frugivoro Egyptian rousette, che vive nelle grotte, è il serbatoio naturale sia per il virus Marburg sia per il virus Ravn. I ricercatori hanno ripetutamente rilevato materiale genetico virale, virus vivi e anticorpi specifici contro il virus in questi pipistrelli in diversi paesi africani. In esperimenti controllati, i pipistrelli infettati con uno dei due virus mostrano pochi o nessun segno evidente di malattia. Invece, presentano brevi picchi di viriremia e rilasciano virus dalla bocca e dall’intestino, soprattutto attorno alle loro stagioni di nascita semestrali. Lavori recenti che hanno seguito direttamente il virus Ravn nei pipistrelli hanno dimostrato che può persistere ed essere eliminato per giorni tramite saliva ed escrementi, talvolta a livelli più elevati e per periodi più lunghi rispetto al virus Marburg. I pipistrelli sviluppano inoltre memoria immunitaria di lunga durata che previene reinfezioni gravi, il che significa che possono ospitare e trasmettere questi virus senza morire per causa loro.
Cosa rivelano gli esperimenti sugli animali sulla malattia
Poiché sono stati confermati soltanto tre casi umani di Ravn, gli scienziati fanno molto affidamento su modelli animali per capire quanto sia pericoloso e come si comporti in diversi ospiti. Topi comuni e porcellini d’India resistono all’infezione da ceppi naturali, perciò i ricercatori adattano il virus attraverso passaggi ripetuti finché non diventa letale, quindi studiano quali mutazioni compaiono. Questi ceppi adattati aiutano a rivelare quali proteine virali consentono al virus di eludere le difese immunitarie o danneggiare i tessuti. Nei primati non umani, che più rispecchiano la malattia umana, il virus Ravn può essere tanto letale quanto i ceppi Marburg più gravi in alcune specie di scimmie ma relativamente mite in altre, sottolineando forti differenze specifiche dell’ospite. È importante che trattamenti sperimentali, come un anticorpo umano isolato originariamente da un sopravvissuto al Marburg, siano stati in grado di curare scimmie infettate sia con il virus Marburg sia con il virus Ravn, mostrando che alcune terapie possono offrire protezione incrociata contro entrambi.
Vaccini che mirano a coprire entrambe le minacce
Gli sviluppatori di vaccini si sono concentrati principalmente sul virus Marburg, ma la relazione stretta—seppur non identica—con il virus Ravn solleva preoccupazioni che un vaccino solo per Marburg possa lasciare lacune nella protezione. La revisione riassume diversi approcci promettenti, inclusi vaccini basati su adenovirus innocui, particelle simili al virus e moderne formulazioni a mRNA. In porcellini d’India e scimmie, alcuni vaccini basati su Marburg hanno generato risposte immunitarie che riconoscono e proteggono anche contro il virus Ravn. Altri, però, mostrano una copertura irregolare: per esempio, un vaccino a mRNA costruito sulla proteina di superficie del virus Ravn ha fornito una forte protezione contro Ravn stesso e solo una protezione incrociata parziale contro Marburg. Questi risultati evidenziano che la direzione della protezione incrociata non è sempre simmetrica e che la piattaforma vaccinale esatta e il design della proteina virale sono determinanti.
Cosa significa per i focolai futuri
Complessivamente, l’articolo sostiene che il virus Ravn è più di una nota a margine del virus Marburg: le sue differenze genetiche, i lievi cambiamenti nel modo in cui si diffonde nei pipistrelli e il comportamento distinto negli animali sperimentali suggeriscono tutti che potrebbe rappresentare rischi unici in futuri eventi di trasbordo. Allo stesso tempo, le caratteristiche condivise tra i due virus offrono una via realistica verso vaccini e terapie ampie, alcuni dei quali hanno già curato scimmie infette in laboratorio. Per il pubblico generale, il messaggio chiave è che comprendendo ora questo cugino più silenzioso—dove si nasconde, come passa dai pipistrelli alle persone e come il nostro sistema immunitario può essere addestrato a bloccarlo—scienziati e agenzie sanitarie possono meglio anticipare e attenuare l’impatto del prossimo focolaio di malattia da virus Marburg o Ravn.
Citazione: Yordanova, I.A., Prescott, J.B. Revisiting Ravn virus as the lesser known orthomarburgvirus. npj Viruses 4, 11 (2026). https://doi.org/10.1038/s44298-026-00180-x
Parole chiave: Virus Ravn, Virus Marburg, pipistrelli frugivori, febbre emorragica, filovirus