Clear Sky Science · it
La proteina G solubile del virus respiratorio sinciziale favorisce la disseminazione virale tramite il priming NLRP3 mediato da TLR2 e la piroptosi
Perché questo virus polmonare riguarda tutti
Il virus respiratorio sinciziale, o RSV, è noto soprattutto come minaccia invernale per i neonati, ma manda anche molti anziani e persone con sistemi immunitari compromessi in ospedale. Anche con nuovi vaccini e anticorpi protettivi, l’RSV reinfetta ripetutamente le persone e può provocare danni polmonari gravi. Questo studio esamina una proteina virale poco conosciuta, una forma solubile della proteina G dell’RSV, e svela come essa possa preparare silenziosamente le cellule polmonari a un’infiammazione esplosiva e aiutare il virus a diffondersi più efficacemente nelle vie aeree.
Una proteina virale secreta che viaggia davanti all’infezione
L’RSV porta sulla sua superficie una proteina di attacco chiamata G che lo aiuta ad agganciarsi alle cellule delle vie aeree. In modo insolito, le cellule infette rilasciano anche grandi quantità di una versione libera di questa proteina, nota come G solubile. I ricercatori hanno mostrato che le cellule polmonari infettate in laboratorio possono rilasciare livelli molto elevati di G solubile nell’ambiente circostante. Poiché questa forma può diffondersi lontano dal sito d’infezione originario, può raggiungere cellule vicine non ancora infette, predisponendo a cambiamenti più estesi nell’epitelio polmonare di quanto il virus da solo provocherebbe.
G solubile come chiave a duplice azione sulle superfici cellulari
Combinando microscopia, test biochimici di pull‑down e trattamenti enzimatici, il gruppo ha mappato come la G solubile si attacca alle cellule. Hanno scoperto che può legarsi a catene zuccherine chiamate glicosaminoglicani, così come a un recettore noto dell’RSV chiamato CX3CR1. In modo cruciale, la G solubile lega anche una molecola sensrice di pattern presente su cellule immunitarie e delle vie aeree chiamata TLR2. Un piccolo motivo nella proteina G, noto come CX3C, si è rivelato importante per un legame forte con CX3CR1 e per un robusto reclutamento di TLR2. Ciò significa che la G solubile può prima essere catturata in modo non specifico sulla superficie cellulare e poi coinvolgere recettori più specifici che controllano la risposta cellulare alle minacce.
Priming delle cellule polmonari per una morte cellulare di tipo infiammatorio
Il legame della TLR2 da parte della G solubile si è rivelato tutt’altro che innocuo. in cellule immunitarie reporter e in linee cellulari polmonari umane, la G solubile ha attivato la via di segnalazione MyD88–NF-κB a valle di TLR2, portando al rilascio di messaggeri infiammatori come IL-6 e IL-8. Allo stesso tempo, ha aumentato la produzione di componenti di un “sistema d’allarme” molecolare chiamato inflammasoma NLRP3 e di enzimi che generano molecole reattive come il monossido di azoto e i radicali dell’ossigeno. Da sole, queste modifiche causarono solo danni lievi. Ma quando le cellule primed furono successivamente infettate con l’RSV, il secondo colpo innescò il pieno assemblaggio dell’inflammasoma, l’attivazione della caspasi‑1, la formazione di pori nella membrana cellulare e una forma di morte infiammatoria nota come piroptosi. Questo processo perforò le cellule, rilasciò contenuti infiammatori e coincise con quantità maggiori di virus infettivo rilasciato nel fluido di coltura.
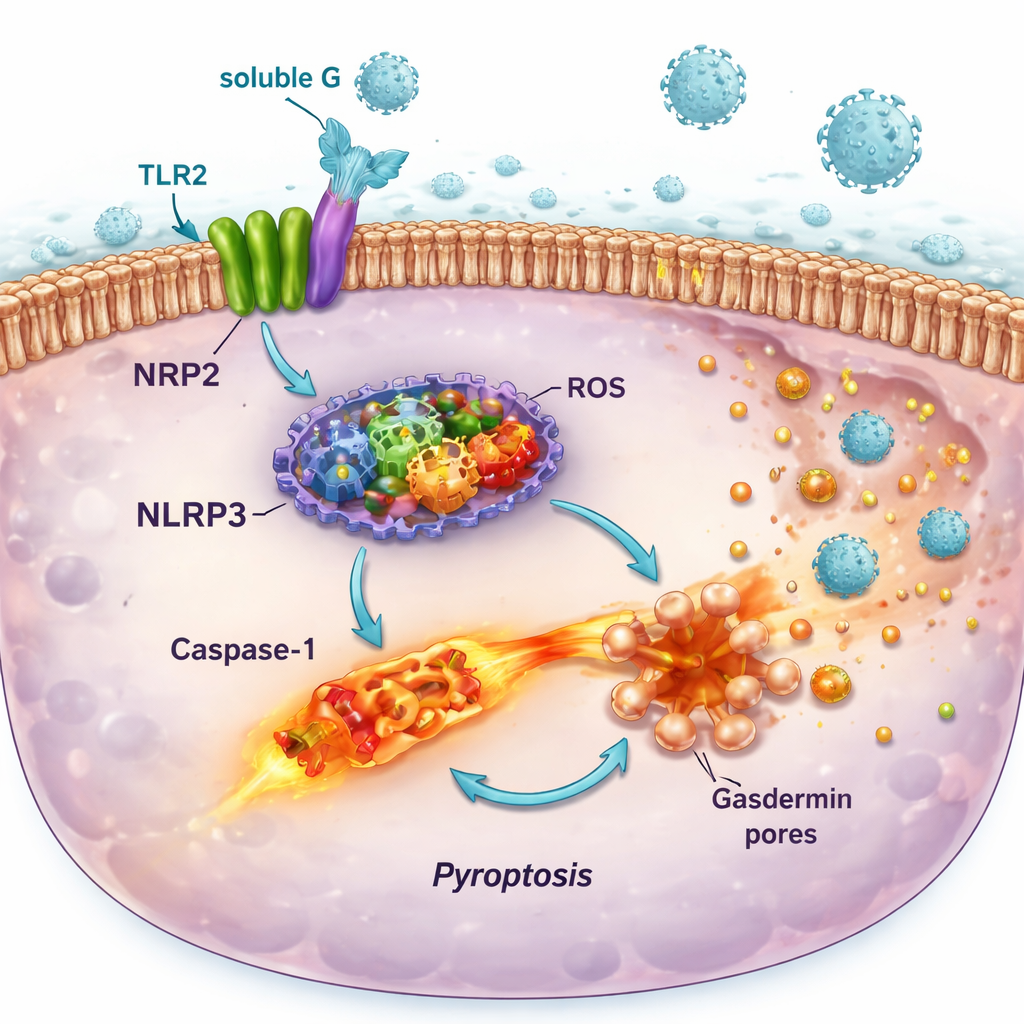
Come questa reazione a catena può peggiorare la malattia polmonare
L’effetto pro‑distruttivo della G solubile era più marcato nelle cellule epiteliali delle vie aeree—le stesse cellule che l’RSV predilige infettare—e dipendeva dall’inflammasoma NLRP3, poiché un inibitore specifico di NLRP3 preservò in larga misura la vitalità cellulare. Al contrario, alcune cellule immunitarie ricche di TLR2 ma povere del recettore CX3CR1 non subirono una morte lisi marcata nelle stesse condizioni. Questo schema suggerisce che l’RSV usa la G solubile per indebolire e distruggere selettivamente il rivestimento protettivo delle vie aeree, preservando nel contempo alcune cellule immunitarie che possono continuare a produrre segnali. Il risultato è un ambiente polmonare con più infiammazione, più detriti cellulari e più opportunità per nuove particelle virali di sfuggire e infettare cellule vicine.
Cosa significa questo per i trattamenti futuri
Per un non specialista, il messaggio chiave è che l’RSV non si affida solo al danno diretto dell’invasione virale. Rilasciando grandi quantità della proteina G solubile, può “ammorbidire” le cellule vicine attraverso TLR2, rendendole più propense a morire in modo infiammatorio e a rilasciare virus. Questo lavoro identifica diversi passaggi in questa catena—la G solubile stessa, il suo motivo CX3C, TLR2 e l’inflammasoma NLRP3—come potenziali bersagli farmacologici. In linea di principio, terapie che bloccano l’interazione tra la G solubile e TLR2, o che attenuano l’attività di NLRP3, potrebbero ridurre sia il danno polmonare sia la diffusione virale. Tali approcci potrebbero un giorno affiancare i vaccini e gli anticorpi esistenti contro l’RSV, offrendo una protezione migliore per i pazienti più giovani e più vulnerabili.
Citazione: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
Parole chiave: virus respiratorio sinciziale, proteina G solubile, inflammasoma TLR2, piroptosi, infiammazione polmonare