Clear Sky Science · it
Terapia ormonale della menopausa e rischio di malattie neuropsichiatriche: uno studio di randomizzazione mendeliana su bersagli farmacologici
Perché questa ricerca è importante
Molte donne si chiedono se assumere ormoni intorno alla menopausa protegga il cervello o aumenti il rischio di problemi come perdita di memoria, depressione o ansia. Anche i medici sono divisi, perché studi precedenti hanno dato risposte contrastanti. Questo articolo utilizza un approccio basato sulla genetica, simile nello spirito a uno studio randomizzato a lungo termine, per porre una domanda semplice: quando i recettori degli estrogeni nel cervello vengono modulati nel modo in cui potrebbe farlo la terapia ormonale della menopausa, questo modifica il rischio di malattia di Alzheimer o di disturbi mentali comuni?
Il dilemma sugli ormoni e il cervello
Le donne hanno una probabilità maggiore rispetto agli uomini di sviluppare depressione, ansia e malattia di Alzheimer. Un’ipotesi principale è che l’estrogeno, un importante ormone sessuale femminile, contribuisca a plasmare il cervello nel corso della vita e possa proteggerlo—fino a quando i suoi livelli non fluttuano o diminuiscono a metà età. Durante la transizione menopausale molte donne ricorrono alla terapia ormonale della menopausa (MHT) per alleviare sintomi come vampate di calore e disturbi del sonno. Tuttavia, gli studi sul fatto che la MHT sia utile o dannosa per la salute cerebrale non sono concordi: alcuni hanno rilevato un aumento del rischio di demenza, altri hanno suggerito un effetto protettivo, e molti non hanno mostrato effetti chiari. Queste incongruenze possono derivare dalla breve durata dei trial, da diverse formulazioni farmacologiche e dal fatto che alle donne con sintomi più gravi è più probabile vengano prescritti gli ormoni fin dall’inizio.
Usare i geni come esperimento naturale
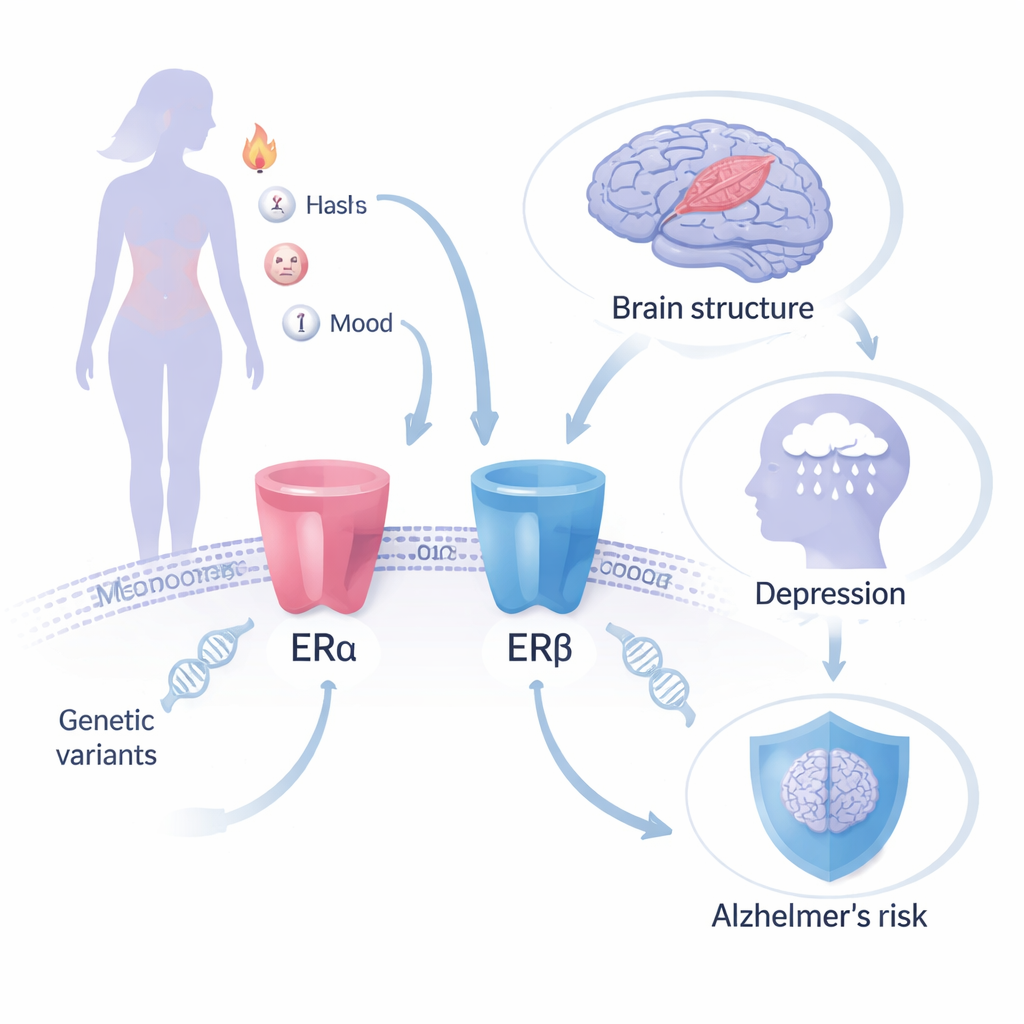
Invece di seguire donne che assumono pillole ormonali, i ricercatori hanno usato la randomizzazione mendeliana, un metodo che sfrutta differenze genetiche naturali come surrogato di un “trattamento” assegnato casualmente per tutta la vita. Si sono concentrati su due proteine dell’organismo chiamate recettori degli estrogeni—ERα ed ERβ—che la MHT mira ad attivare. Varianti genetiche specifiche nei geni che codificano questi recettori (ESR1 ed ESR2) hanno effetti noti su tratti “a valle” che cambiano quando l’estrogeno agisce, come la densità minerale ossea, una proteina plasmatica che trasporta gli ormoni sessuali e i livelli di emoglobina. Tracciando come queste varianti legate ai recettori si correlano con grandi set di dati genetici sulla malattia di Alzheimer, sulla struttura cerebrale, sulla depressione e sull’ansia, il team ha potuto stimare come la modulazione di ciascun recettore potrebbe influenzare i rischi a lungo termine per la salute cerebrale e mentale.
Cosa hanno mostrato le prove genetiche
Gli autori hanno costruito tre strumenti genetici: due che catturano l’attività di ERα (tramite varianti legate alla densità ossea e alla globulina legante gli ormoni sessuali) e uno che cattura l’attività di ERβ (tramite una variante legata all’emoglobina). Hanno quindi combinato questi strumenti con alcuni dei più ampi studi di associazione genome‑wide disponibili sulla malattia di Alzheimer, misure MRI cerebrali (massa grigia complessiva, volume dell’ippocampo e “macchie” della materia bianca associate all’invecchiamento), depressione e ansia. Complessivamente, non hanno trovato prove convincenti che cambiamenti simulati geneticamente in uno qualsiasi dei recettori degli estrogeni modifichino in modo significativo il rischio di malattia di Alzheimer o influenzino queste misure di struttura cerebrale. Alcuni segnali deboli per variazioni nella massa grigia o nel volume dell’ippocampo non hanno resistito alla correzione statistica, suggerendo che potrebbero essere dovuti al caso piuttosto che a un vero effetto biologico.
Un segnale d’allarme per il rischio di depressione
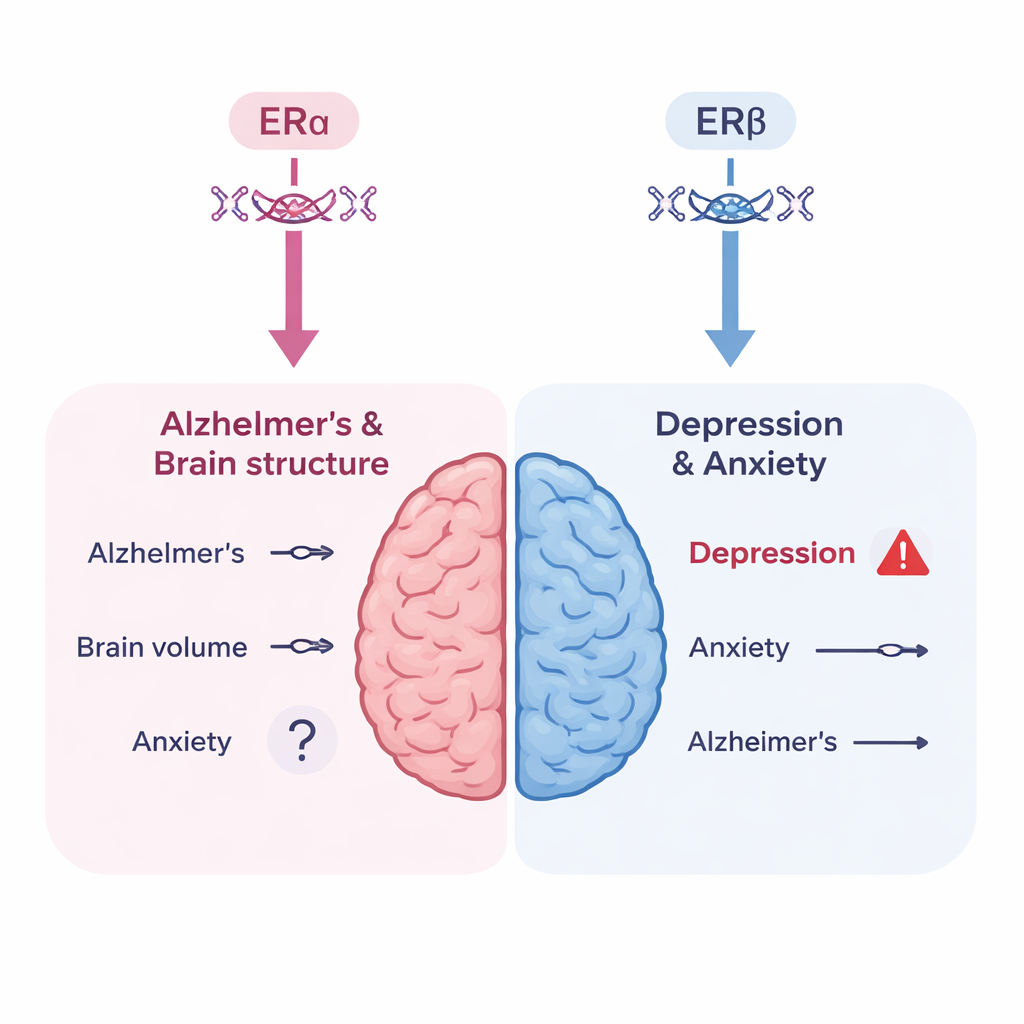
La storia è stata diversa per l’umore. Quando i ricercatori hanno esaminato l’attività di ERβ, come catturata dal surrogato genetico basato sull’emoglobina, hanno osservato un legame statisticamente solido con un rischio più elevato di depressione. Questo risultato è coerente con quanto noto sulle regioni cerebrali in cui ERβ è più attivo—aree come l’ippocampo e il talamo fortemente coinvolte nella regolazione dell’umore. Tuttavia, gli autori avvertono che il surrogato basato sull’emoglobina è imperfetto: una bassa emoglobina stessa può contribuire a stanchezza e umore basso, il che potrebbe confondere l’interpretazione. Non hanno trovato prove genetiche solide che l’attività di ERα da sola aumenti il rischio di depressione, e solo un’indicazione suggerente e non definitiva che ERα possa essere correlato all’ansia. È importante notare che gli effetti genetici che agiscono costantemente dalla nascita non sono identici all’iniziare una terapia ormonale a metà della vita, quindi questi risultati non devono essere letti come una previsione diretta di uno specifico regime di MHT.
Cosa significa per le donne e i loro medici
Tradotto in decisioni quotidiane, questo studio suggerisce che mirare ai recettori degli estrogeni in modi simili alla MHT non aumenta né riduce in modo chiaro il rischio di malattia di Alzheimer nel corso della vita né provoca grandi cambiamenti nella struttura cerebrale, almeno nelle persone di ascendenza europea. Allo stesso tempo, il risultato che indica ERβ e depressione sottolinea che i circuiti cerebrali sensibili agli ormoni sono legati all’umore, e che recettori estrogenici diversi possono avere implicazioni differenti per la salute mentale. Il lavoro non sostituisce gli studi clinici, ma offre un potente “controllo di realtà” genetico che può aiutare a perfezionare future terapie ormonali e orientare la ricerca verso trattamenti più sicuri e personalizzati per le donne che affrontano la menopausa.
Citazione: Schindler, L.S., Gill, D., Oppenheimer, H. et al. Menopausal hormone therapy and risk of neuropsychiatric disease: a drug target Mendelian randomisation study. npj Womens Health 4, 10 (2026). https://doi.org/10.1038/s44294-026-00130-1
Parole chiave: terapia ormonale della menopausa, recettori degli estrogeni, malattia di Alzheimer, rischio di depressione, randomizzazione mendeliana