Clear Sky Science · it
Valutazione STAR (stroma-tumor AI risk): associazione tra la proporzione tumore‑stroma derivata dall’IA e la sopravvivenza dei pazienti fornisce valore prognostico aggiuntivo oltre KELIM nel carcinoma ovarico epiteliale
Perché il “vicinato” intorno a un tumore conta
Quando pensiamo al cancro, di solito immaginiamo una massa di cellule fuori controllo. Ma i tumori vivono in un contesto ricco di tessuto di sostegno, vasi sanguigni e cellule immunitarie chiamato stroma. Questo studio pone una domanda semplice ma potente: possiamo usare l’equilibrio tra le cellule tumorali e il tessuto circostante, misurato tramite intelligenza artificiale (IA) su vetrini microscopici di routine, per prevedere quali pazienti con carcinoma ovarico avranno esiti migliori o peggiori — prima ancora che inizi il trattamento?
Un nuovo modo di leggere i vetrini bioptici standard
Le pazienti con carcinoma ovarico epiteliale di solito vengono sottoposte a rimozione di tessuto durante l’intervento chirurgico o la biopsia. Quei campioni vengono colorati ed esaminati al microscopio in ogni ospedale. I ricercatori si sono concentrati su una caratteristica chiamata proporzione tumore–stroma (TSP): quanto dell’immagine è costituito da tessuto di sostegno rispetto alle cellule tumorali. In lavori precedenti, i patologi stimavano questa proporzione a occhio e osservavano che i tumori ricchi di stroma spesso si comportavano in modo più aggressivo e resistevano alla chemioterapia a base di platino. Nel presente studio, il gruppo ha utilizzato un sistema di deep learning per misurare automaticamente la TSP su vetrini digitalizzati, con l’obiettivo di trasformare un compito manuale e in parte soggettivo in una lettura rapida e riproducibile disponibile già alla diagnosi.
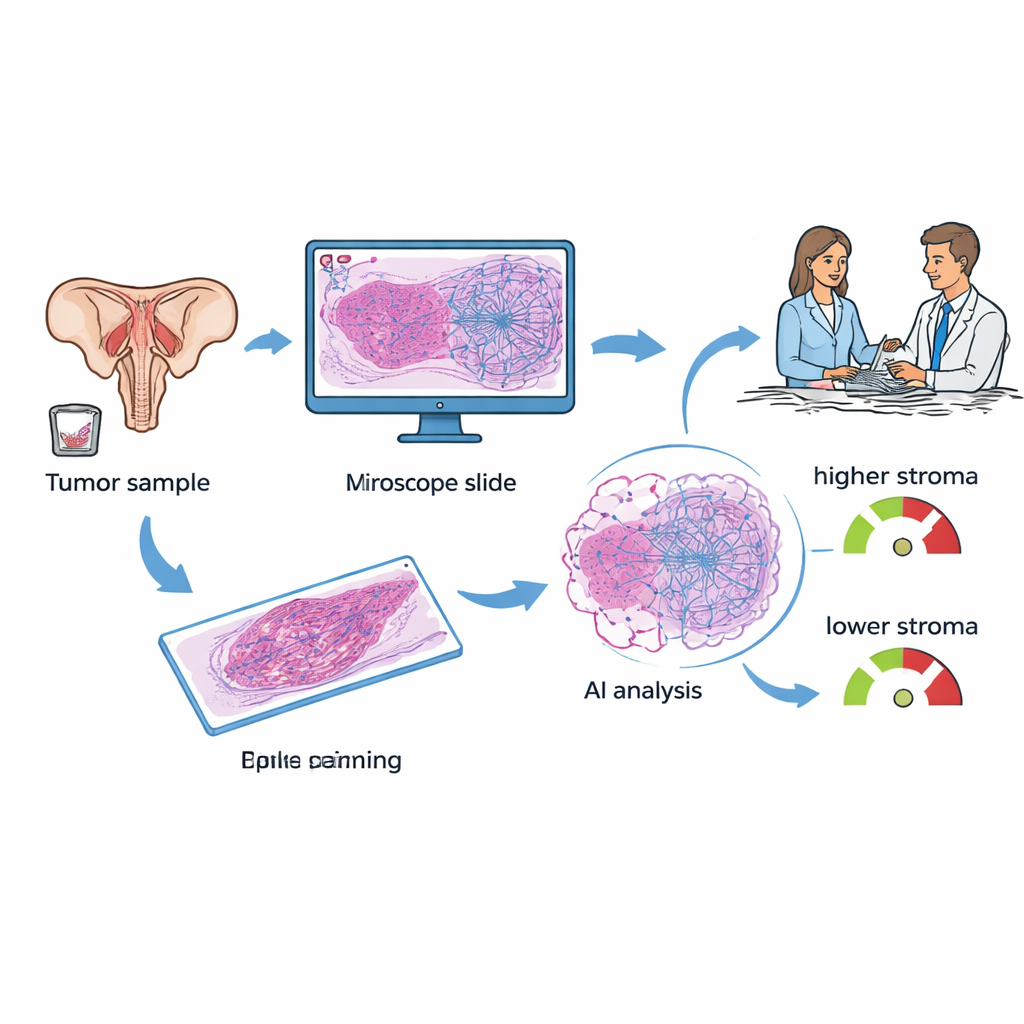
Confrontare l’analisi tissutale da IA con un indice basato sul sangue
Oggi, uno strumento ampiamente discusso per il carcinoma ovarico è KELIM, un punteggio basato sulla velocità con cui un marcatore ematico chiamato CA‑125 diminuisce nei primi 100 giorni di chemioterapia. KELIM è economico e utile, ma può essere calcolato solo dopo alcune settimane di trattamento e non tutte le pazienti hanno abbastanza esami ematici precoci per generare il punteggio. Gli investigatori hanno raccolto dati da 89 donne trattate in un unico centro oncologico che avevano sia vetrini tissutali sia almeno tre misurazioni di CA‑125. Hanno calcolato il KELIM per ogni paziente, fatto etichettare le regioni tumorali sui vetrini da un patologo e poi hanno lasciato che il modello IA stimasse la TSP, classificando ogni caso come “stroma‑basso” (meno del 50% di stroma) o “stroma‑alto” (50% o più).
L’IA corrisponde agli esperti e individua tumori a rischio più elevato
Il giudizio dell’IA ha corrisposto strettamente a quello di patologi esperti: nel 94% dei casi, la classificazione automatica della TSP concordava con quella manuale, un livello di concordanza considerato eccellente. Quando il gruppo ha analizzato gli esiti dei pazienti, ha trovato che le donne i cui tumori risultavano stroma‑alti secondo l’IA avevano una sopravvivenza globale significativamente peggiore rispetto a quelle con tumori stroma‑bassi. In termini statistici, un’elevata TSP ha quasi raddoppiato il rischio di morte durante il follow‑up, e questo effetto è persistito anche tenendo conto del punteggio KELIM. Per contro, in questo gruppo di pazienti real‑world, il KELIM era collegato alla probabilità che i tumori fossero resistenti ai farmaci a base di platino ma non risultava chiaramente correlato alla durata della sopravvivenza.
Cosa potrebbe significare per le decisioni terapeutiche
Poiché la TSP può essere misurata su vetrini di routine prelevati al momento della diagnosi, la TSP basata su IA offre un modo per valutare il rischio prima che inizi la chemioterapia, potenzialmente mesi prima rispetto al KELIM. Un risultato di TSP elevata potrebbe avvisare i clinici che un tumore è più probabile che sia aggressivo e più difficile da trattare, inducendo a un monitoraggio più stretto, a una considerazione anticipata di terapie aggiuntive o a strategie chirurgiche diverse. Il metodo è anche relativamente a basso costo: si basa su immagini di patologia esistenti e su un modello software invece che su nuovi test di laboratorio. Gli autori sostengono che la TSP automatizzata potrebbe affiancare altri marcatori, come test genetici e l’andamento del CA‑125, per raffinare la prognosi senza aggiungere un onere rilevante alle pazienti o ai team di patologia.
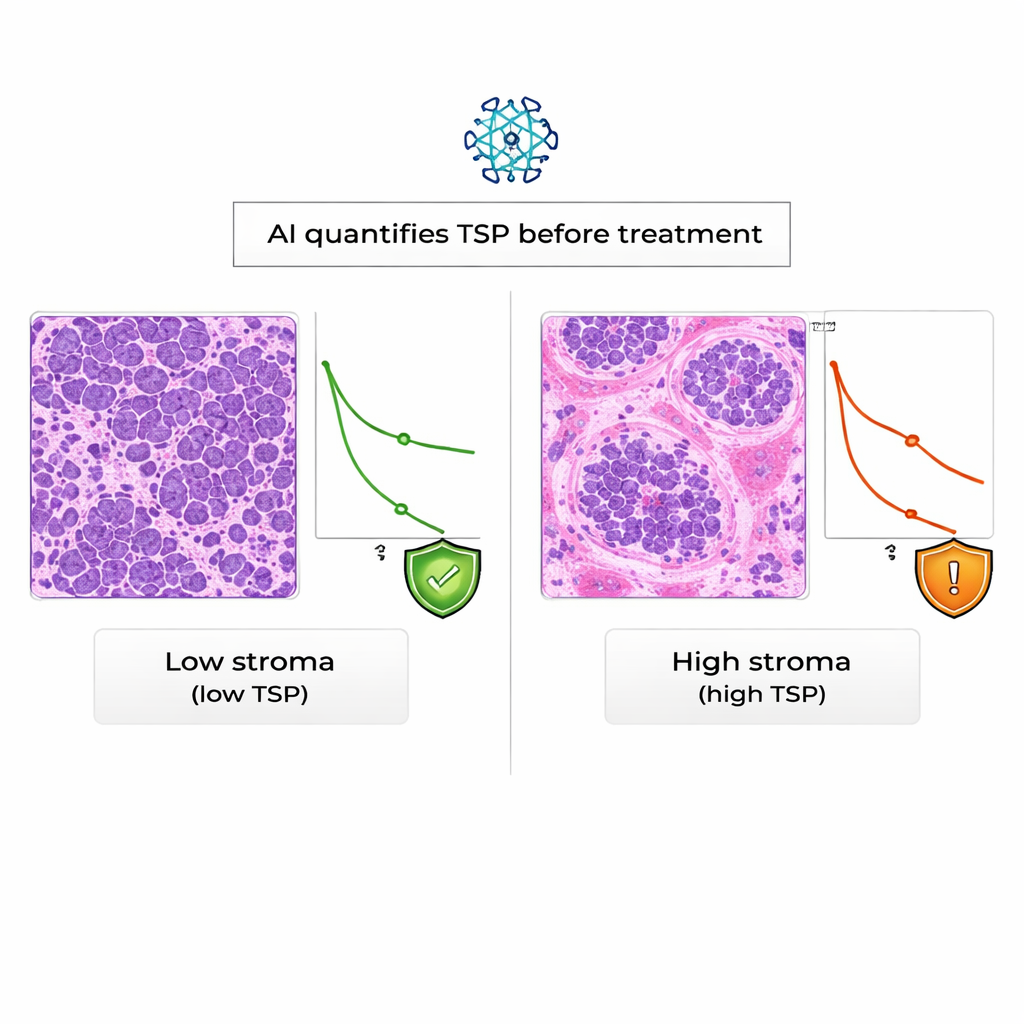
Prospettive future: orientamenti più intelligenti e precoci per le pazienti
Per il pubblico non specialistico, il messaggio principale è che non tutti i carcinomi ovarici sono uguali, e il tessuto di supporto intorno al tumore porta indizi importanti sul comportamento della malattia. Questo studio mostra che l’IA può leggere tali indizi in modo affidabile su vetrini bioptici standard e che un tumore ricco di stroma tende ad associarsi a una sopravvivenza peggiore, indipendentemente dai punteggi ematici esistenti. Sebbene siano necessari studi più ampi e diversificati prima che questo approccio entri nella pratica routinaria, la TSP derivata dall’IA promette di essere un segnale di allarme precoce che potrebbe aiutare i medici a personalizzare i piani terapeutici e a fornire alle pazienti aspettative più chiare fin dall’inizio.
Citazione: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
Parole chiave: carcinoma ovarico, intelligenza artificiale, microambiente tumorale, biomarcatore prognostico, patologia digitale