Clear Sky Science · it
Studio genomico rivela l’emergere di una lineage dominante multiresistente nelle popolazioni di Proteus mirabilis
Perché questo germe ospedaliero è importante per te
Per molte persone, le infezioni del tratto urinario sono un fastidio occasionale e doloroso. Ma in ospedali e strutture per anziani, alcune infezioni sono causate da batteri resistenti che si attaccano ai cateteri, resistono a molteplici antibiotici e si diffondono silenziosamente tra persone e animali. Questo studio segue uno di questi colpevoli, Proteus mirabilis, in tutto il mondo, usando il suo DNA come diario di viaggio per rivelare come una singola famiglia difficile da trattare sia salita silenziosamente a dominare nel corso dell’ultimo secolo.
Uno sguardo globale a una minaccia nascosta
I ricercatori hanno assemblato genomi di 1.142 campioni di Proteus mirabilis raccolti in 34 paesi da esseri umani, bestiame, carne al dettaglio e altri ambienti. Confrontando i genomi completi, hanno suddiviso i batteri in 178 famiglie genetiche. Una ha risaltato: la “Cluster-1”, una lineage principale che rappresentava un campione su cinque e includeva ceppi provenienti da ospedali in più continenti. La maggior parte di questi ceppi proveniva da persone, ma una parte significativa è stata isolata anche da animali da allevamento e carne, indicando che questa lineage si muove tra specie e lungo la filiera alimentare.
Una lineage armata di molti scudi contro i farmaci
Quando il team ha esaminato i genomi alla ricerca di geni di resistenza agli antibiotici, Cluster-1 presentava un carico nettamente maggiore. In media, i suoi membri ospitavano quasi 18 geni di resistenza ciascuno, molto più delle altre lineages. Tra questi c’erano geni che neutralizzano alcuni dei nostri antibiotici più potenti, come i carbapenemi, spesso riservati come terapie di ultima istanza. Molti di questi geni di resistenza si trovano all’interno di una grande “isola” di DNA chiamata PmGRI1, che può saltare tra batteri. Alcune versioni di questa isola contengono più di 20 geni di resistenza contemporaneamente, trasformando di fatto Proteus in una farmacia ambulante di difese e lasciando ai medici poche opzioni terapeutiche.
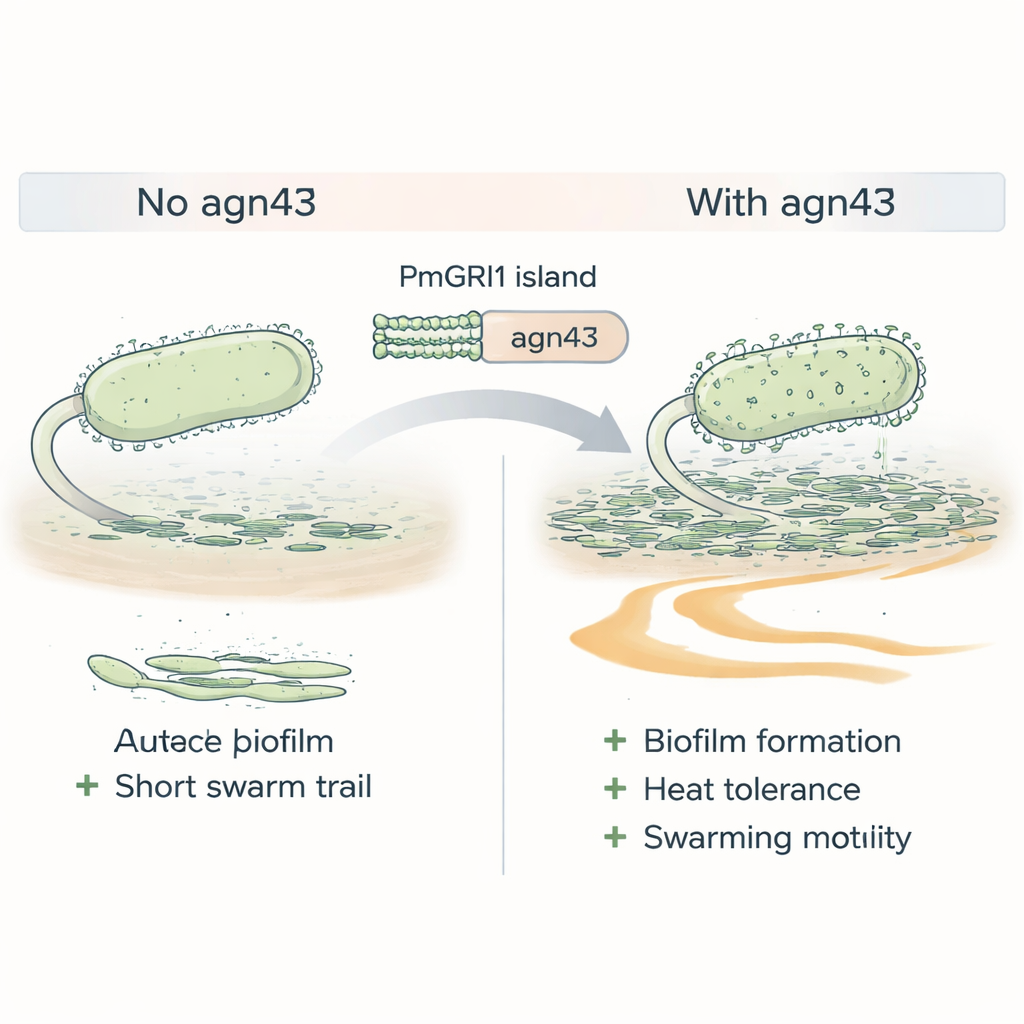
Caratteristiche appiccicose che aiutano il batterio a persistere
La resistenza da sola non garantisce il successo; i batteri devono anche essere bravi a sopravvivere nell’organismo e nell’ambiente ospedaliero. I ceppi di Cluster-1 erano arricchiti di geni associati all’adesione alle cellule e alla formazione di biofilm—comunità viscose che proteggono i batteri da farmaci e dal sistema immunitario. Un gene di rilievo sull’isola PmGRI1, chiamato agn43, codifica una proteina di superficie che funziona come un velcro molecolare, favorendo l’aggregazione cellulare. Quando gli scienziati hanno eliminato agn43 in un ceppo di Cluster-1, il mutante ha formato biofilm più deboli, ha tollerato meno bene lo stress termico e si è spostato meno efficacemente sulle superfici, tutte caratteristiche che normalmente aiutano Proteus a colonizzare i cateteri urinari e a diffondersi nel tratto urinario.
Come e dove si è diffusa questa super-lineage
Combinando le differenze genetiche con le date di isolamento, i ricercatori hanno ricostruito una linea temporale per Cluster-1. Hanno stimato che il suo antenato comune più recente sia apparso intorno al 1910, decenni prima che gli antibiotici moderni fossero ampiamente utilizzati. La lineage si è poi divisa in due rami di rilevanza medica: uno principalmente osservato in Cina che porta un gene che rompe i carbapenemi chiamato blaKPC-2, e un altro soprattutto negli Stati Uniti che porta un gene correlato, blaIMP-27. Dalla fine degli anni ’80 in poi, Cluster-1 si è espansa rapidamente ed è stata ripetutamente rilevata mentre si muoveva tra paesi e tra esseri umani, bestiame e carne, sottolineando il suo potenziale epidemico.
Cosa significa per i pazienti e la salute pubblica
Per un pubblico non specialistico, il messaggio è che una particolare famiglia di Proteus mirabilis si è evoluta in un germe ospedaliero altamente efficace combinando due vantaggi: un’armatura spessa di geni di resistenza agli antibiotici e una maggiore “appiccicosità” che la aiuta a formare film protettivi e persistere su cateteri e tessuti. Questa combinazione rende le infezioni più difficili da trattare e più facili da diffondere. Il lavoro mette in evidenza la necessità di una sorveglianza genetica ravvicinata di questa lineage sia negli ospedali sia in agricoltura, di controlli di infezione più rigorosi intorno ai cateteri e di un uso prudente degli antibiotici per rallentare l’ascesa e la circolazione globale di ceppi multiresistenti.
Citazione: Zhang, T., Wei, H., Ju, Z. et al. Genomic survey uncovers the emergence of a multidrug-resistant dominant lineage in Proteus mirabilis populations. npj Antimicrob Resist 4, 17 (2026). https://doi.org/10.1038/s44259-026-00189-5
Parole chiave: resistenza agli antibiotici, infezione del tratto urinario, infezioni ospedaliere, genomica batterica, biofilm