Clear Sky Science · it
Risposta globale all’esposizione agli antibiotici rivela un ruolo critico del metabolismo dei nucleotidi nella tolleranza ad alto livello ai β-lattamici
Perché alcuni batteri resistono ai nostri migliori antibiotici
Gli antibiotici dovrebbero eliminare i batteri nocivi, eppure molte infezioni persistono ostinatamente o ricompaiono dopo il trattamento. Questo articolo esplora una ragione poco considerata: alcuni batteri riescono ad adottare uno stato di sopravvivenza temporanea anche di fronte a dosi molto elevate di farmaci potenti come la penicillina. Scoprendo come questi microrganismi rimodellano la loro chimica interna per resistere all’attacco, i ricercatori individuano nuove strade per ripristinare l’efficacia degli antibiotici esistenti.
Una tattica di sopravvivenza silenziosa nelle infezioni
Esposti a antibiotici beta-lattamici come la penicillina, molti batteri Gram-negativi pericolosi non muoiono semplicemente. Possono invece perdere la loro parete cellulare rigida e trasformarsi in corpi fragili e sferici chiamati sferoplasti. In questa forma smettono di moltiplicarsi ma restano vivi e metabolicamente attivi. Una volta che il farmaco viene rimosso, ricostruiscono la parete, riprendono la normale forma a bastoncello e possono riattivare l’infezione. Poiché questa “tolleranza” è un passaggio verso la piena resistenza agli antibiotici e il fallimento del trattamento, comprendere come gli sferoplasti sopravvivono è cruciale per la medicina futura.
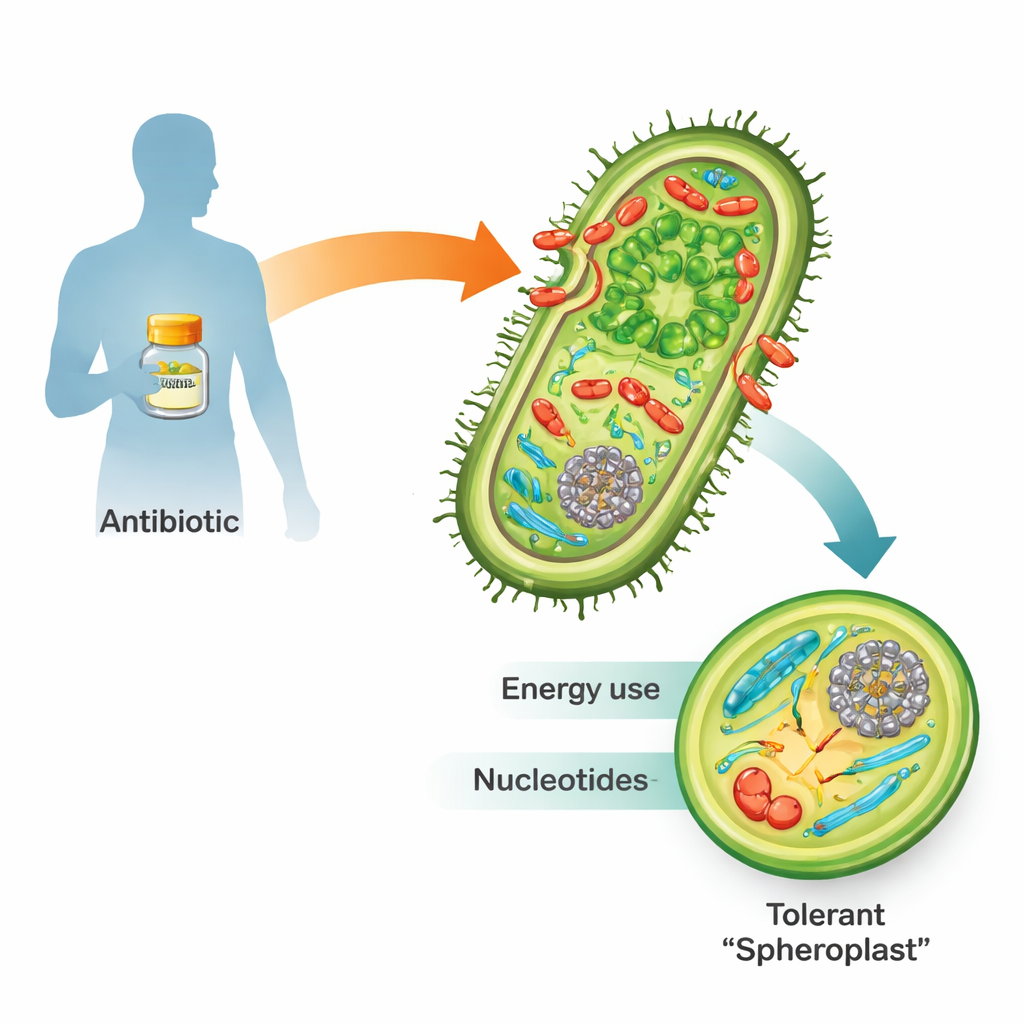
Ascoltare il segnale di emergenza della cellula
Il gruppo ha usato Vibrio cholerae, il batterio che causa il colera, come modello perché è particolarmente tollerante ai beta-lattamici e facile da manipolare geneticamente. Ha immerso i batteri in una concentrazione di penicillina dieci volte superiore alla dose letale minima e ha seguito la risposta nel tempo con due strumenti potenti. La transcriptomica ha tracciato quali geni venivano attivati o disattivati, mentre la metabolomica ha misurato centinaia di piccole molecole che alimentano e costruiscono la cellula. Insieme, queste tecniche “multi-omiche” hanno creato una mappa temporale di come una cellula tollerante riorganizza il proprio funzionamento interno durante l’assalto farmacologico.
Riorientamento metabolico e una vulnerabilità nascosta
I dati hanno rivelato cambiamenti estesi nelle vie metaboliche di base. I geni per la sintesi della parete cellulare si sono fortemente attivati, coerentemente con il tentativo della cellula di riparare i danni e prepararsi al recupero. Anche i sistemi di risposta al calore e allo stress si sono intensificati, probabilmente per gestire proteine mal ripiegate o ossidate generate dallo stress indotto dall’antibiotico. Allo stesso tempo, il metabolismo del carbonio centrale si è spostato: alcune tappe del ciclo di Krebs (il principale generatore di energia della cellula) sono state potenziate, mentre intermedi chiave della glicolisi come glucosio-6-fosfato e fruttosio-6-fosfato sono risultati drasticamente impoveriti. Questi intermedi normalmente alimentano sia la produzione di energia sia la sintesi della parete cellulare, suggerendo che un continuo e sprecone “ciclo futile” di materiali per la parete stava prosciugando le risorse.
Nucleotidi sotto pressione
Il cambiamento più marcato ha riguardato i nucleotidi, i mattoni del DNA, dell’RNA e di molte molecole trasportatrici di energia. I livelli di molti nucleotidi e dei loro precursori sono crollati nelle cellule trattate con penicillina, nonostante i geni per la loro sintesi de novo fossero fortemente attivati. Contemporaneamente, sono stati repressi i geni coinvolti nel “riciclo” dei nucleotidi, come se la cellula cercasse di conservare quel poco che rimaneva. Questi schemi suggerivano che gli sferoplasti sono sottoposti a un grave stress dei nucleotidi. Quando i ricercatori hanno deliberatamente interferito con le vie che forniscono precursori dei nucleotidi — come la via del pentoso fosfato — oppure hanno bloccato la produzione di nucleotidi con un altro farmaco, il trimetoprim, la combinazione con i beta-lattamici ha ucciso molto più efficacemente i batteri rispetto a ciascun farmaco da solo. Questa forte sinergia è stata osservata non solo in Vibrio cholerae ma anche in ceppi clinici altamente tolleranti di Klebsiella pneumoniae ed Escherichia coli.
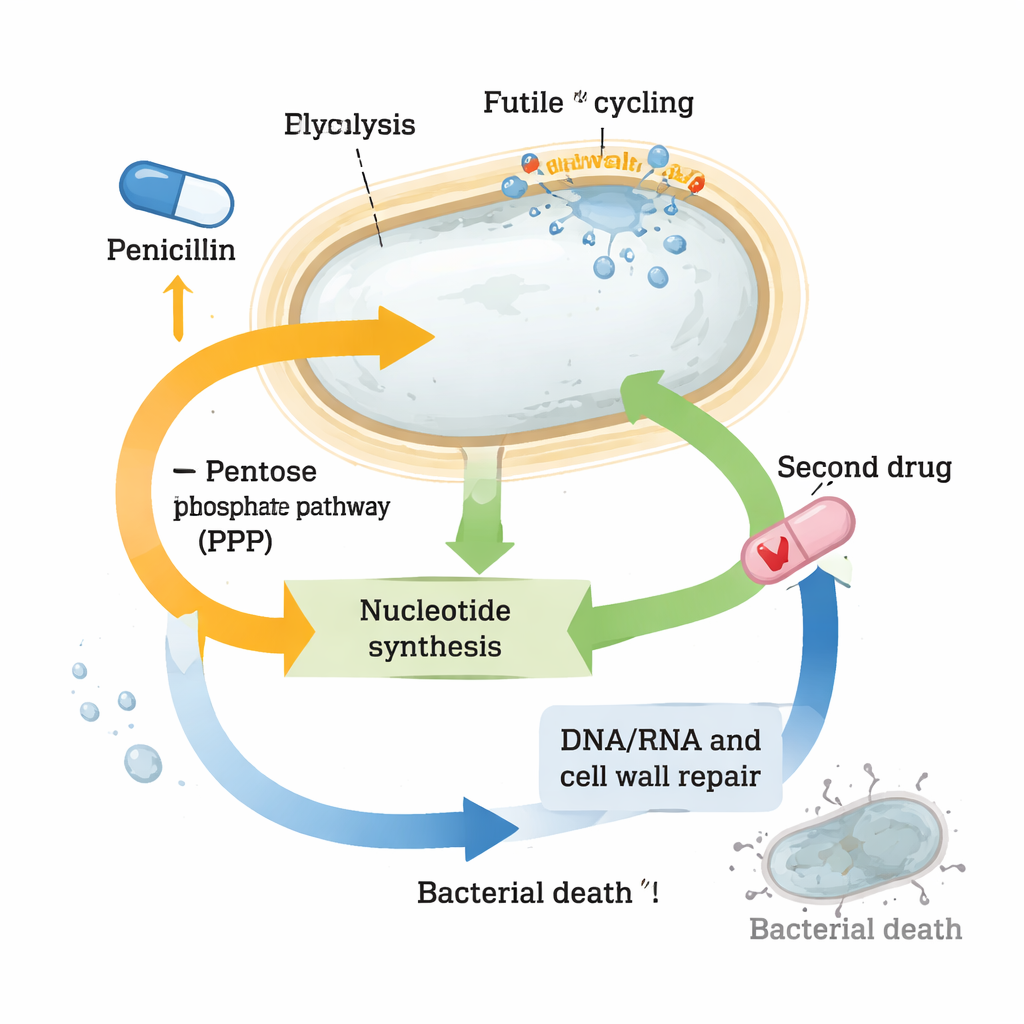
Trasformare la chimica della sopravvivenza in un vantaggio terapeutico
Nonostante una profonda rimodellazione del loro metabolismo, gli sferoplasti tolleranti riescono a mantenere relativamente stabile la loro moneta energetica, l’ATP, ed evitare danni catastrofici, il che li aiuta a sopravvivere a esposizioni prolungate agli antibiotici. Ma lo studio mostra che, nel farlo, portano i loro pool di nucleotidi sull’orlo del collasso. Quell’equilibrio precario crea una vulnerabilità: alterare leggermente il metabolismo dei nucleotidi con un secondo farmaco fa crollare le loro difese e ripristina un’uccisione potente. Per il lettore generale, la conclusione è che alcuni batteri sopravvivono agli antibiotici non perché i farmaci non colpiscano i loro bersagli, ma perché le cellule rimodellano rapidamente la loro chimica per resistere al colpo. Trovando ed esplicitando i punti deboli di questa rete di sopravvivenza — qui, il metabolismo dei nucleotidi — i ricercatori potrebbero trasformare vecchi antibiotici in terapie combinatorie potenti che sovvertono anche i patogeni altamente tolleranti.
Citazione: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
Parole chiave: tolleranza agli antibiotici, antibiotici beta-lattamici, metabolismo dei nucleotidi, persistenza batterica, combinazioni farmacologiche