Clear Sky Science · it
Attenuazione dell’attivazione epicardica e dell’abbondanza di miofibroblasti tramite l’asse Fbln2–Nupr1b stimola la rigenerazione cardiaca nel pesce zebra
Perché alcuni cuori possono guarire da soli
Quando una persona subisce un infarto, il muscolo danneggiato viene di solito coperto da una cicatrice rigida che non si rigenera mai completamente. I pesci zebra, piccoli pesci da acquario a strisce, fanno invece qualcosa di straordinario: ricrescono il tessuto cardiaco e alla fine smantellano buona parte della cicatrice. Questo studio pone una domanda apparentemente semplice, ma con grandi implicazioni mediche: come fa un cuore in riparazione a sapere quando costruire tessuto cicatriziale e quando rimuoverlo per permettere la crescita di nuovo muscolo? Decodificando questo equilibrio nei pesci zebra, il lavoro indica strategie che un giorno potrebbero aiutare i cuori umani lesionati a ripararsi invece che a deteriorarsi.
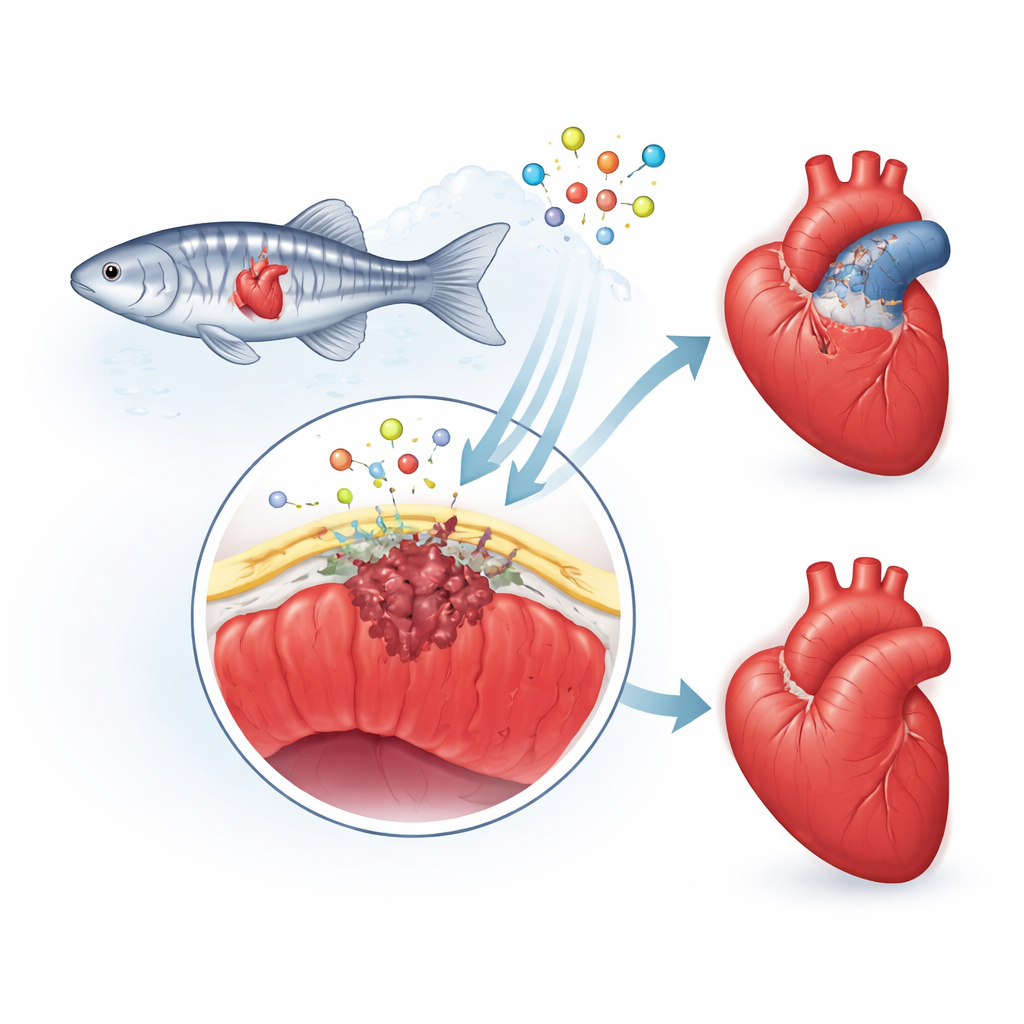
La pelle protettiva del cuore
I ricercatori si concentrano sull’epicardio, un sottile «rivestimento» che copre il cuore. Dopo un danno, questo strato si risveglia: le sue cellule cambiano identità e alcune migrano nella zona lesa. Lì diventano cellule di supporto e cellule che formano la cicatrice, e rilasciano segnali chimici che guidano la crescita di nuovi vasi sanguigni e tessuto cardiaco. Nell’uomo questa risposta riparativa tende a esagerare, lasciando una cicatrice spessa e permanente. Nei pesci zebra, però, la cicatrice è temporanea e viene progressivamente smantellata mentre il muscolo sano ritorna. Il gruppo ha ipotizzato che una proteina chiamata fibulina-2 (Fbln2), presente nell’impalcatura che circonda il cuore, contribuisca a regolare il ritmo e l’intensità di questa risposta epicardica.
Un dimmer molecolare sulla cicatrizzazione
Utilizzando l’editing genico nei pesci zebra, gli scienziati hanno generato due tipi di animali con livelli diversi di Fbln2: una linea con Fbln2 ridotta e un’altra con la proteina completamente assente. Hanno lesionato i cuori dei pesci con una sonda congelante, imitando un infarto, e seguito la guarigione per settimane e mesi. Quando i livelli di Fbln2 erano ridotti, la divisione cellulare precoce nel muscolo cardiaco e nell’endotelio dei vasi diminuiva, ma la cicatrice fibrosa che si formava era più piccola e più facilmente rimodellabile. Dopo tre mesi, questi cuori si erano rigenerati bene e avevano poco collagene, il principale componente della cicatrice. Al contrario, i pesci privi completamente di Fbln2 mostravano un più marcato spegnimento di una via chiave di crescita e cicatrizzazione, coinvolgente una famiglia di segnali nota come TGFβ, e avevano molto meno cellule formatrici di cicatrice immediatamente sotto l’epicardio. Anche le loro cicatrici iniziali erano più piccole, ma successivamente questi cuori non riuscivano a eliminare il collagene e finivano con grandi cicatrici permanenti e scarsa rigenerazione.
Ingrandire i cambiamenti dello stato epicardico
Per osservare il comportamento delle cellule epicardiche a risoluzione unicellulare, il team ha utilizzato il single-cell RNA sequencing poco dopo la lesione. Hanno identificato diversi «stati» delle cellule epicardiche, inclusi stati quiescenti, cellule recentemente attivate, cellule sotto stress per basso ossigeno e cellule in divisione attiva. Nei pesci con livelli normali di Fbln2, le cellule epicardiche progredivano fluidamente dallo stato quiescente a quello attivato e poi a stati più maturi. Nei pesci con Fbln2 ridotta o assente, questa progressione si bloccava: le cellule restavano nelle fasi iniziali e i gruppi di cellule attivate più mature erano sottorappresentati, in particolare negli animali con perdita completa. Molti geni che normalmente si attivano durante l’attivazione epicardica e in risposta alla segnalazione TGFβ risultavano downregolati, indicando Fbln2 come un regolatore di questa via che decide quanto intensamente l’epicardio si impegna nella formazione e nel rimodellamento della cicatrice.
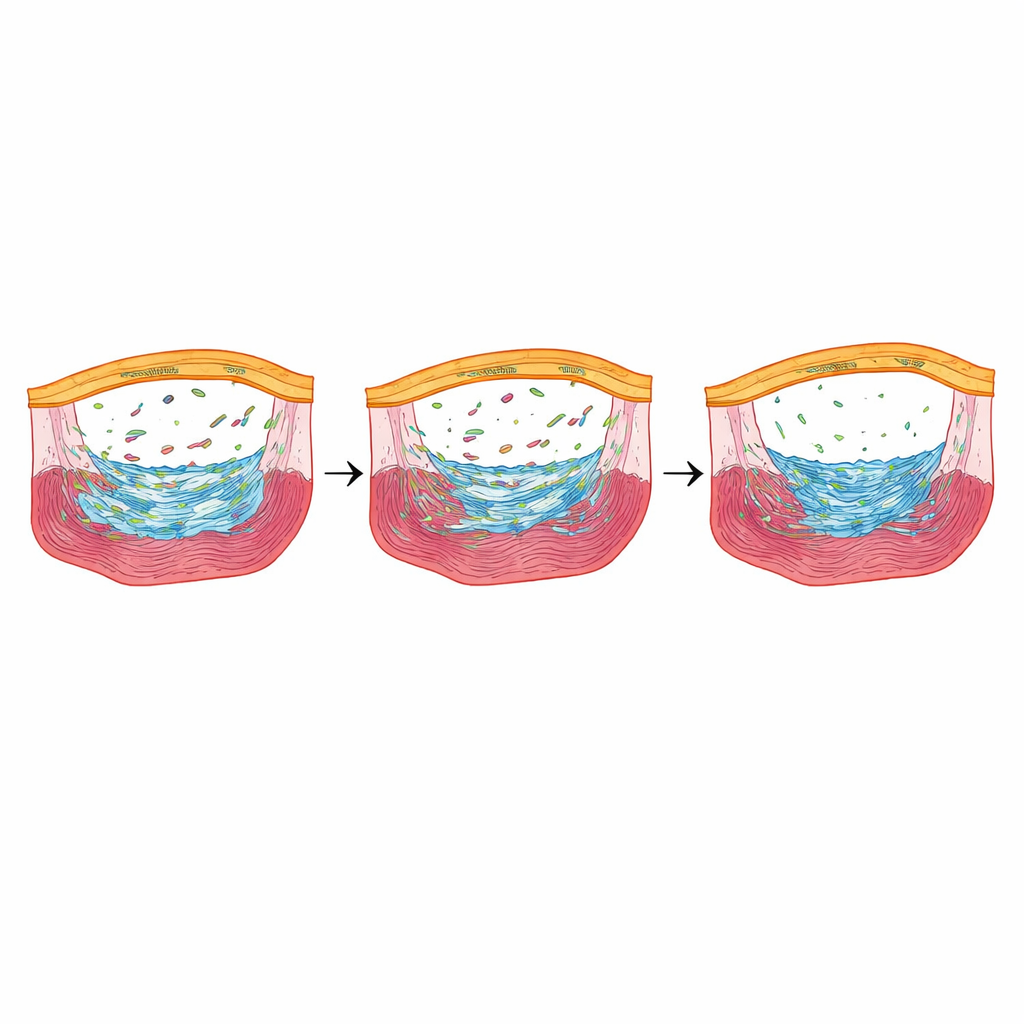
Un risponditore allo stress che affina la riparazione
Tra i geni maggiormente ridotti quando Fbln2 era basso, uno ha attirato l’attenzione: nupr1b, un regolatore sensibile allo stress attivo nelle cellule epicardiche nelle fasi precoci della guarigione. Quando i ricercatori hanno eliminato nupr1b, i pesci zebra mostravano meno cellule epicardiche formatrici di cicatrice e una ridotta proliferazione dei miociti, e mantenevano grandi depositi di collagene mesi dopo la lesione—molto simili ai pesci completamente privi di Fbln2. Colpisce che, quando hanno riattivato temporaneamente nupr1b soltanto nelle cellule epicardiche dei pesci con Fbln2 ridotta, il numero di cellule formatrici di cicatrice e la proliferazione dei miociti sono tornati rispetto ai livelli precedenti, e la cicatrizzazione tardiva è aumentata. Il blocco chimico dei recettori TGFβ riduceva i livelli di nupr1b, collocando nupr1b a valle di un asse di segnalazione Fbln2–TGFβ.
Cosa significa per la guarigione del cuore umano
Nel complesso, questi risultati rivelano un «asse epicardico Fbln2–Nupr1b» che aiuta i cuori dei pesci zebra a camminare su una sottile linea tra troppa e troppo poca fibrosi. Ridurre leggermente questo asse attenua il picco iniziale di cicatrizzazione e favorisce la rimozione efficiente della cicatrice, mentre spegnerlo completamente compromette la rigenerazione e lascia dietro di sé una cicatrice rigida. Per la medicina umana, la lezione è che l’obiettivo non è bloccare del tutto la cicatrizzazione, ma modulare il processo—mantenendo sufficiente struttura per prevenire la rottura ma assicurando che il tessuto cicatriziale sia temporaneo e possa essere sostituito dal muscolo sano. Comprendere e, in futuro, sfruttare questo sistema di controllo nel pesce zebra potrebbe guidare terapie che inducano il cuore umano lesionato verso una vera rigenerazione invece che verso una cicatrizzazione cronica.
Citazione: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
Parole chiave: rigenerazione cardiaca, fibrosi, pesce zebra, epicardio, segnalazione TGF-beta