Clear Sky Science · it
Valutazione integrativa genomica e bibliografica della cardiomiopatia aritmogena correlata a desmogleina 2 con validazione su coorte italiana
Perché questo gene cardiaco è importante per le famiglie
Molti problemi cardiaci improvvisi in persone giovani e per il resto sane non sono casuali: sono scritti, almeno in parte, nel loro DNA. Questo articolo esplora una proteina chiave che fa da “collante” nel cuore chiamata desmogleina‑2 e mostra come piccole variazioni nel suo gene possano indebolire il muscolo cardiaco, alterare il ritmo elettrico e aumentare il rischio di eventi pericolosi. Combinando grandi banche dati genetiche con un gruppo di pazienti italiani seguito con cura, i ricercatori offrono risposte più chiare per le famiglie che si chiedono cosa significhi davvero un risultato positivo a questo test genetico.
Il collante meccanico del cuore
Le cellule del muscolo cardiaco devono rimanere saldamente aderenti tra loro mentre battono milioni di volte nella vita. La desmogleina‑2 è parte di una struttura microscopica a incastro che blocca le cellule vicine insieme in modo che possano tirare come una squadra. Gli autori spiegano come questa proteina attraversi l’esterno della cellula, dove afferra un partner corrispondente sulla cellula successiva, fino all’interno, dove si aggancia a un’impalcatura di sostegno. Poiché la desmogleina‑2 è l’unico membro della sua famiglia presente nelle cellule cardiache, qualsiasi danno serio non può essere compensato da un sostituto, rendendo il cuore particolarmente vulnerabile.
Distinguere le varianti significative dal rumore di fondo
Il sequenziamento moderno individua migliaia di differenze nel gene della desmogleina‑2 nella popolazione, ma la maggior parte non causa malattia. Il gruppo ha rivisto sistematicamente 115 studi pubblicati e si è basato su due grandi banche dati pubbliche che insieme elencavano più di 5.000 varianti. Utilizzando regole ampiamente accettate della genetica medica, hanno riclassificato ogni variante in base alla probabilità che sia dannosa. Hanno scoperto che le varianti realmente dannose si concentrano in regioni specifiche della proteina—in particolare i segmenti esterni che necessitano di calcio per formare un ponte rigido tra le cellule, un breve tratto che deve essere tagliato affinché la proteina matura, e la regione interna che si aggancia a un’altra proteina cardiaca chiave. Molte altre varianti sono rimaste “incerte”, ma un sottoinsieme ha mostrato forti indizi di rilevanza ed è stato segnalato per approfondimenti.
Cosa rivela il gruppo di pazienti italiano
Per vedere come questi schemi genetici si traducono nelle persone reali, i ricercatori hanno studiato 95 individui in Italia portatori di varianti di desmogleina‑2, valutati in modo approfondito con ecografie, esami del ritmo cardiaco e follow‑up a lungo termine. Circa la metà rispettava criteri stringenti per la cardiomiopatia aritmogena, una condizione in cui parti del muscolo cardiaco vengono progressivamente sostituite da tessuto cicatriziale e adiposo, predisponendo a pericolose alterazioni del ritmo. Tra i parenti portatori di una variante, solo circa quattro su dieci mostravano effettivamente segni di malattia, sottolineando che un test genetico positivo non garantisce la malattia ma indica la necessità di un monitoraggio attento. Chi presentava una malattia evidente aveva un carico significativo di eventi aritmici gravi, mentre trapianti e decessi erano meno frequenti ma comunque presenti.
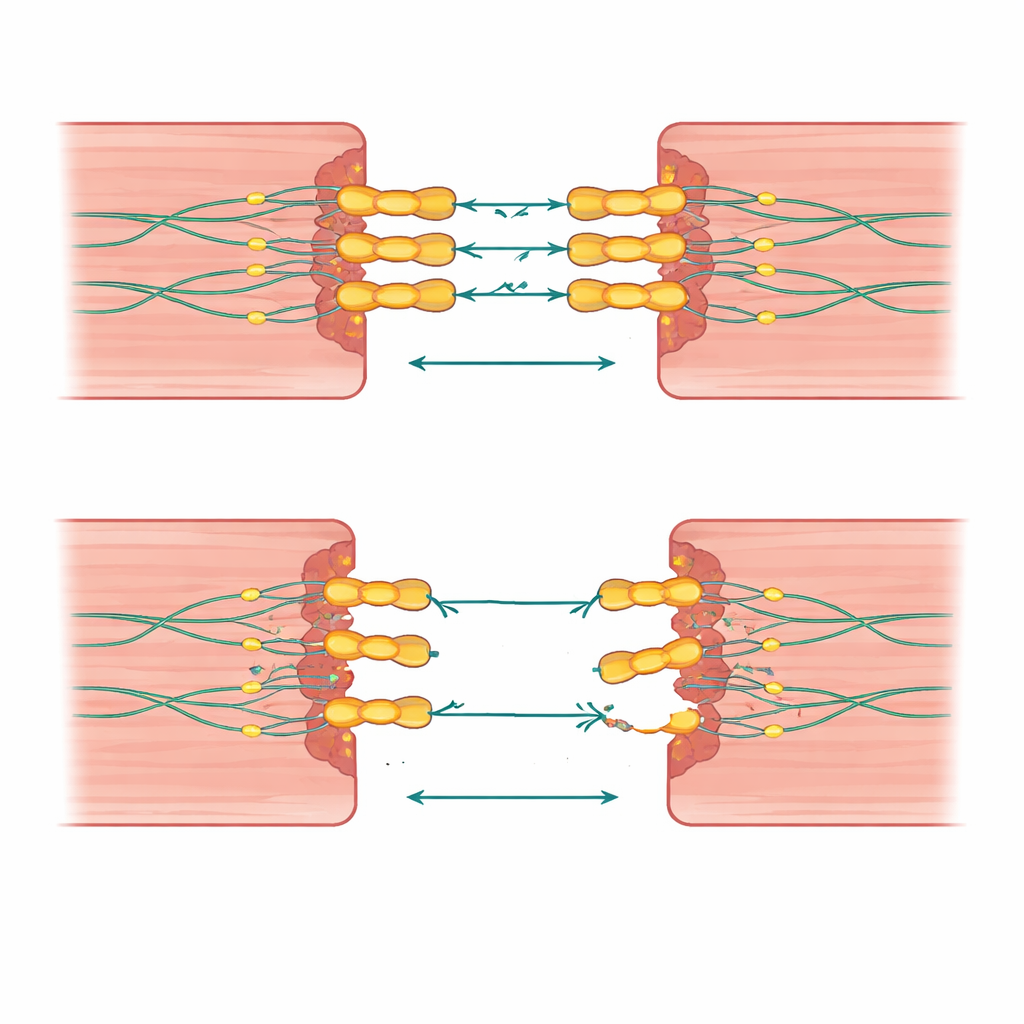
Quando un colpo non basta
Un’intuizione importante di questo lavoro è che il numero e la combinazione di varianti contano. Le persone che hanno ereditato due copie difettose di desmogleina‑2, o una variante in desmogleina‑2 insieme a una variazione in un gene correlato del “collante” cardiaco, tendevano ad ammalarsi più giovani e presentavano danni più estesi a entrambi i lati del cuore. Alcune famiglie portavano grandi delezioni o duplicazioni che rimuovevano o raddoppiavano non solo la desmogleina‑2 ma anche geni vicini, collegando ancora una volta queste alterazioni a malattie aggressive e a cluster di morti improvvise. Al contrario, molti parenti con una singola variante avevano sintomi lievi o assenti, suggerendo che geni di background e fattori di vita come l’esercizio fisico possano spostare l’equilibrio tra rischio silente e malattia manifesta.
Dalla forma della proteina al rischio per il paziente
Per collegare il codice DNA agli effetti fisici, il gruppo ha utilizzato modelli proteici 3D avanzati per vedere come specifiche sostituzioni potessero allentare l’impalcatura della desmogleina‑2. Le varianti che deformavano le anse di legame del calcio o spezzavano punti di attacco chiave erano previste come destabilizzanti per la proteina e indebolivano l’adesione cellula‑cellula. Questi indizi strutturali sono stati integrati nel sistema di classificazione, contribuendo a spostare alcune varianti borderline verso una valutazione più probabile di dannosità o di benignità. Questo ponte tra modellazione molecolare e dati clinici spinge il test genetico oltre la semplice lettura del codice verso una comprensione più funzionale.
Cosa significa per pazienti e famiglie
Per le famiglie coinvolte dalla cardiomiopatia aritmogena, questo studio offre sia cautela sia indicazioni pratiche. Mostra che non tutte le varianti di desmogleina‑2 sono una condanna a malattia cardiaca grave, ma che certi schemi—soprattutto multiple varianti o alterazioni in regioni critiche della proteina—sono associati a problemi più precoci e severi. Gli autori sostengono che le persone portatrici di queste varianti non debbano essere considerate “sane fino a prova contraria”, ma seguite per tutta la vita con controlli del ritmo e immagini personalizzate. Il loro approccio integrativo—che fonde genetica di big‑data, studi familiari dettagliati e struttura proteica—indica la strada verso stime di rischio più precise e una consulenza più sicura quando una variante di desmogleina‑2 compare in un test genetico.
Citazione: Pinci, S., Celeghin, R., Martini, M. et al. Integrative genomic and literature assessment of desmoglein 2-related arrhythmogenic cardiomyopathy with Italian cohort validation. Commun Med 6, 145 (2026). https://doi.org/10.1038/s43856-026-01416-w
Parole chiave: cardiomiopatia aritmogena, desmogleina-2, malattia cardiaca ereditaria, rischio genetico, morte cardiaca improvvisa