Clear Sky Science · it
Blocco selettivo dell’attivazione latente di TGF-β1 sopprime la fibrosi tissutale con buona sicurezza
Perché la cicatrizzazione nascosta conta
Molte malattie croniche danneggiano silenziosamente i nostri organi depositando tessuto cicatriziale rigido, un processo chiamato fibrosi. Questa cicatrizzazione può progressivamente compromettere la funzione normale del fegato, dei reni, dei polmoni e persino intorno ai tumori, dove può anche attenuare l’efficacia delle moderne immunoterapie oncologiche. La proteina TGF-β1 è al centro di questo processo fibrotico, ma bloccarla ovunque nell’organismo si è rivelato pericoloso. Questo studio descrive un nuovo anticorpo, chiamato SOF10, progettato per bloccare solo l’attivazione dannosa di TGF-β1 preservandone i ruoli essenziali, mostrando benefici promettenti in modelli animali di malattia epatica, insufficienza renale e cancro.
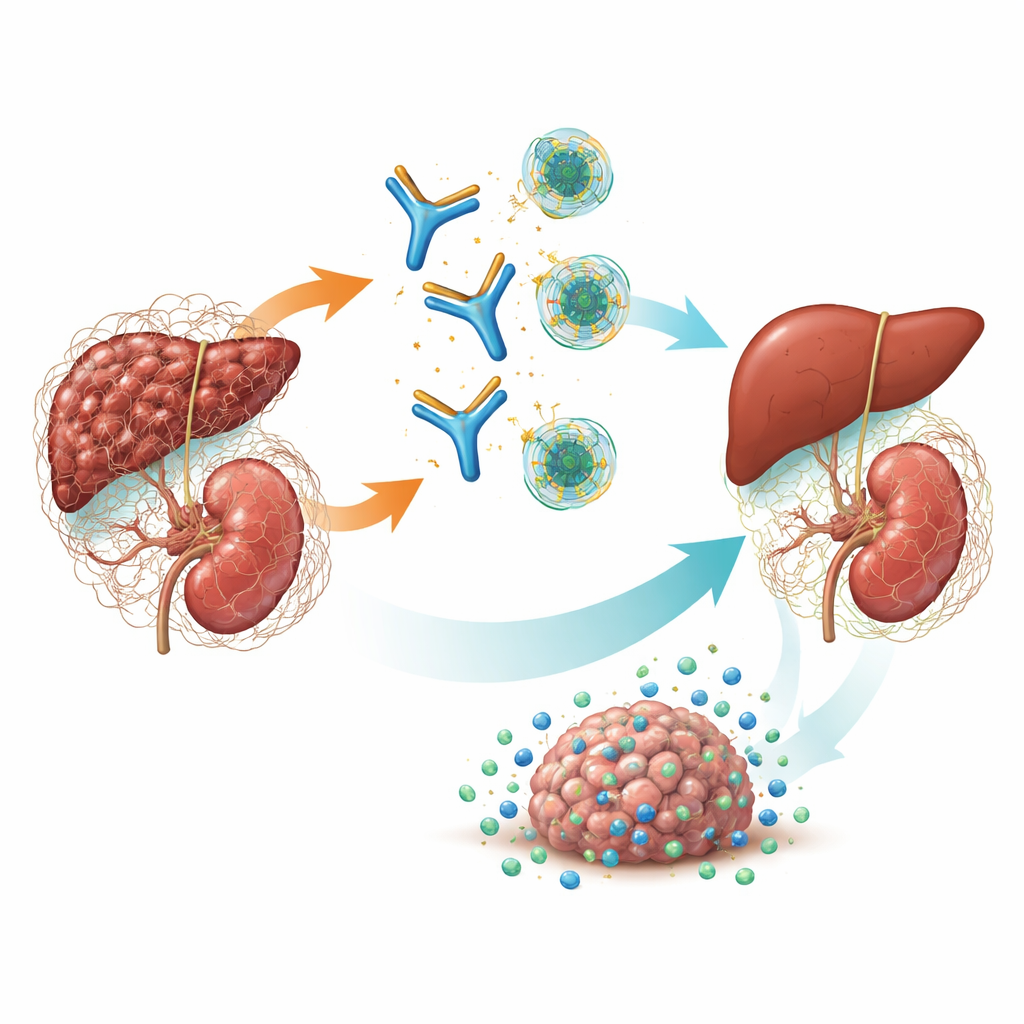
Un interruttore maestro per cicatrizzazione e cancro
TGF-β è una potente molecola di segnalazione che aiuta a controllare come le cellule crescono, guariscono e interagiscono con il sistema immunitario. Nelle malattie croniche, una forma—TGF-β1—spinge i fibroblasti a costruire tessuto connettivo in eccesso, portando all’irrigidimento e al fallimento degli organi. Modellando inoltre una conchiglia fibrotica e immunosoppressiva intorno ai tumori, impedisce alle cellule immunitarie e ai farmaci di raggiungere le cellule cancerose. Farmaci precedenti hanno cercato di spegnere tutte e tre le forme di TGF-β contemporaneamente, ma questa “pan-inibizione” ha causato gravi effetti collaterali come danni alle valvole cardiache, sanguinamenti e tumori cutanei. Studi genetici e modelli precedenti suggerivano che TGF-β1 sia il principale responsabile nella fibrosi renale e in molti tumori solidi, aprendo la possibilità che colpire con cura solo questa isoforma possa essere sia efficace sia più sicuro.
Bloccare TGF-β1 nella sua forma inattiva
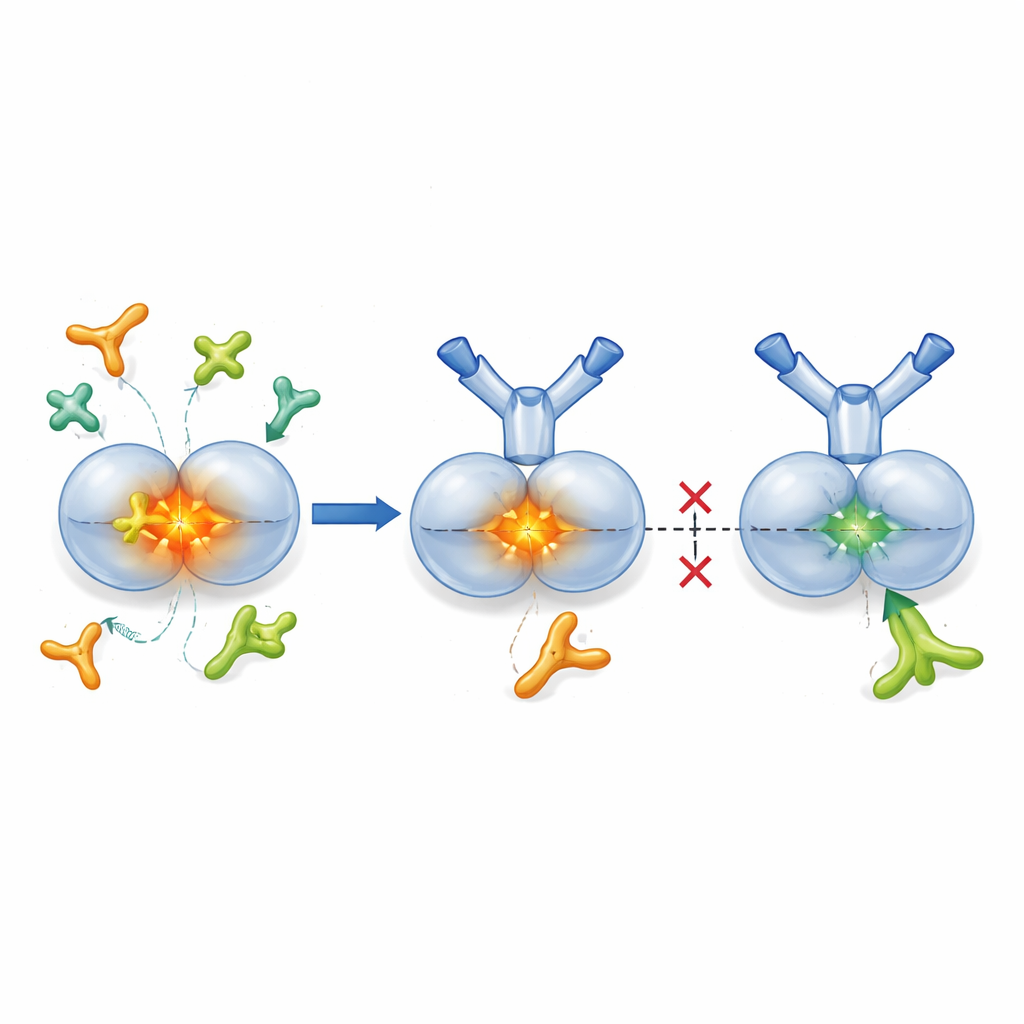
TGF-β1 è normalmente prodotto in un involucro “latente”, dove il nucleo attivo è avvolto da una proteina partner che lo mantiene spento fino al momento del bisogno. Enzimi chiamati proteasi e certe proteine di superficie cellulare note come integrine possono aprire questo involucro, rilasciando TGF-β1 attivo nel tessuto circostante. I ricercatori hanno ingegnerizzato SOF10, un anticorpo umanizzato che si lega solo alla forma latente di TGF-β1, non all’ormone attivo né alle altre isoforme. Studi strutturali con cristallografia a raggi X hanno mostrato che SOF10 si inserisce nell’interfaccia tra le due metà del complesso latente, stabilizzandolo come una morsa. Nei test in vitro ciò ha impedito alle proteasi e a una integrina (αvβ8) di liberare TGF-β1 attivo, lasciando invece in gran parte intatta un’altra integrina (αvβ6)—importante per mantenere l’equilibrio immunitario nei tessuti sani. In pratica, SOF10 silenzia selettivamente le vie di attivazione dannose preservando una via omeostatica chiave.
Proteggere fegato e reni dal danno lento
Per valutare se questa morsa selettiva su TGF-β1 potesse effettivamente limitare la cicatrizzazione, il team ha testato SOF10 in diversi modelli murini. In un modello alimentare a insorgenza rapida di steatoepatite che progredisce verso fibrosi epatica, il trattamento con SOF10 ha ridotto l’espressione epatica di geni rispondenti a TGF-β e di geni per la sintesi del collagene, e ha diminuito l’idrossiprolina, un marcatore chimico del tessuto cicatriziale accumulato. In due diversi modelli renali—un modello chirurgico di ostruzione che induce fibrosi interstiziale e un modello genetico di sindrome di Alport che sviluppa sia cicatrizzazione glomerulare sia insufficienza renale—SOF10 ha ridotto l’attività dei geni fibrotici, il contenuto di collagene e ha visibilmente ridotto le aree cicatrizzate al microscopio. Nel modello cronico di Alport, i test ematici hanno mostrato un miglioramento della funzione renale, e questi benefici erano paragonabili a quelli di un anticorpo più ampio contro TGF-β, ma senza bloccare le altre isoforme di TGF-β.
Liberare il sistema immunitario all’interno dei tumori
Poiché il tessuto fibrotico attorno ai tumori può agire sia come barriera fisica sia come freno immunitario, i ricercatori hanno verificato se SOF10 potesse migliorare la risposta ai farmaci inibitori dei checkpoint. In modelli murini di carcinoma mammario e colon che normalmente rispondono poco alla terapia anti–PD-L1, l’aggiunta di SOF10 ha rallentato significativamente la crescita tumorale, mentre SOF10 o anti–PD-L1 da soli hanno avuto scarso effetto. I tumori degli animali trattati in combinazione contenevano più cellule CD8 citotossiche e più degli enzimi tossici che utilizzano per eliminare le cellule tumorali. I fibroblasti isolati da questi tumori mostravano minore attività nelle vie di costruzione del collagene e della matrice ma maggiore attività nelle vie dell’interferone e della presentazione dell’antigene, uno spostamento verso uno stroma più favorevole all’immunità. Questi cambiamenti rispecchiavano strettamente quanto osservato con il blocco ampio di TGF-β, suggerendo che mirare solo al TGF-β1 latente può riprogrammare l’ambiente tumorale in modo simile.
Segnali di sicurezza negli animali
Poiché i tentativi precedenti di bloccare ampiamente TGF-β hanno incontrato problemi di sicurezza, il team ha condotto studi di tossicità di 13 settimane in topi e in scimmie cynomolgus, somministrando ripetutamente alte dosi di SOF10. Il farmaco si è comportato come un anticorpo tipico nel circolo ematico e, su un’ampia gamma di dosi, non sono stati osservati segni di danno nei principali organi, nei conteggi delle cellule del sangue o nella funzione cardiaca e polmonare. Le dosi più alte testate—fino a 200 mg/kg ogni due settimane nei topi e 100 mg/kg nelle scimmie—sono state designate come livelli senza effetti nocivi osservati. Questo profilo di sicurezza supporta l’idea che risparmiare TGF-β2, TGF-β3 e l’attivazione mediata da αvβ6 riduca i rischi visti con approcci precedenti meno selettivi.
Cosa potrebbe significare per i pazienti
Nel complesso, i risultati suggeriscono che bloccare TGF-β1 nella sua conchiglia inattiva—piuttosto che cancellare tutta la segnalazione di TGF-β—può alleviare la cicatrizzazione in più organi, migliorare la funzione renale e rendere i tumori ostinati più vulnerabili all’immunoterapia, il tutto con segnali di sicurezza incoraggianti nei test animali. Sebbene siano necessari studi clinici sull’uomo per confermare questi benefici e monitorare gli effetti a lungo termine, SOF10 e strategie simili potrebbero aprire una nuova via per trattare malattie fibrotiche croniche e alcuni tumori, riducendo la cicatrizzazione dannosa preservando al contempo i ruoli di riparazione e bilanciamento immunitario di cui i tessuti hanno ancora bisogno.
Citazione: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
Parole chiave: fibrosi, TGF-beta1, anticorpo monoclonale, malattie del fegato e del rene, immunoterapia oncologica