Clear Sky Science · it
Predizione dell’esito dal profilo spaziale delle proteine nei carcinomi mammari triplo-negativi
Perché conta la disposizione delle cellule tumorali
Quando i medici osservano al microscopio un tumore mammario aggressivo, vedono un paesaggio affollato di cellule tumorali, cellule immunitarie e tessuto di supporto. Ma fino a poco tempo fa la maggior parte dei test si è concentrata su quanto di una determinata molecola è presente, non su dove si trova. Questo studio mostra che l’assetto fisico di proteine e cellule all’interno dei carcinomi mammari triplo-negativi può prevedere l’andamento clinico dei pazienti e introduce un nuovo modo di leggere quei pattern spaziali direttamente dalle immagini ad alta risoluzione.
Osservare il tessuto tumorale a molti colori
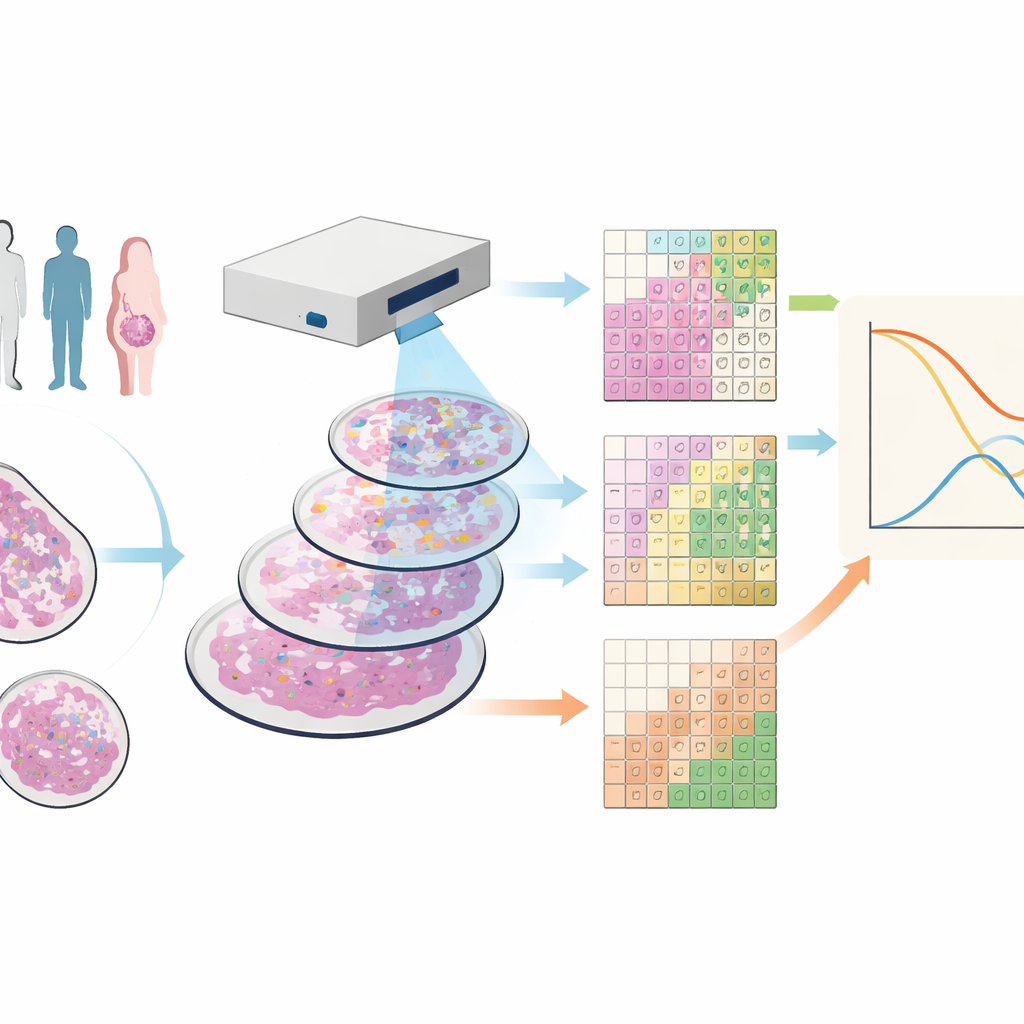
I ricercatori hanno lavorato su campioni di tessuto di 88 persone affette da carcinoma mammario triplo-negativo, una forma della malattia che è priva di comuni bersagli farmacologici e spesso presenta una prognosi sfavorevole. Hanno utilizzato una tecnica chiamata imaging con spettrometria di massa, che colora ogni campione con dozzine di anticorpi marcati con metalli. Sotto uno scanner specializzato, questo produce immagini in cui ogni punto del tessuto ha un’impronta dettagliata di molte proteine diverse, rivelando simultaneamente cellule tumorali, varie cellule immunitarie, vasi sanguigni e fibre strutturali.
Suddividere l’immagine in riquadri invece che in cellule
La maggior parte degli strumenti attuali tenta di tracciare confini attorno a ogni cellula e poi classificarle per tipo, un processo che può essere soggetto a errori e lento, specialmente nei tagli di tessuto sottili dove le cellule sono solo parzialmente rappresentate. Il gruppo ha invece creato SparTile, un metodo che evita di delineare i contorni cellulari individuali. SparTile spezza ogni immagine in molti quadrati piccoli sovrapposti, o riquadri, e usa tecniche matematiche per imparare pattern ricorrenti di combinazioni proteiche all’interno di quei riquadri. Innanzitutto raggruppa i riquadri in regioni ampie—tumore, tessuto di supporto (stroma) o zone ricche di cellule immunitarie—e poi suddivide ciascuna regione in “microambienti” più specifici, ognuno con la propria miscela di proteine e tipi cellulari vicini.
Quartieri nascosti legati all’esito dei pazienti
Con questi microambienti mappati, gli scienziati hanno misurato quanto ciascun pattern fosse presente nel campione di ogni paziente e hanno confrontato questi dati con la sopravvivenza a lungo termine. Sono emerse diverse correlazioni rilevanti. Un microambiente centrato sul tumore, ricco di una proteina chiamata MX1 e di marcatori delle cellule mieloidi, è risultato associato a un rischio di morte molto più elevato. Un altro pattern tumorale contrassegnato dalla vimentina—segno che le cellule tumorali hanno assunto uno stato più mobile e invasivo—ha anch’esso mostrato una forte correlazione con una peggiore sopravvivenza. Al contrario, aree dominate da certi linfociti T erano collegate a esiti migliori, mentre le regioni ricche di cellule B hanno mostrato effetti più deboli, probabilmente perché rare nei piccoli nuclei di tessuto analizzati.
Distanza fra tumore e cellule immunitarie come segnale di rischio
Oltre alla presenza di particolari quartieri, contavano anche le loro relazioni spaziali. Il gruppo ha valutato quanto fossero vicine le zone tumorali e le zone mieloidi calcolando una misura statistica di quanto i loro segnali proteici si sovrapponessero nello spazio. I pazienti i cui tumori presentavano aree ricche di cellule mieloidi incuneate fra cellule tumorali tendevano ad avere prognosi peggiori rispetto a quelli in cui le due popolazioni erano più separate. Questa misura di “distanza” è rimasta un forte predittore di rischio anche dopo aver tenuto conto dei fattori clinici standard, e la sua importanza è stata confermata su due set di immagini di carcinoma mammario indipendenti provenienti da altri gruppi di ricerca.
Un nuovo modo di leggere il paesaggio tumorale
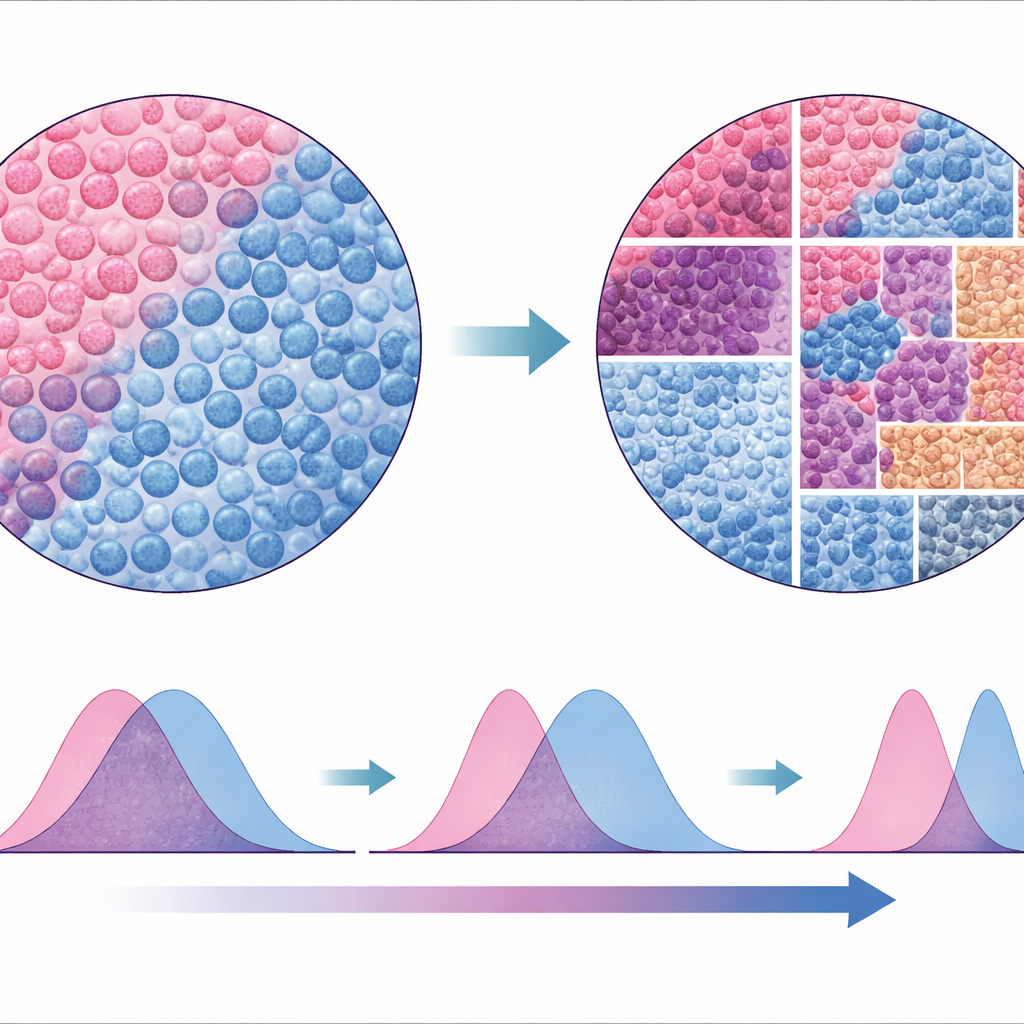
Per verificare la robustezza dell’approccio, gli autori hanno confrontato SparTile con i metodi tradizionali che si basano sulla segmentazione e classificazione delle singole cellule e poi costruiscono intorni attorno a esse. Pur recuperando alcuni degli stessi pattern, le analisi basate sulle cellule si sono rivelate meno coerenti tra i dataset e meno affidabili nell’individuare certi microambienti rischiosi, come quelli che coinvolgono MX1 e cellule mieloidi. Poiché SparTile lavora direttamente sulle immagini proteiche grezze, evita molte delle ipotesi e delle insidie tecniche degli approcci cella per cella, pur potendo essere integrato con essi in seguito quando sono necessari tipi cellulari dettagliati per progettare esperimenti o terapie.
Cosa significa per i pazienti e per le cure future
Questo lavoro mostra che non contano solo gli ingredienti, ma anche la loro disposizione per prevedere l’andamento di un paziente con carcinoma mammario triplo-negativo. Convertendo immagini complesse multi-proteiche in pattern spaziali interpretabili e in misure di distanza semplici, SparTile offre un modo per individuare pazienti ad alto rischio a partire da piccoli campioni di tessuto e per scoprire disposizioni biologiche che potrebbero essere mirate da future terapie. Pur richiedendo ulteriori validazioni prima di poter guidare la pratica clinica di routine, l’approccio indica un futuro in cui la “mappa” di un tumore diventa importante quanto il suo elenco molecolare.
Citazione: Foroughi pour, A., Wu, TC., Noorbakhsh, J. et al. Prediction of outcome from spatial Protein profiling of triple-negative breast cancers. Commun Med 6, 133 (2026). https://doi.org/10.1038/s43856-026-01400-4
Parole chiave: carcinoma mammario triplo-negativo, microambiente tumorale, proteomica spaziale, imaging con spettrometria di massa, biomarcatori prognostici