Clear Sky Science · it
IdentifiHR prevede la carenza di ricombinazione omologa nel carcinoma ovarico sieroso di alto grado usando l’espressione genica
Perché questa ricerca è importante per le pazienti con cancro ovarico
Per le persone con carcinoma ovarico sieroso di alto grado, una delle forme più letali di cancro ovarico, le scelte terapeutiche possono essere questione di vita o di morte. Circa metà di questi tumori presenta una vulnerabilità nei meccanismi di riparazione del DNA, che li rende particolarmente sensibili a determinati farmaci detti inibitori PARP. La sfida è stabilire, per ciascuna paziente, se il proprio tumore possieda questa vulnerabilità. Questo studio presenta IdentifiHR, un nuovo strumento che legge i modelli di attività genica, anziché basarsi solo sulle mutazioni del DNA, per prevedere quali tumori hanno difetti nella riparazione del DNA e potrebbero trarre maggior beneficio da questi trattamenti mirati.
Dalle cicatrici del DNA ai modelli di attività genica
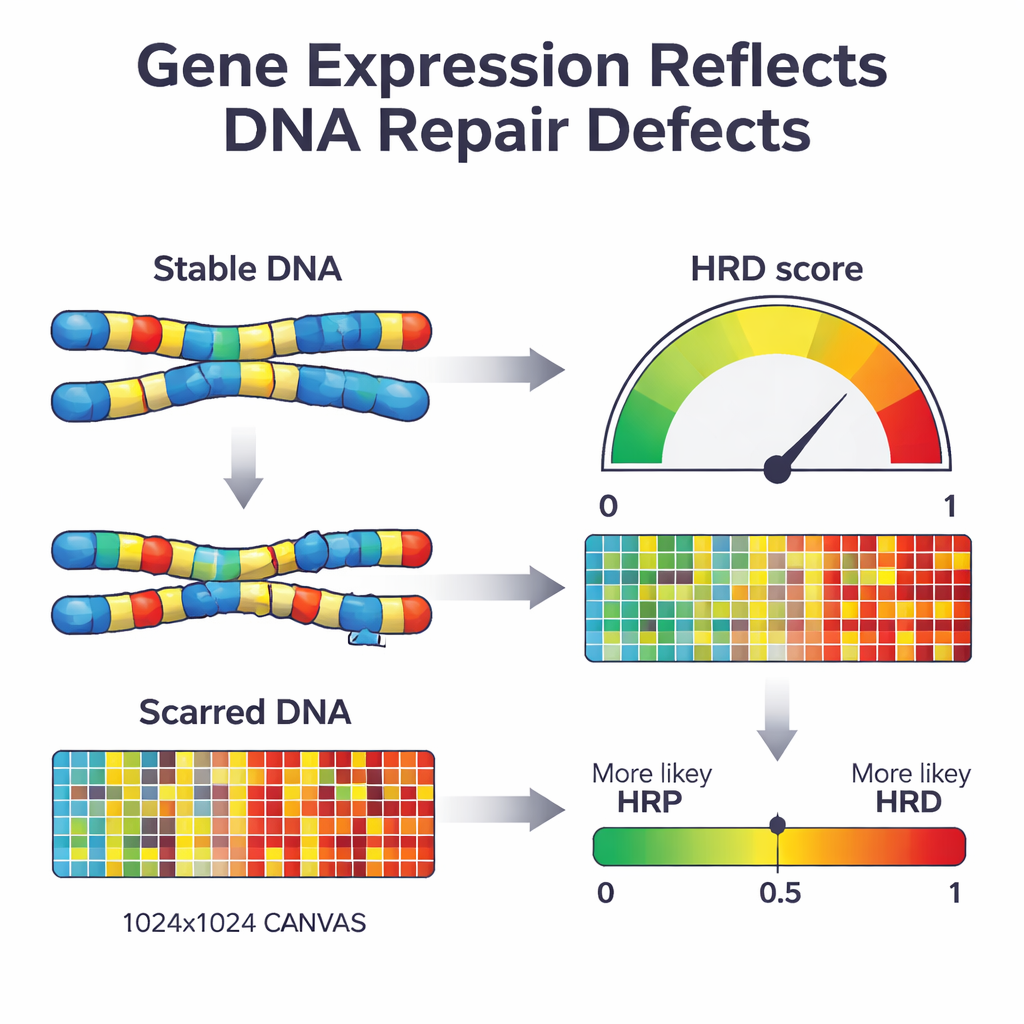
Quando una cellula perde una via di riparazione importante chiamata ricombinazione omologa, inizia a riparare il DNA con metodi più soggetti a errori. Nel tempo questo lascia un pattern caratteristico di “cicatrici” nel genoma: regioni mancanti, copie in più e segmenti cromosomici frammentati. I test clinici esistenti cercano queste cicatrici direttamente nel DNA o mutazioni specifiche in geni chiave come BRCA1 e BRCA2. Pur essendo potenti, questi test richiedono sequenziamenti del DNA estesi e non sempre catturano lo stato attuale della capacità di riparazione del tumore. Gli autori si sono chiesti se un diverso livello biologico — il profilo dei geni attivati o silenziati nel tumore — potesse funzionare come una lettura in tempo reale di questo danno e servire a classificare i tumori come carenti o competenti nella riparazione.
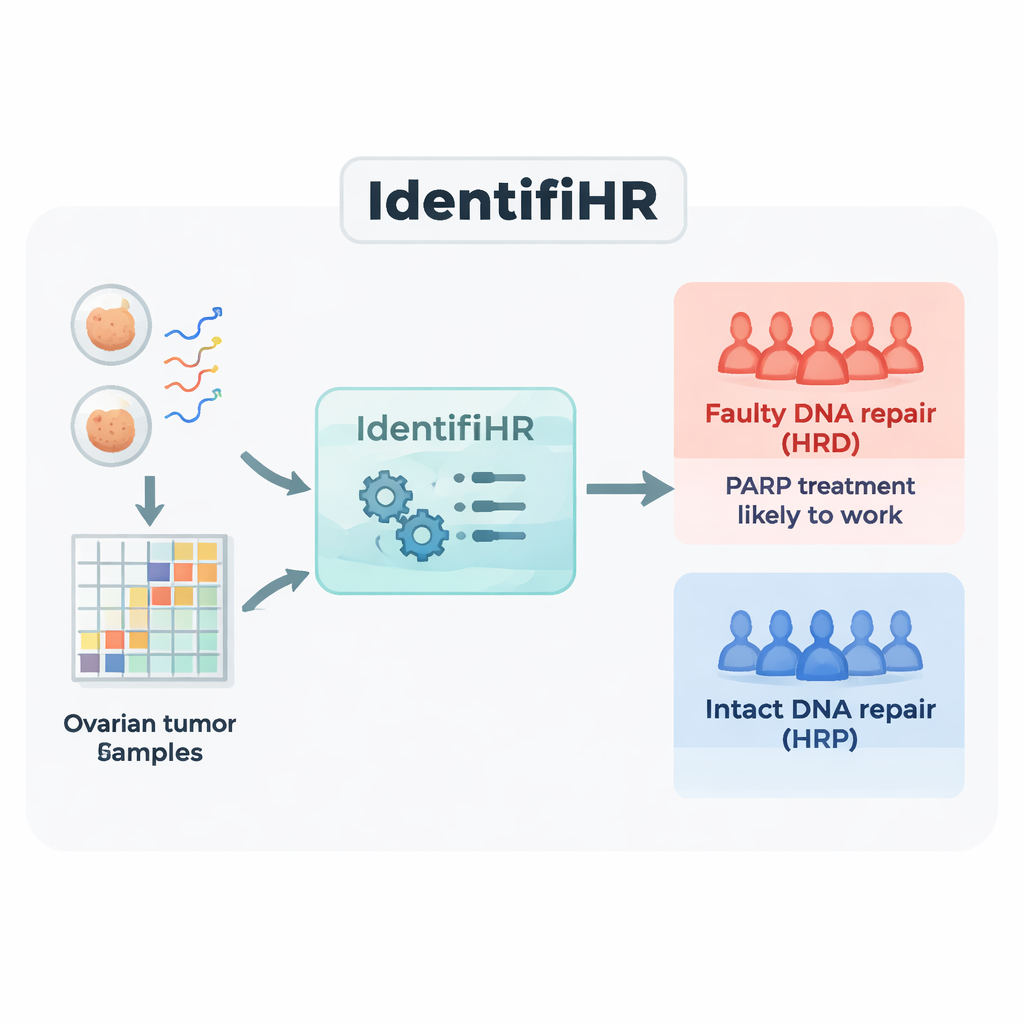
Costruire un predittore basato sui geni: IdentifiHR
Il team ha iniziato con dati di RNA sequencing provenienti da 361 tumori ovarici in una grande risorsa pubblica, The Cancer Genome Atlas. L’RNA sequencing misura quali geni sono attivi, e in quale misura, in ciascun campione. Hanno diviso i tumori in un gruppo di addestramento e uno di test, etichettando ogni caso come carente di riparazione (HRD) o competente nella riparazione (HRP) usando lo standard attuale basato sul DNA che combina diverse misure di cicatrici genomiche. Nei tumori di addestramento hanno identificato 2.604 geni la cui attività differiva in modo consistente tra i tumori HRD e HRP. Molti di questi geni erano collocati in regioni del genoma già note per essere ripetutamente amplificate o delezionate nei tumori con difetti di riparazione, a indicare che il segnale dell’espressione genica rispecchiava il danno del DNA sottostante.
Una firma di 209 geni che riflette lo stato di riparazione
Successivamente i ricercatori hanno usato un approccio di machine learning noto come regressione logistica penalizzata per ridurre la lista di 2.604 geni ai più informativi. Il modello risultante, chiamato IdentifiHR, si basa sull’attività di appena 209 geni per stimare la probabilità che un tumore sia carente nella riparazione. Interessante notare che solo uno di questi geni è un classico gene di riparazione del DNA; la maggior parte sono geni ordinari la cui attività è alterata a causa di cambiamenti più ampi nella struttura cromosomica. IdentifiHR non fornisce semplicemente un’etichetta sì/no: produce un punteggio di probabilità che varia in modo continuo con il punteggio di danno basato sul DNA, riflettendo l’idea che la carenza di riparazione esista su uno spettro piuttosto che come uno stato netto acceso/spento.
Validazione dello strumento su più coorti di pazienti
Gli autori hanno testato con rigore IdentifiHR in tre set di dati indipendenti che non erano mai stati usati per l’addestramento. Nel sottoinsieme non utilizzato di The Cancer Genome Atlas, il modello ha distinto correttamente tumori HRD da HRP in circa l’85% dei casi. Ha ottenuto prestazioni analoghe — circa l’86% di accuratezza — in uno studio australiano separato che includeva non solo tumori primari ma anche campioni prelevati all’autopsia, da liquido addominale (ascite) e da tube di Falloppio normali, il sito probabile in cui molti di questi tumori originano. In ogni campione di tube di Falloppio normali, IdentifiHR ha previsto correttamente una riparazione del DNA intatta. Lo strumento ha funzionato anche su dati single-cell “pseudobulkati”, dove migliaia di singole cellule tumorali sono state combinate computazionalmente per imitare un campione bulk, raggiungendo nuovamente circa l’84% di accuratezza. In questi test, IdentifiHR ha eguagliato o superato le prestazioni di diversi metodi basati sull’espressione genica sviluppati originariamente per altri tumori o per prevedere punteggi di danno correlati.
Come questo potrebbe cambiare ricerca e assistenza clinica
Poiché IdentifiHR si basa su dati di RNA, che sono spesso più economici e facili da raccogliere rispetto ai profili del DNA dell’intero genoma, offre un modo pratico per ricercatori — e potenzialmente, in futuro, per i clinici — di stimare lo stato della riparazione del DNA quando sono disponibili solo dati di espressione genica. Il modello è distribuito come pacchetto R open-source, quindi qualsiasi gruppo con dati di sequenziamento adeguati può applicarlo. Pur non sostituendo ancora i test del DNA considerati gold standard, e nonostante rimanga da valutare la sua capacità di catturare cambiamenti più sottili come il ripristino della riparazione, IdentifiHR fornisce una nuova e potente lente per identificare quali tumori ovarici hanno più probabilità di rispondere agli inibitori PARP e farmaci simili. Per le pazienti, questo lavoro avvicina il campo a decisioni terapeutiche più precise e guidate dalla biologia reale delle loro cellule tumorali.
Citazione: Weir, A.L., Lee, S.C., Li, M. et al. IdentifiHR predicts homologous recombination deficiency in high-grade serous ovarian carcinoma using gene expression. Commun Med 6, 119 (2026). https://doi.org/10.1038/s43856-026-01387-y
Parole chiave: cancro ovarico, riparazione del DNA, carenza di ricombinazione omologa, espressione genica, apprendimento automatico