Clear Sky Science · it
Deficit di ricombinazione omologa nel carcinoma mammario primario ER-positivo e HER2-negativo
Perché questo è importante per le pazienti con cancro al seno
La maggior parte dei carcinomi mammari rientra in un ampio gruppo definito come recettore degli estrogeni positivo e HER2-negativo. Questi tumori vengono di solito trattati con farmaci che bloccano gli ormoni, talvolta in combinazione con chemioterapia. Tuttavia molte pazienti recidivano e i medici non dispongono di strumenti precisi per stabilire chi ha davvero bisogno di terapie intensive o potrebbe beneficiare di nuovi farmaci mirati. Questo studio esplora una debolezza specifica in alcuni tumori — chiamata deficit di ricombinazione omologa, o HRD — che rende le cellule tumorali meno efficaci nel riparare il DNA rotto, aprendo potenzialmente la strada a terapie più personalizzate.
Una debolezza nascosta presente solo in alcuni tumori
La ricombinazione omologa è uno dei principali meccanismi cellulari per riparare rotture pericolose del DNA. Quando questo sistema fallisce — spesso a causa di alterazioni in geni noti come BRCA1, BRCA2, PALB2 o RAD51C — le cellule accumulano mutazioni e possono diventare particolarmente sensibili a certi farmaci, inclusi chemioterapici al platino e inibitori di PARP. L’HRD è comune in una forma aggressiva di carcinoma mammario chiamata triple-negativo, ma il suo ruolo nel più comune gruppo ER-positivo, HER2-negativo è stato incerto. Per chiarirlo, i ricercatori hanno analizzato 502 di questi tumori dallo studio svedese SCAN-B mediante sequenziamento dell’intero genoma, insieme a dati abbinati sull’espressione genica, metilazione del DNA, terapie ricevute e outcome a lungo termine.
Come è stato condotto lo studio
Tutti i tumori sono stati raccolti al momento dell’intervento chirurgico, prima di qualsiasi trattamento farmacologico, fornendo un’istantanea chiara della loro biologia originale. Il gruppo ha utilizzato uno strumento sofisticato di riconoscimento dei pattern, HRDetect, per leggere le “impronte mutazionali” lasciate nel DNA tumorale quando la ricombinazione omologa è compromessa. I tumori sono stati etichettati come HRD se superavano una soglia di probabilità rigorosa. Gli scienziati hanno anche confrontato diversi metodi di rilevamento dell’HRD — da altri punteggi basati sul DNA a un test di espressione genica basato su RNA — per valutare quanto affidabilmente i vari approcci concordino. Inoltre, hanno esaminato caratteristiche più ampie come il carico mutazionale complessivo, i pattern di guadagni e perdite cromosomiche, l’attività genica legata al sistema immunitario e i segnali chimici sul DNA (metilazione) che possono attivare o spegnere i geni.
Quanto è comune l’HRD e cosa lo causa?
I ricercatori hanno rilevato che solo l’8,4% dei tumori ER-positivi, HER2-negativi nel loro campione sequenziato mostrava evidenze robuste di HRD — molto meno rispetto al circa 60% osservato nella malattia triple-negativa. Combinando questi dati con informazioni da registri nazionali e altri studi, hanno stimato che circa 1 tumore su 20 in questo sottogruppo clinico, e circa 1 su 9 dei carcinomi mammari complessivi nelle popolazioni dell’Europa occidentale/Nordiche, sia HRD. Nei tumori HRD si è spesso riusciti a identificare una causa plausibile: circa il 70% mostrava danni evidenti a BRCA1, BRCA2, RAD51C o PALB2, tramite mutazioni ereditarie, mutazioni specifiche del tumore o delezioni, o silenziamento epigenetico dei promotori genici. Colpisce il fatto che circa un terzo dei casi HRD fosse dovuto ad ipermetilazione del promotore — un rivestimento chimico che spegne i geni della riparazione del DNA senza modificarne la sequenza. Tuttavia, approssimativamente il 30% dei tumori HRD non mostrava un colpo singolo evidente, suggerendo l’esistenza di vie aggiuntive, ancora da scoprire, che portano a questo difetto di riparazione.
Come appaiono i tumori HRD al microscopio e in clinica
I tumori HRD in questo gruppo comune tendevano a mostrare caratteristiche tipiche di malattia più aggressiva: spesso avevano tassi di divisione cellulare più elevati, livelli più bassi di colorazione per i recettori ormonali e genomi più complessi e ricchi di mutazioni rispetto ai tumori con funzionalità di ricombinazione (HR-proficient). Si riscontravano in quasi tutti i principali sottotipi molecolari, ma erano rari nella più indolente classe Luminal A e relativamente arricchiti in un sottogruppo più piccolo di tipo basal-like. Tuttavia, quando i ricercatori hanno analizzato il profilo di espressione genica e i pattern di metilazione del DNA, i tumori HRD non sono risultati omogenei in un unico profilo facilmente riconoscibile. Le loro espressioni erano diversificate e le differenze all’interno di sottotipi specifici erano modeste. Alcuni tumori HRD, in particolare nei gruppi Luminal B e basal-like, hanno mostrato segnali più elevati di attività immunitaria e una maggiore espressione di PD-L1, suggerendo che potrebbero essere più visibili al sistema immunitario e potenzialmente più sensibili alle immunoterapie.
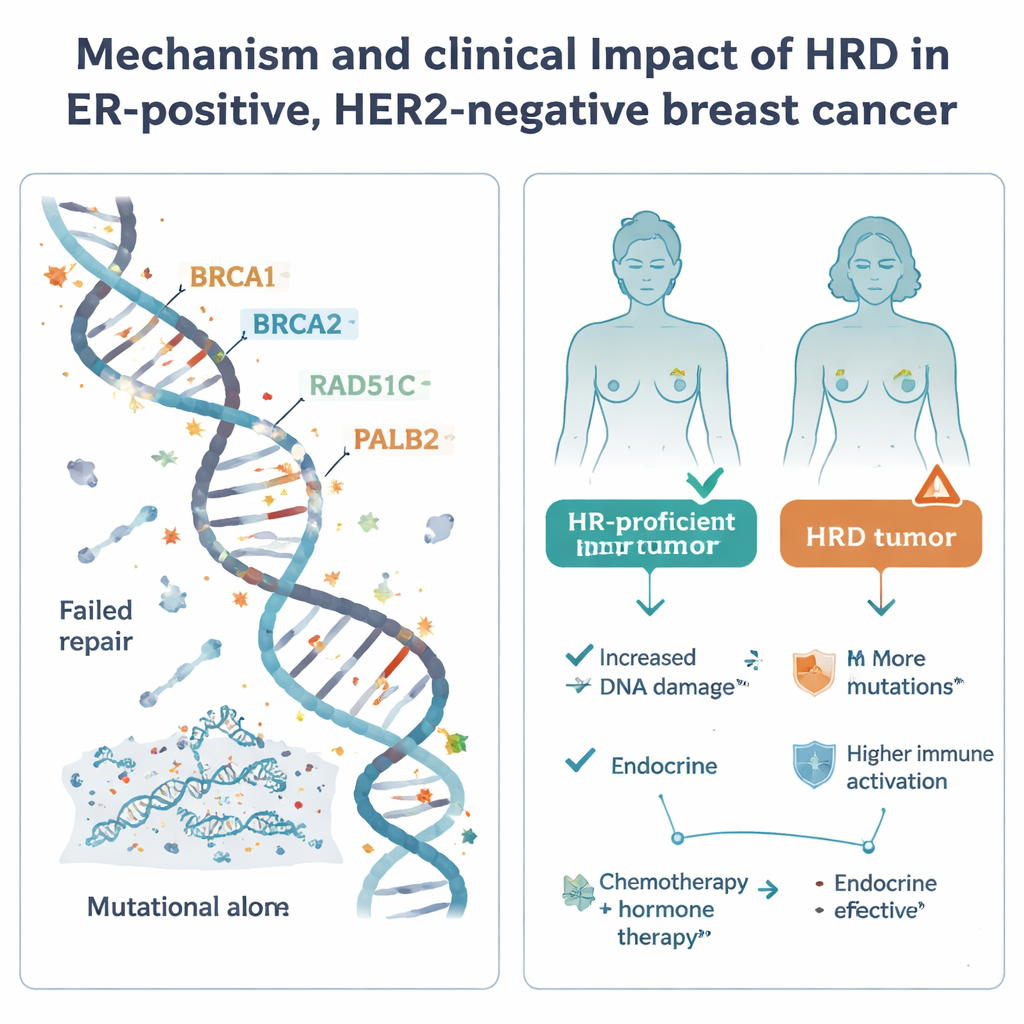
L’HRD influisce sugli esiti delle pazienti?
Lo studio ha poi esaminato come lo stato di HRD si relazionasse agli esiti nel mondo reale sotto la cura standard. Nelle pazienti trattate solo con terapia endocrina dopo l’intervento, i tumori HRD mostravano una tendenza a una sopravvivenza libera da recidiva a distanza peggiore, sebbene il numero di casi HRD fosse ridotto e il risultato non avesse raggiunto la significatività statistica formale. Questo pattern, insieme alle caratteristiche molecolari più aggressive, suggerisce che fare affidamento esclusivamente sulla terapia endocrina potrebbe essere rischioso per le pazienti i cui tumori sono HRD. Al contrario, tra le pazienti che hanno ricevuto sia chemioterapia sia terapia endocrina, lo stato HRD non è risultato chiaramente associato a esiti migliori o peggiori; tutti i gruppi presentavano tassi di recidiva sostanzialmente simili e la chemioterapia potrebbe attenuare parte del rischio aggiuntivo nei tumori HRD.
Cosa significa questo per le scelte terapeutiche future
Per il lettore generale, il messaggio chiave è che soltanto una minoranza di carcinomi mammari ER-positivi, HER2-negativi presenta questa specifica debolezza nella riparazione del DNA, ma quando è presente tende a identificare una malattia più aggressiva che potrebbe non essere ben controllata solo con la terapia ormonale. Il lavoro supporta l’idea che il sequenziamento dell’intero genoma può individuare in modo affidabile l’HRD e chiarirne le cause sottostanti, oltre al semplice test per le mutazioni ereditarie di BRCA1 o BRCA2. Sebbene lo studio non dimostri ancora che modificare il trattamento in base allo stato di HRD migliori la sopravvivenza, fornisce evidenze iniziali che le pazienti con tumori HRD potrebbero beneficiare della chemioterapia e, in futuri trial, di inibitori di PARP o di immunoterapie. In breve, il test per l’HRD potrebbe diventare un elemento di una cassetta degli attrezzi più raffinata per adattare l’intensità della terapia — e le nuove opzioni mirate — alla biologia del cancro mammario di ogni paziente.
Citazione: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
Parole chiave: carcinoma mammario, riparazione del DNA, geni BRCA, sequenziamento del genoma, terapia mirata