Clear Sky Science · it
Sottotipizzazione del morbo di Alzheimer e del morbo di Parkinson utilizzando cartelle cliniche elettroniche longitudinali
Perché è importante per famiglie e pazienti
Si tende a parlare di Alzheimer e Parkinson come se fossero malattie uniche e uniformi. Chi ha però visto un congiunto deteriorarsi sa che non esistono due percorsi uguali. Questo studio pone una domanda semplice ma potente: le cartelle cliniche che raccogliamo nel corso degli anni possono rivelare “varianti” nascoste di queste malattie cerebrali, in modo da orientare in futuro cure più su misura? Usando strumenti moderni per individuare pattern nelle storie sanitarie di oltre 100.000 persone nel Regno Unito, gli autori mostrano che Alzheimer e Parkinson possono ciascuno essere suddivisi in cinque sottotipi distinti, con rischi, sintomi e prospettive diverse.
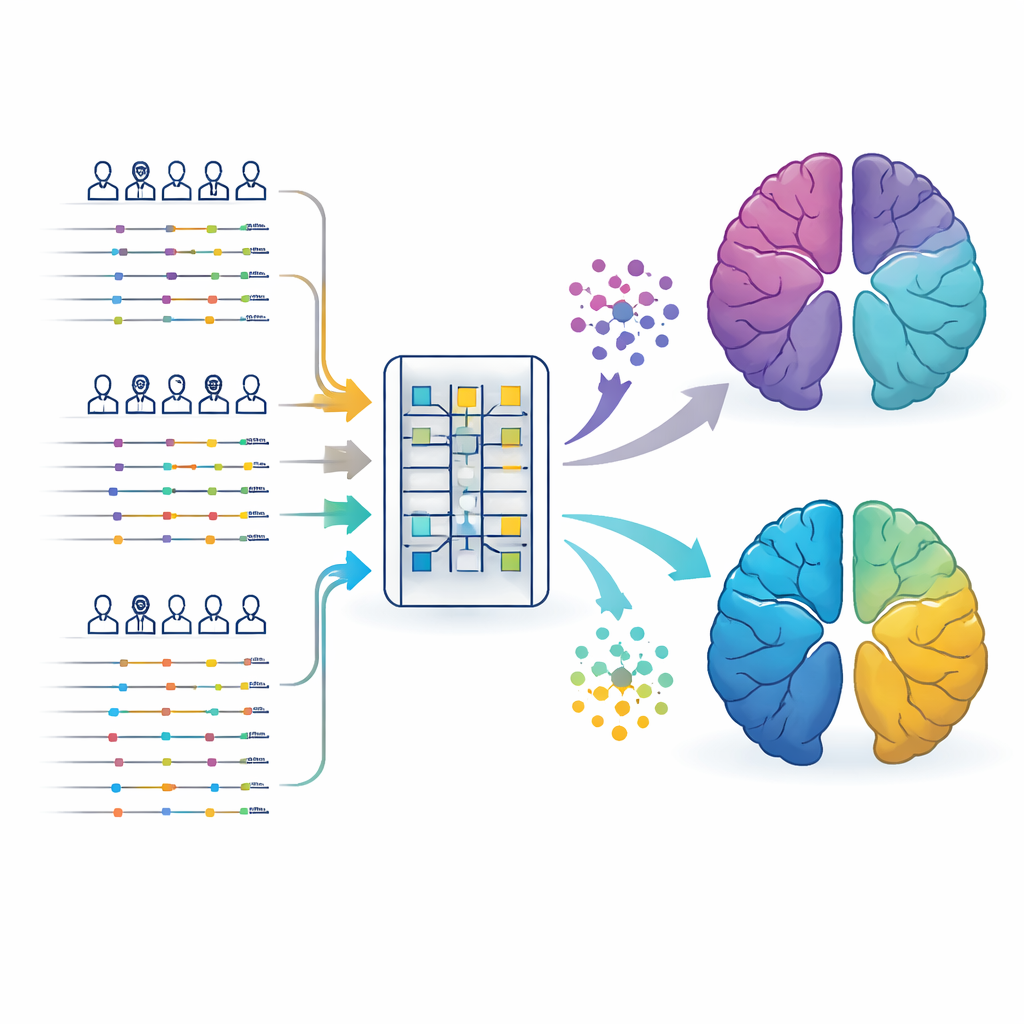
Seguire le storie di salute delle persone per decenni
I ricercatori hanno utilizzato cartelle cliniche elettroniche anonimizzate provenienti da due grandi risorse britanniche: il Clinical Practice Research Datalink, che contiene informazioni dei medici di medicina generale, e lo UK Biobank, un progetto di ricerca di lunga durata che collega visite ambulatoriali, ricoveri ospedalieri, prescrizioni e dati genetici. Si sono concentrati su più di 113.000 persone con Alzheimer e oltre 45.000 con Parkinson, ciascuna con circa due–tre decenni di storia medica antecedente alla diagnosi. Invece di considerare solo esami effettuati dopo il riconoscimento della malattia cerebrale, il team ha inserito queste lunghe “storie” sanitarie marcate nel tempo in un transformer, un tipo di intelligenza artificiale efficace nell’interpretare sequenze come il linguaggio o, in questo caso, una cronologia di visite mediche.
Lasciare che i dati raggruppino i pazienti in gruppi nascosti
Dal record di ciascuna persona il modello ha creato un compatto “impronta” numerica che catturava pattern di malattie, prescrizioni e temporizzazione. Un metodo di clustering ha quindi ordinato queste impronte in gruppi senza indicazioni preconcepite su cosa cercare. Per entrambe le malattie la soluzione più stabile e riproducibile è risultata essere di cinque sottotipi ciascuna. Un gruppo per ciascuna malattia assomigliava a un disturbo cerebrale classico e per lo più “puro”: persone con punteggi di rischio genetico più elevati ma con relativamente pochi altri problemi medici e con esiti migliori dopo la diagnosi. Altri gruppi erano caratterizzati da pattern comparsi anni prima, come una prevalente malattia vascolare, problemi metabolici come diabete e obesità, o una lunga storia di ansia e depressione.
Percorsi diversi, esiti diversi
I cinque sottotipi di Alzheimer variano da una forma comune a esordio tardivo con poche comorbilità, a uno schema dominato da fattori vascolari con ipertensione diffusa, fino a una forma “salute mentale” caratterizzata da depressione e ansia marcate e da un declino cognitivo più rapido. Un altro sottotipo era fortemente associato a diabete, malattia renale e segni di infiammazione cronica, nonostante un rischio ereditario inferiore; questi pazienti tendevano ad ammalarsi prima e ad avere una mortalità più elevata. Un ultimo gruppo di Alzheimer mostrava più malattie cardiache e problemi di movimento e presentava i tassi più elevati di ricovero ospedaliero e mortalità. I sottotipi di Parkinson riflettevano temi simili: un gruppo con storie cliniche relativamente “pulite” e rischio genetico più alto, uno dominato da ipertensione e malattia vascolare, uno con gravi difficoltà dell’umore e del movimento, uno con marcati tratti metabolici e infiammatori e uno che combinava importanti problemi cardiaci e motori con una sopravvivenza particolarmente scarsa.
Geni e fattori di rischio condivisi tra le malattie cerebrali
Poiché lo UK Biobank include dati sul DNA, gli autori hanno potuto verificare se questi sottotipi clinicamente definiti differiscono anche biologicamente. In entrambe le condizioni, tutti i gruppi di pazienti mostravano punteggi di rischio genetico correlati alla malattia più alti rispetto alle persone senza diagnosi, com’era prevedibile. Tuttavia alcune classi presentavano segnali genetici particolarmente forti o deboli. Per esempio, un sottotipo “metabolico–infiammatorio” di Alzheimer mostrava punteggi più bassi per i geni di rischio classici dell’Alzheimer ed era relativamente arricchito per una forma protettiva del gene APOE, suggerendo che condizioni di vita come diabete e obesità possano guidare un quadro simile alla demenza anche quando il rischio ereditario è modesto. Attraverso Alzheimer e Parkinson, i sottotipi plasmati da ipertensione, rischio di ictus o disturbi dell’umore ricorrevano in modi simili, suggerendo che la salute dei vasi sanguigni, il metabolismo e la salute mentale possano orientare il cervello verso diversi modelli di degenerazione più che essere meri effetti collaterali dell’invecchiamento.
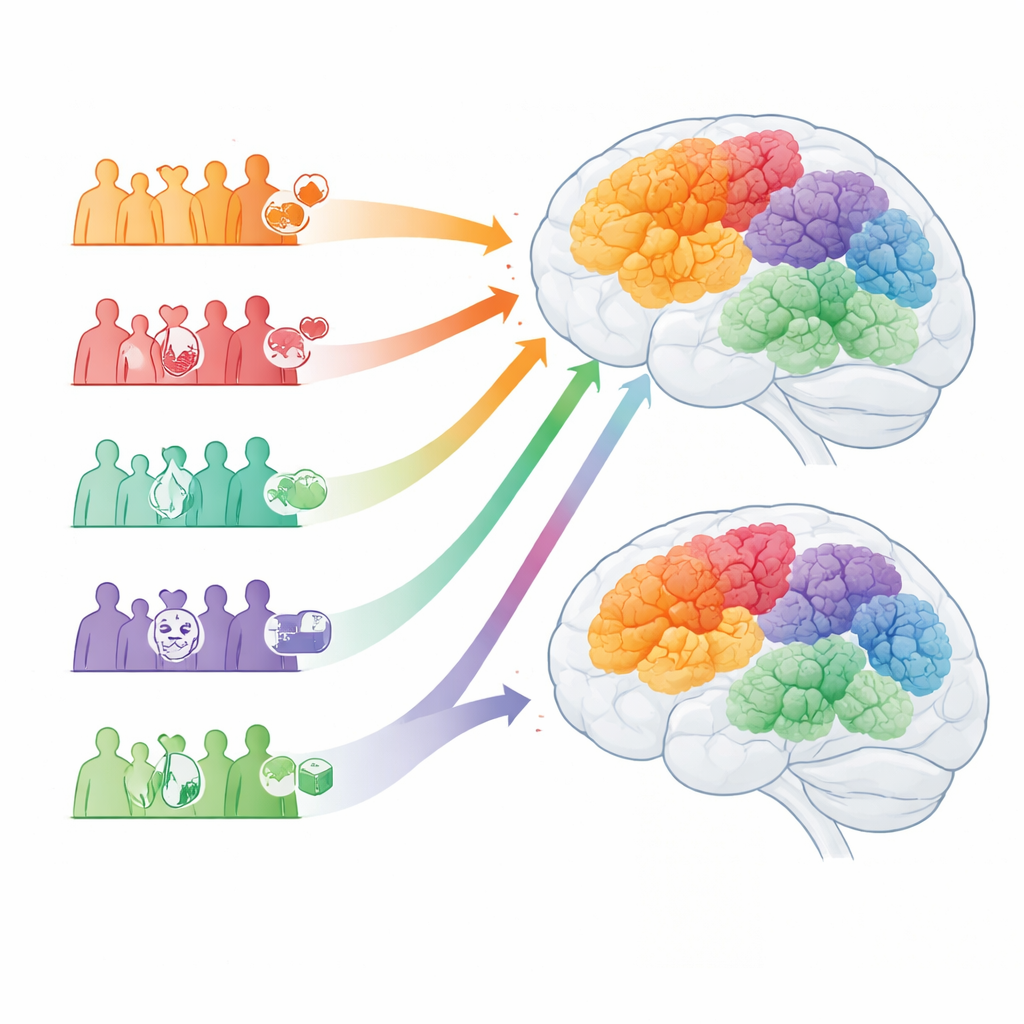
Cosa potrebbe significare per le cure future
Questo lavoro non cambia ancora il modo in cui i medici diagnosticano i pazienti al letto del malato, e gli autori sottolineano che le cartelle cliniche da sole non possono dimostrare con certezza le esatte cause biologiche dietro ogni sottotipo. Tuttavia, mostrando che dati di routine a lungo termine si raggruppano naturalmente in categorie coerenti e significative che corrispondono a differenze nei sintomi, nella sopravvivenza e nella genetica, lo studio fornisce un modello per una profilazione del rischio più precisa e precoce. In futuro, persone con determinate combinazioni di malattia vascolare, diabete o disturbi dell’umore potrebbero essere monitorate più attentamente per pattern specifici di Alzheimer o Parkinson, e gli studi farmacologici potrebbero mirare ai sottotipi più probabilmente responsivi. In sintesi, i risultati sostengono uno spostamento dal trattare queste condizioni come malattie monolitiche verso la loro considerazione come famiglie di percorsi correlati ma distinti—aprendo la porta a prevenzione e terapie più personalizzate.
Citazione: Lian, J., Fan, Z., Petrazzini, B.O. et al. Subtyping Alzheimer’s disease and Parkinson’s disease using longitudinal electronic health records. Nat Aging 6, 612–625 (2026). https://doi.org/10.1038/s43587-026-01085-3
Parole chiave: Sottotipi della malattia di Alzheimer, Sottotipi della malattia di Parkinson, cartelle cliniche elettroniche, apprendimento automatico in neurologia, fattori di rischio nella neurodegenerazione