Clear Sky Science · it
Lo Studio 201: uno studio randomizzato controllato con placebo di fase 2 sulla sicurezza e tollerabilità dell’inibitore della chinasi c‑Abl risvodetinib nella malattia di Parkinson non trattata
Perché questo studio è importante per le famiglie che affrontano il Parkinson
La malattia di Parkinson sottrae progressivamente movimento e autonomia alle persone, e i farmaci attuali alleviano soprattutto i sintomi senza modificare il decorso della malattia. Questo studio ha testato una nuova compresse, risvodetinib, in persone con Parkinson in fase iniziale non ancora trattate per valutarne la sicurezza e se potesse iniziare ad agire sulle cause della malattia. Piuttosto che limitarsi a mascherare tremore o rigidità, il farmaco mira a interferire con un segnale di stress nelle cellule nervose che si ritiene sia alla base della morte cellulare e dell’accumulo di proteine dannose.
Un nuovo bersaglio all’interno delle cellule cerebrali vulnerabili
Da tempo gli scienziati sanno che il Parkinson è associato ad ammassi di una proteina chiamata alfa‑sinucleina che si accumulano all’interno delle cellule nervose e si propagano nel sistema nervoso. Questi aggregati possono attivare un sensore di stress cellulare chiamato c‑Abl, che a sua volta innesca una reazione a catena che porta le cellule verso la morte. Il risvodetinib è una compressa progettata per entrare nel cervello e bloccare selettivamente c‑Abl. Nei modelli animali di Parkinson, una somministrazione quotidiana ha protetto le cellule nervose, ridotto l’accumulo di proteine dannose e migliorato il movimento. Questi risultati incoraggianti hanno portato i ricercatori ad avviare quello che hanno chiamato lo “Studio 201”, il primo studio con somministrazione prolungata di risvodetinib nell’uomo.
Come è stato impostato lo Studio 201
Lo studio ha arruolato 137 adulti negli Stati Uniti recentemente diagnosticati con Parkinson e che non avevano ancora iniziato i farmaci standard anti‑Parkinson. I partecipanti sono stati assegnati casualmente a ricevere una delle tre dosi giornaliere di risvodetinib (50, 100 o 200 milligrammi) o un placebo per 12 settimane, seguite da un follow‑up di sicurezza di due settimane. Né i partecipanti né i medici sapevano chi riceveva il farmaco attivo. L’obiettivo principale non era dimostrare un beneficio sui sintomi, ma monitorare attentamente gli effetti collaterali, gli eventi medici gravi e quante persone riuscivano a proseguire la terapia per l’intero periodo.
Sicurezza, effetti collaterali e funzionamento quotidiano
Il risvodetinib ha superato questo primo test di sicurezza. Circa il 95% delle persone che erano entrate nello studio dopo una breve sospensione regolatoria ha completato il periodo di trattamento di 12 settimane, con un’aderenza quasi perfetta alla terapia. Il numero di persone che ha riportato almeno un nuovo problema medico è stato simile nei gruppi trattati con risvodetinib e con placebo, e non si sono verificati decessi. Eventi gravi, come infezioni o traumi che hanno richiesto cure ospedaliere, sono stati rari e ritenuti non correlati al farmaco di studio. Effetti collaterali comunemente osservati con altri farmaci della stessa ampia famiglia, come stress cardiaco, edema marcato o danno oculare, sono stati minimi o assenti. Nel complesso, il risvodetinib è risultato sorprendentemente ben tollerato per un farmaco che agisce su un enzima di segnalazione potente.
Poiché lo studio è stato breve e relativamente piccolo, non ci si aspettava che mostrasse un miglioramento clinico netto. In effetti, le scale standard per il movimento e per le attività della vita quotidiana sono cambiate poco in 12 settimane, e il punteggio combinato principale sul movimento non è risultato significativamente diverso tra risvodetinib e placebo. Alcune misure hanno mostrato piccoli miglioramenti “nominali” a determinate dosi, come modesti progressi nelle attività quotidiane auto‑valutate, ma questi segnali sono troppo deboli e di breve durata per essere considerati prove che il farmaco migliori i sintomi. È importante sottolineare che il risvodetinib non sembra aver peggiorato complessivamente le funzioni motorie o non motorie.
Uno sguardo al processo patologico nella pelle
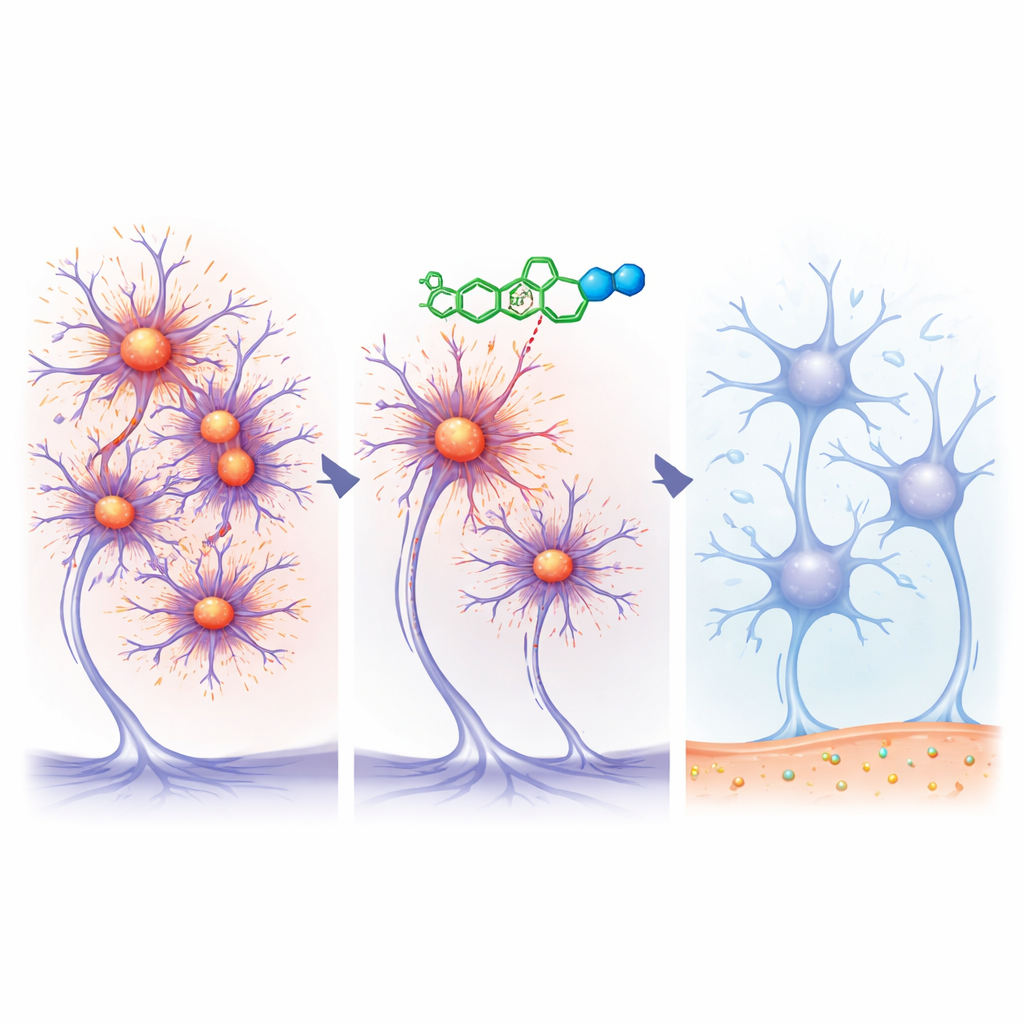
Per guardare oltre i sintomi, il gruppo di ricerca ha utilizzato una finestra insolita sulla malattia: piccoli prelievi cutanei. Le fibre nervose nella pelle delle persone con Parkinson possono anch’esse accumulare alfa‑sinucleina anomala, visibile con microscopia fluorescente. Circa il 40% dei partecipanti ha accettato campionamenti cutanei ripetuti, e 36 hanno fornito tessuto utilizzabile sia prima sia dopo il trattamento. Nel gruppo placebo, molte persone hanno mostrato livelli di depositi proteici invariati o in aumento in 12 settimane, sebbene alcune abbiano mostrato riduzioni spontanee. Tra coloro che assumevano risvodetinib, gli aumenti dei depositi sono stati meno comuni, e la proporzione di persone con depositi ridotti è aumentata con dosi maggiori, raggiungendo circa i due terzi nel gruppo a dose più alta. Tuttavia, i gruppi erano piccoli e le differenze non hanno raggiunto le soglie statistiche standard, dunque i risultati sono indicativi più che definitivi.
Cosa significa per il futuro delle terapie
Lo Studio 201 dimostra che bloccare c‑Abl con risvodetinib è fattibile in sicurezza per almeno tre mesi in persone con Parkinson in fase iniziale, a livelli farmacologici molto superiori a quelli usati per alcuni farmaci antitumorali che colpiscono la stessa via. I primi risultati dalle biopsie cutanee suggeriscono che il medicinale potrebbe influenzare il processo di base della malattia aiutando le cellule nervose a rimuovere l’accumulo di proteine dannose, ma sono necessari studi più ampi e più lunghi per confermare questo effetto e per capire se tali cambiamenti si traducano in un rallentamento della progressione dei sintomi. Per ora, lo studio non sostiene che il risvodetinib migliori la sensazione o il funzionamento delle persone: mostra soltanto che sembra sufficientemente sicuro da giustificare il passo successivo: studi più grandi e di durata maggiore per verificare se può davvero modificare il corso della malattia di Parkinson.
Citazione: Werner, M.H., McGarry, A., Meyer, C. et al. The 201 Trial: a placebo-controlled randomized phase 2 study of safety and tolerance of the c-Abl kinase inhibitor risvodetinib in untreated Parkinson’s disease. Nat Aging 6, 626–635 (2026). https://doi.org/10.1038/s43587-026-01084-4
Parole chiave: Malattia di Parkinson, neuroprotezione, studio clinico, aggregazione proteica, inibitore della tirosina chinasi