Clear Sky Science · it
Firma strutturale delle proteine plasmatiche classifica lo stato della malattia di Alzheimer
Perché un test del sangue per il declino della memoria è importante
La malattia di Alzheimer è spesso già ben avviata molto prima che i problemi di memoria diventino evidenti, ma i test attuali per individuarla precocemente possono essere invasivi, costosi o difficili da ottenere. Questo studio esplora un’idea diversa: se piccole modifiche nelle forme tridimensionali delle proteine circolanti nel sangue possano rivelare a che punto si trova una persona lungo il percorso dall’invecchiamento sano al lieve disturbo della memoria fino alla malattia di Alzheimer conclamata. Se efficace, un tale test del sangue potrebbe semplificare lo screening, supportare trattamenti più precoci e aiutare i ricercatori a monitorare chi beneficia di nuove terapie.
Osservare la forma delle proteine, non solo la quantità
La maggior parte degli esami del sangue misura quanto di una determinata molecola è presente. Qui, gli scienziati si sono invece concentrati sulla forma delle proteine. All’interno delle nostre cellule, un sistema di controllo qualità mantiene le proteine correttamente ripiegate; quando questo sistema viene meno con l’età, proteine mal ripiegate possono accumularsi e danneggiare le cellule cerebrali. Il team si è chiesto se questo cedimento nella “gestione delle proteine” lasci una firma strutturale nelle proteine del sangue. Da 520 volontari, cognitivamente sani, con lieve disturbo cognitivo (MCI) o con malattia di Alzheimer, hanno prelevato il sangue e usato una tecnica chimica chiamata profilazione covalente delle proteine per marcare le parti esposte delle proteine. Più un sito è esposto, più facilmente viene marcato, fornendo una lettura numerica della struttura proteica che è in gran parte indipendente da quanta proteina è presente.
Individuare impronte strutturali nel sangue
Su quasi 900 frammenti proteici marcati, i ricercatori hanno osservato una tendenza sottile ma coerente: man mano che le persone passavano dallo stato sano a MCI e poi ad Alzheimer, alcune superfici proteiche risultavano meno esposte e più variabili da individuo a individuo. Questo pattern è coerente con l’idea che il controllo del ripiegamento proteico peggiori con l’avanzare della malattia. Il team ha anche esaminato come un importante fattore di rischio genetico per l’Alzheimer, la variante APOE ε4, influenzasse la forma delle proteine. Hanno trovato che le persone con due copie di ε4 mostravano spostamenti strutturali distintivi in diverse proteine che interagiscono con la proteina APOE, suggerendo che questo gene a rischio altera non solo quali proteine sono presenti, ma anche come sono ripiegate e organizzate.
Collegare le proteine del sangue all’umore e al comportamento
L’Alzheimer interessa molto più della memoria; sintomi come agitazione, depressione e allucinazioni sono comuni e spesso differiscono tra uomini e donne. I ricercatori hanno combinato valutazioni cliniche di 12 tipi di sintomi neuropsichiatrici con le loro misure sulla forma delle proteine. In entrambi i sessi, sintomi peggiori tendevano a correlare con proteine che diventavano più strutturalmente “chiuse”. Alcune proteine, inclusa la clusterina e diverse altre legate all’accumulo di amiloide, seguivano la gravità dei sintomi in modo simile in uomini e donne, mentre altre mostravano schemi specifici per il sesso. Questi risultati suggeriscono che la struttura delle proteine del sangue potrebbe riflettere non solo la presenza della malattia, ma anche come essa si manifesta nel comportamento e nell’umore.
Un pannello di tre proteine per classificare lo stadio della malattia
Per trasformare queste misure complesse in qualcosa di clinicamente utile, il team ha inserito i dati strutturali in 18 diversi approcci di apprendimento automatico. Il modello con le migliori prestazioni, basato sul deep learning, si è appoggiato a soli tre frammenti proteici provenienti da C1QA, clusterina (nota anche come CLUS) e apolipoproteina B (ApoB). Usando solo le letture strutturali di questi tre frammenti, il modello ha classificato correttamente le persone come sane, MCI o affette da Alzheimer in circa l’83% dei casi in un set di test indipendente. Quando sono state poste domande binarie più semplici — per esempio distinguere sano da MCI, o MCI da Alzheimer — le prestazioni del pannello sono risultate ancora più forti, con misure di accuratezza comparabili o superiori a molte attuali metodiche basate sul sangue che si concentrano sulle quantità proteiche piuttosto che sulla struttura.
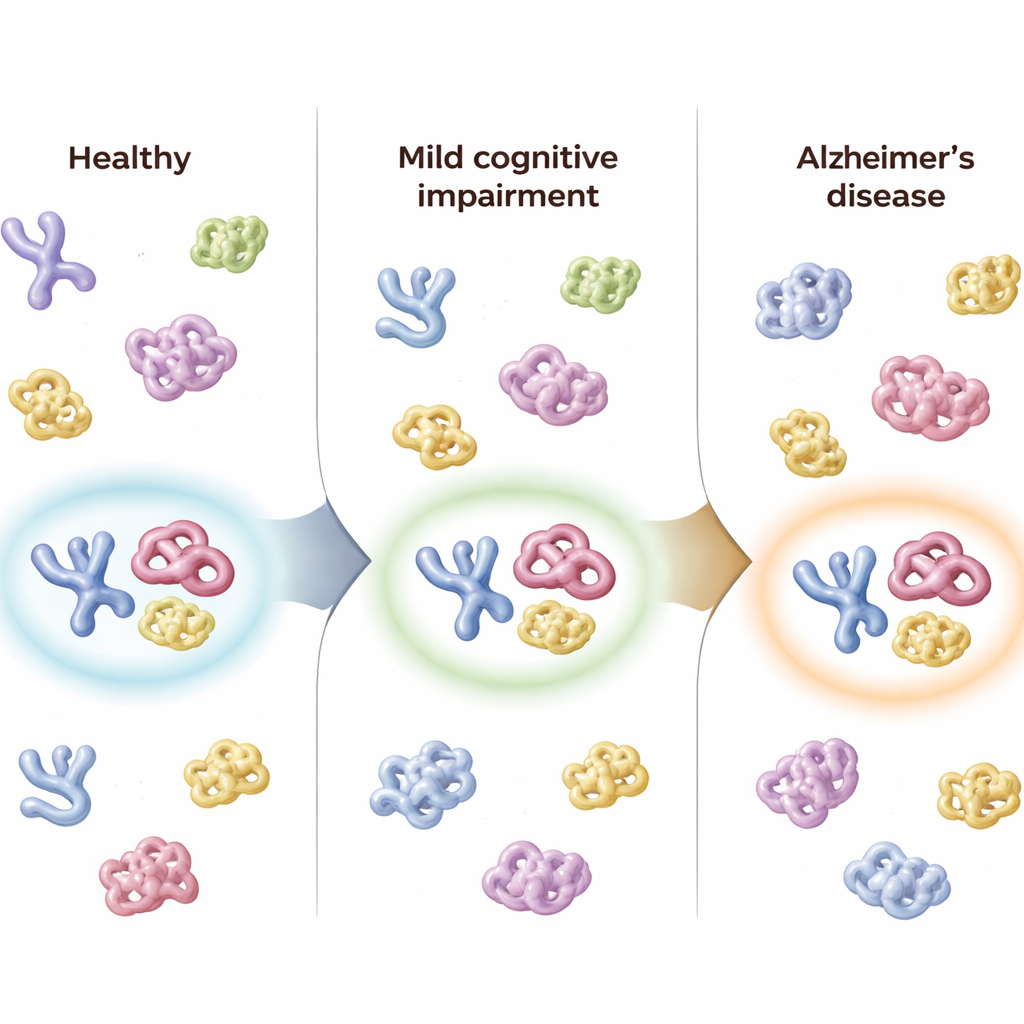
Seguire le persone nel tempo
I ricercatori disponevano anche di campioni di follow-up da 50 partecipanti prelevati fino a circa otto mesi dopo. Nelle persone la cui diagnosi è peggiorata — per esempio da sano a MCI, o da MCI ad Alzheimer — il punteggio combinato del pannello a tre proteine si è spostato nella stessa direzione, riflettendo la progressione della malattia. Al contrario, gli individui il cui stato clinico è rimasto invariato hanno mostrato poche variazioni nei punteggi del pannello. Il punteggio complessivo di “confidenza Alzheimer” del pannello ha seguito da vicino i test cognitivi standard, le misure di funzionamento quotidiano, il restringimento cerebrale visibile alle risonanze magnetiche e i marcatori consolidati nel liquido cerebrospinale relativi ad amiloide e tau, suggerendo che il segnale strutturale rilevato nel sangue rispecchia i cambiamenti sottostanti nel cervello.
Cosa potrebbe significare per i pazienti
Nel complesso, il lavoro mostra che piccoli cambiamenti coordinati nelle forme di poche proteine abbondanti nel sangue possono segnalare in modo affidabile se una persona è cognitivamente sana, leggermente compromessa o affetta dalla malattia di Alzheimer. Poiché il test utilizza il sangue anziché il liquido cerebrospinale o l’imaging cerebrale, potrebbe, in linea di principio, essere scalato per screening di routine o per selezionare e monitorare partecipanti in trial clinici. Gli autori avvertono che sono necessari studi più ampi e di più lunga durata e che la chimica coinvolta è ancora specializzata. Tuttavia, i loro risultati indicano la struttura delle proteine — non solo i livelli proteici — come una nuova e promettente fonte di informazioni per rilevare e monitorare la malattia di Alzheimer in modo più precoce e preciso.
Citazione: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
Parole chiave: Biomarcatori della malattia di Alzheimer, esame del sangue per la demenza, cambiamenti nel ripiegamento delle proteine, diagnosi con apprendimento automatico, clusterina e C1QA