Clear Sky Science · it
La resistenza ai chemioterapici a base di platino in tumori polmonari e ovarici è guidata da un secretoma senescente attaccabile tramite TGFβ
Quando il trattamento anticancro si ritorce contro
La chemioterapia a base di platino è uno dei pilastri della terapia oncologica moderna, in particolare per i tumori del polmone e dell’ovaio. È pensata per danneggiare il DNA tumorale così gravemente che le cellule cancerose non possano più dividersi. Eppure molti pazienti vedono i loro tumori ridursi all’inizio, per poi ricomparire in forma più aggressiva. Questo studio pone una domanda semplice ma inquietante: gli stessi farmaci che salvano vite possono anche aiutare le cellule tumorali sopravvissute a riprendersi? La risposta, secondo gli autori, risiede in un gruppo speciale di cellule danneggiate, simili a cellule invecchiate, e nei potenti messaggi chimici che esse rilasciano.
La doppia vita delle cellule tumorali «invecchiate»
La chemioterapia non colpisce tutte le cellule tumorali allo stesso modo. Alcune vengono eliminate, ma altre entrano in uno stato chiamato senescenza cellulare — fermo perenne nella divisione, ma metabolicamente attivo. Queste cellule senescenti aumentano di volume e cominciano a secernere un cocktail di proteine e segnali noto come fenotipo secretorio associato alla senescenza, o SASP. Utilizzando cellule tumorali umane di polmone e ovaio in coltura, e modelli murini, i ricercatori hanno mostrato che farmaci a base di platino come il cisplatino e il carboplatino inducono cellule senescenti particolarmente potenti. Quando cellule tumorali fresche sono state coltivate in mezzo prelevato da queste colture senescenti, sono cresciute più rapidamente, hanno migrato con maggiore facilità e hanno formato aggregati e sfere più grandi e aggressive rispetto alle cellule di controllo.
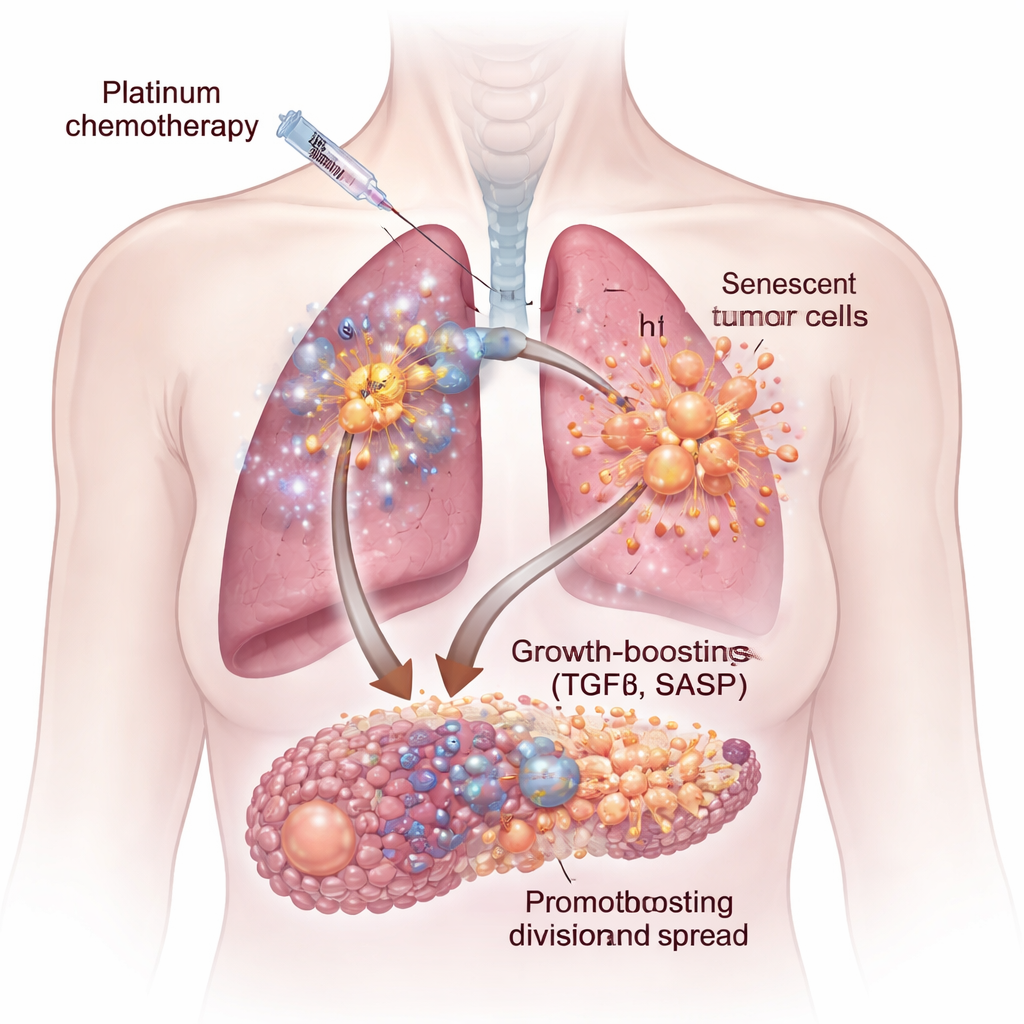
Un segnale di crescita nascosto: il TGFβ
Non tutte le chemioterapie scatenano le stesse secretioni dannose. Quando il gruppo ha confrontato i farmaci a base di platino con altri due agenti comuni, docetaxel e palbociclib, solo le cellule trattate con platino producevano una SASP che aumentava marcatamente la crescita tumorale. Combinando studi di espressione genica, misure proteiche e un microarray ad alto rendimento dell’ambiente microambientale, hanno identificato un colpevole chiave: la molecola di segnalazione transforming growth factor-beta, o TGFβ. Le cellule senescenti indotte dal cisplatino erano arricchite di multiple forme di TGFβ e di vie correlate. L’aggiunta di TGFβ purificato alle cellule tumorali ha riprodotto l’aumento di crescita osservato con il mezzo delle cellule senescenti, mettendo in luce questa famiglia di citochine come motore centrale del secretoma pro-tumorale.
Come il segnale rimodella le cellule tumorali
Lo studio ha quindi tracciato come questi segnali ricchi di TGFβ modificano il comportamento delle cellule tumorali vicine. Sulla superficie delle cellule riceventi, il TGFβ si lega a un recettore chiamato TGFBR1. Questo a sua volta attiva una catena interna di proteine — in particolare le vie AKT e mTOR — note per controllare crescita cellulare, metabolismo e sopravvivenza. Sia nelle cellule tumorali polmonari umane che in quelle murine, l’esposizione alle secretioni derivate dal cisplatino aumentava rapidamente le forme attivate (fosforilate) di AKT e del suo bersaglio a valle p70S6K, e incrementava l’espressione di geni del ciclo cellulare. Bloccare TGFBR1 con un farmaco chiamato galunisertib, o inibire direttamente mTOR, ha sostanzialmente spento questo picco di segnalazione e ridotto la proliferazione extra, la formazione di colonie e la crescita invasiva delle sfere indotte dal secretoma senescente.
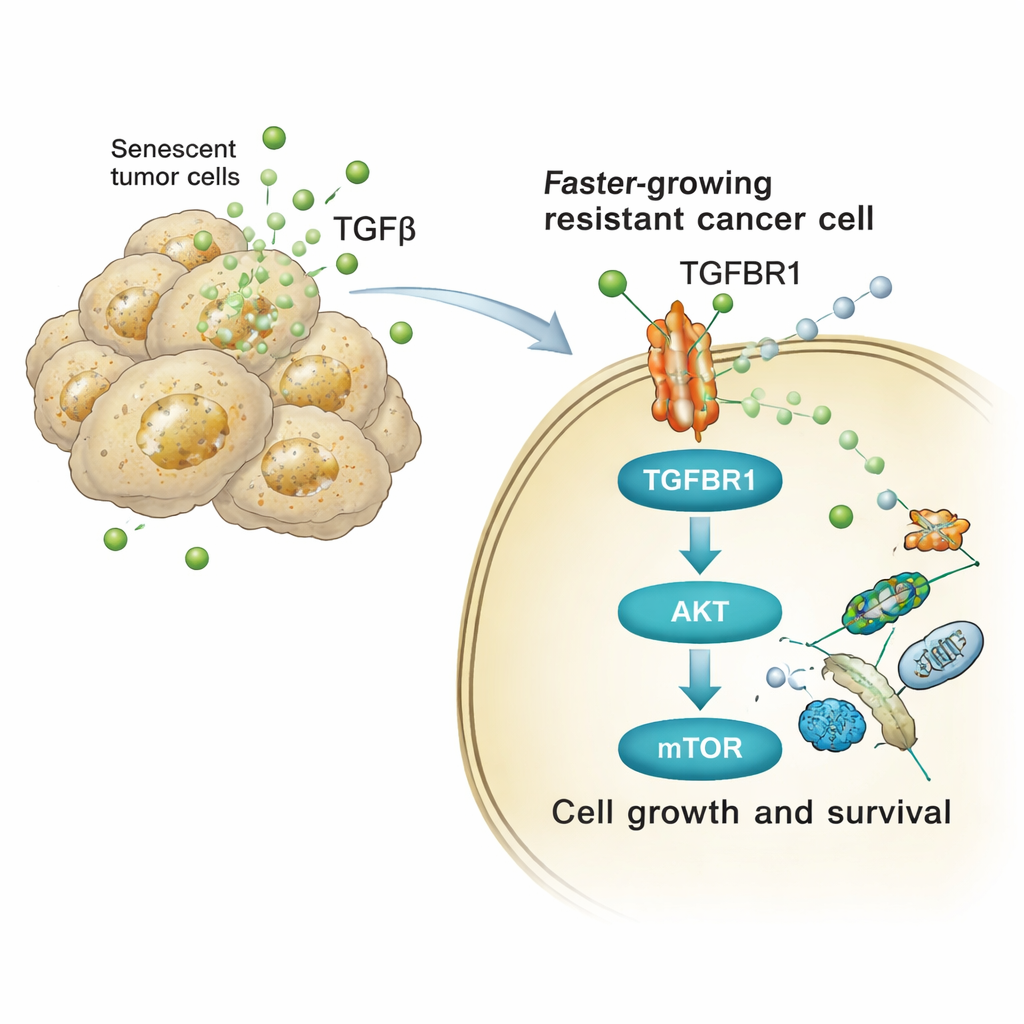
Dal topo al paziente: una vulnerabilità comune
Questi meccanismi non erano confinati alle provette. In topi portatori di tumori polmonari, la mescolanza di cellule senescenti e non senescenti ha portato a tumori a crescita più rapida e a una sopravvivenza più breve, mentre l’eliminazione delle cellule senescenti o il blocco di TGFBR1 hanno attenuato questo effetto. Quando ai topi con tumori polmonari ingegnerizzati geneticamente è stato somministrato il cisplatino standard, i tumori hanno accumulato marcatori di senescenza insieme a elevata attività AKT/mTOR nelle cellule vicine che ancora si dividevano. Combinare il cisplatino con l’inibizione di TGFBR1 o con farmaci senolitici (che eliminano selettivamente le cellule senescenti) ha ridotto il carico tumorale e prolungato la sopravvivenza rispetto alla sola chemioterapia. In modo cruciale, le analisi di campioni umani di cancro del polmone e di carcinoma sieroso ovarico di alto grado prelevati dopo terapia a base di platino hanno rivelato schemi simili: aumento dei marcatori di senescenza e potenziamento della segnalazione AKT/mTOR nel microambiente tumorale, specialmente nelle regioni ricche di cellule senescenti.
Trasformare una passività in un vantaggio
Per il lettore non specialista, il messaggio è che la chemioterapia a base di platino può lasciare dietro di sé una popolazione di cellule “zombie” danneggiate ma pericolose. Queste cellule tumorali senescenti non si dividono più, ma rilasciano segnali ricchi di TGFβ che risvegliano le cellule cancerose vicine, favorendo la ricrescita tumorale e la resistenza ai trattamenti successivi. La buona notizia è che questa debolezza è attaccabile. In modelli preclinici di cancro del polmone e dell’ovaio, l’aggiunta di farmaci che bloccano il recettore TGFBR1 o che eliminano selettivamente le cellule senescenti ha reso la chemioterapia a base di platino più efficace e ha migliorato la sopravvivenza senza evidenti tossicità aggiuntive. Il lavoro indica la strada a futuri trial clinici che combinino il trattamento standard a base di platino con strategie senolitiche o anti‑TGFβ, con l’obiettivo di preservare i benefici della chemioterapia disinnescando i suoi effetti collaterali nascosti guidati dalla senescenza.
Citazione: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
Parole chiave: resistenza alla chemioterapia, senescenza cellulare, segnalazione TGFβ, cancro del polmone, cancro ovarico