Clear Sky Science · it
Il danno al DNA nei macrofagi guida l’autoreattività immunitaria tramite la presentazione di antigeni nucleari
Quando l’usura cellulare fa sì che il sistema immunitario si rivolga contro di noi
L’invecchiamento comporta un rischio maggiore di malattie autoimmuni, in cui il sistema immunitario comincia ad attaccare il corpo che dovrebbe proteggere. Questo studio esplora un colpevole sorprendente: il danno quotidiano al DNA all’interno di cellule immunitarie chiamate macrofagi. Tracciando come questo danno cambi ciò che i macrofagi mostrano ad altre cellule immunitarie, i ricercatori mettono in luce un possibile anello mancante tra l’invecchiamento e lo sviluppo di patologie come il lupus.
I guardiani del corpo che escono dal copione
I macrofagi sono difensori in prima linea che inghiottono microbi e detriti e poi espongono frammenti proteici alle cellule T, aiutando il sistema immunitario a decidere cosa attaccare. Il gruppo ha ingegnerizzato topi i cui macrofagi erano difettosi in una proteina chiave per la riparazione del DNA, ERCC1-XPF, in modo che queste cellule accumulassero danni persistenti al DNA. Con l’età, questi topi hanno sviluppato segni distintivi di autoimmunità: focolai infiammatori nei reni, depositi di complessi immuni e proteine del complemento, milza ingrossata e alti livelli di anticorpi antinucleo simili a quelli osservati in animali naturalmente anziani. Un profilo immunitario dettagliato ha mostrato un’espansione di plasmacellule, cellule T attivate e cellule natural killer, tutti segnali di un sistema immunitario cronicamente stimolato.
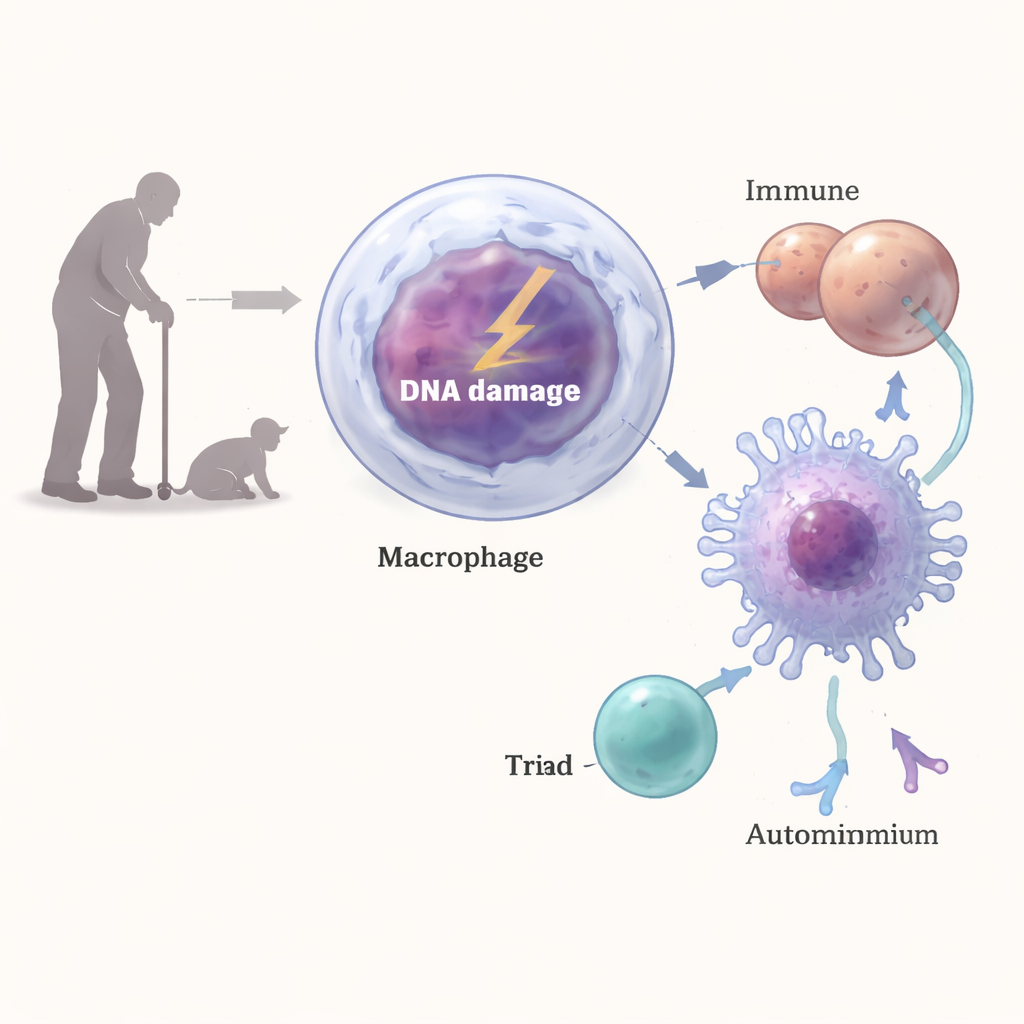
Dal DNA rotto alle cellule T che prendono di mira il sé
In che modo il danno al DNA nei macrofagi poteva innescare una risposta così forte simile all’autoimmunità? I ricercatori hanno scoperto che le rotture del DNA attivavano una classica via di risposta al danno in queste cellule, coinvolgendo enzimi come ATM, ATR e DNA‑PK. Questa segnalazione aumentava i livelli di MHC di classe II sulla superficie, le vetrine molecolari usate per presentare frammenti proteici alle cellule T CD4. Quando macrofagi con danno al DNA venivano mescolati con cellule T, inducevano un’attivazione più intensa delle cellule T e una maggiore produzione di interferone‑gamma rispetto ai macrofagi normali. Bloccare MHC‑II o interferire con la risposta al danno del DNA invertiva gran parte di questo effetto, e negli animali viventi anticorpi che bloccavano MHC‑II o deplezionavano le cellule T CD4 riducevano l’infiammazione renale e i livelli di autoanticorpi.
Proteine del sé provenienti dal nucleo messe in vetrina
Per vedere esattamente cosa i macrofagi danneggiati mostravano alle cellule T, il team ha isolato i peptidi legati a MHC‑II e li ha analizzati tramite spettrometria di massa. Rispetto a cellule normali o stimolate con lipopolisaccaride, i macrofagi con DNA danneggiato presentavano un repertorio di peptidi sorprendentemente diverso. Invece di provenire principalmente da proteine di membrana ed extracellulari, le loro molecole di MHC‑II risultavano arricchite per frammenti derivati da proteine nucleari e ribosomiali, comprese le istoni e altri componenti strettamente associati al DNA. Quando alcuni di questi peptidi nucleari sono stati sintetizzati e usati per ristimolare cellule immunitarie provenienti dai topi ingegnerizzati, hanno scatenato forti risposte delle cellule T, suggerendo che questi frammenti di origine endogena fossero effettivamente immunogenici.
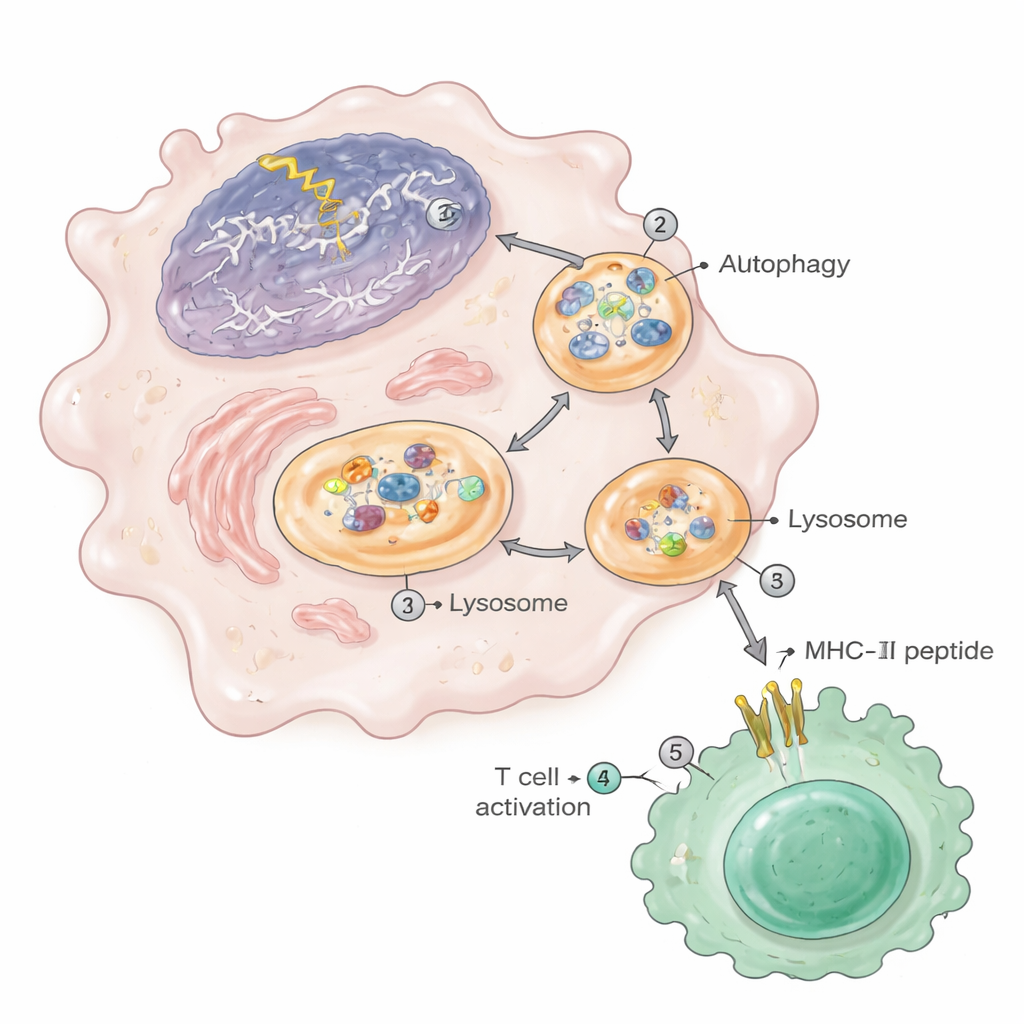
Autofagia: la via di pulizia che alimenta l’autoimmunità
Il percorso del materiale nucleare verso la vetrina MHC‑II dipendeva fortemente dall’autofagia, il sistema interno di riciclo della cellula. In presenza di danno al DNA, l’autofagia aumentava e convogliava frammenti di cromatina — provenienti dal nucleo cellulare — negli autofagosomi che poi si fondevano con i lisosomi, dove le proteine vengono spezzate in peptidi. Questi lisosomi nei macrofagi danneggiati contenevano livelli elevati di proteine nucleari e ribosomiali. Quando i ricercatori bloccarono l’autofagia con farmaci o rimossero geneticamente un gene essenziale per l’autofagia (Atg5) nelle stesse cellule mieloidi, gli animali mostrarono meno lesioni renali, meno cellule T attivate e plasmacellule, e una drastica riduzione dei peptidi nucleari che comparivano su MHC‑II. Frammenti di cromatina simili e un’aumentata presentazione di antigeni furono osservati anche nei macrofagi di topi suscettibili al lupus, in linee cellulari di monociti umani esposte a farmaci che danneggiano il DNA e nei macrofagi di topi molto anziani.
Perché questo conta per l’invecchiamento e le malattie autoimmuni
Nel complesso, i risultati suggeriscono un’idea semplice ma potente: con l’avanzare dell’età, il danno al DNA si accumula nei macrofagi, che a loro volta utilizzano l’autofagia per rimuovere i detriti nucleari. Facendo ciò, tagliano involontariamente il materiale nucleare in peptidi che vengono caricati su MHC‑II e mostrati alle cellule T come se fossero estranei. Col tempo, questa esposizione cronica ad antigeni nucleari del sé può istruire il sistema immunitario a reagire contro il proprio corpo, promuovendo l’autoimmunità. Identificando questa via — dal danno al DNA all’autofagia fino alla presentazione di antigeni nucleari — lo studio mette in luce nuove strategie per attenuare l’autoimmunità correlata all’età, come migliorare la riparazione del DNA, modulare finemente l’autofagia o bloccare selettivamente la presentazione di peptidi nucleari del sé senza spegnere le difese vitali del sistema immunitario.
Citazione: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
Parole chiave: invecchiamento e autoimmunità, danno al DNA, macrofagi, autofagia, anticorpi antinucleo