Clear Sky Science · it
I senotossine prendono di mira la senescenza tramite specificità di legame lipidico, squilibrio ionico e rimodellamento del lipidoma
Perché eliminare le cellule “zombie” potrebbe rendere più efficace il trattamento del cancro
Con l’avanzare dell’età — o a seguito di trattamenti aggressivi come la chemioterapia — alcune cellule smettono di dividersi ma rifiutano di morire. Queste cellule “zombie”, note come cellule senescenti, possono secernere molecole infiammatorie che danneggiano i tessuti e possono favorire la ricomparsa dei tumori. Questo studio esplora un modo sorprendente per eliminare selettivamente queste cellule problematiche usando una proteina derivata da un veleno, con il potenziale di rendere i trattamenti oncologici sia più efficaci che più sicuri.
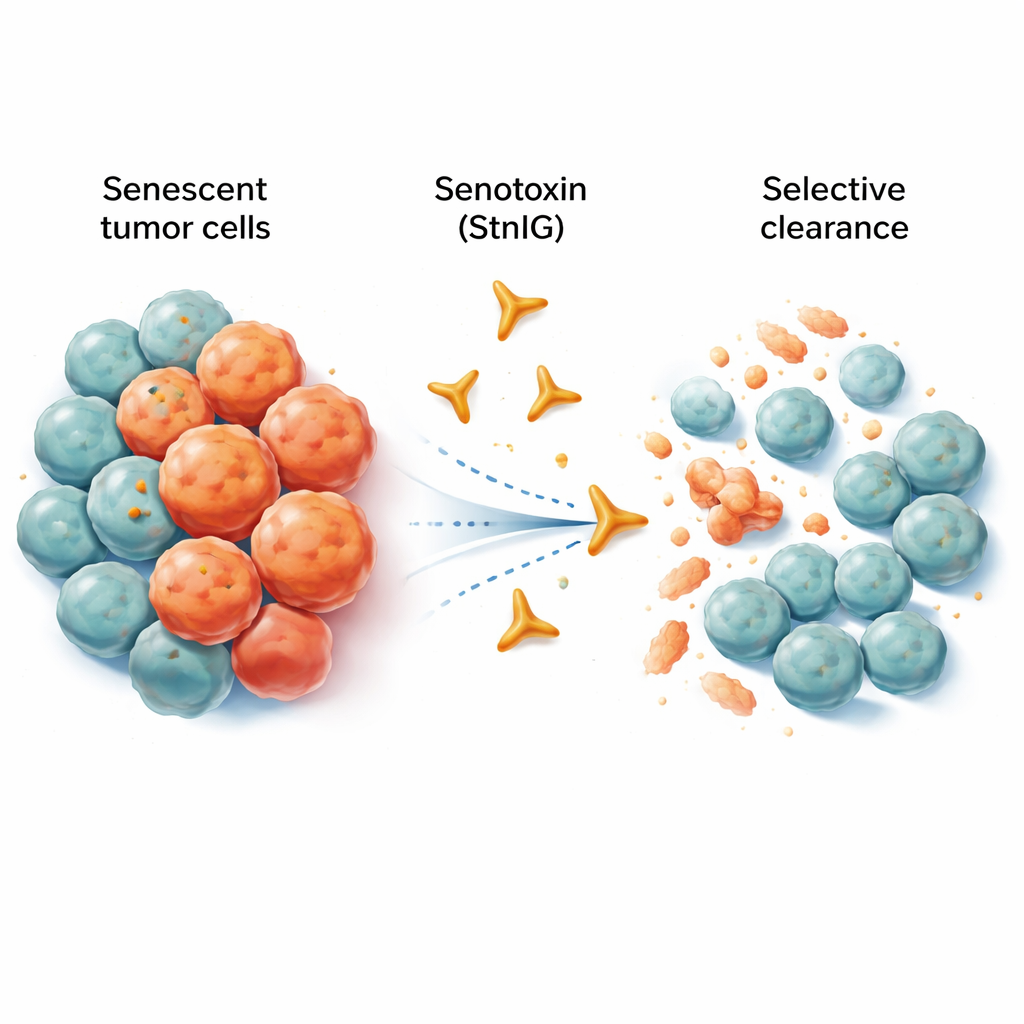
Cellule invecchiate che non mollano
Le cellule senescenti sono come lavoratori in pensione che continuano a occupare la scrivania e a disturbare l’ufficio. Non si moltiplicano più, ma rilasciano un mix di segnali infiammatori che possono indebolire i tessuti circostanti, promuovere l’invecchiamento e persino sostenere la crescita e la diffusione dei tumori. La chemioterapia, pur eliminando molte cellule tumorali, lascia spesso dietro di sé una scia di cellule senescenti all’interno e intorno al tumore. Queste cellule residue possono alimentare infiammazione cronica, effetti collaterali e, infine, recidive. I farmaci sperimentali esistenti chiamati senolitici mirano a rimuovere le cellule senescenti, ma molti di essi colpiscono anche cellule sane, funzionano solo in finestre di dosaggio molto ristrette o sono difficili da assorbire per l’organismo.
Trasformare il veleno di anemone di mare in uno strumento di precisione
I ricercatori si sono rivolti agli specialisti naturali della morte cellulare: i veleni animali. Si sono concentrati su una proteina che forma pori chiamata sticholysina I (StnI), presente in un’anemone di mare caraibica. Questa proteina può praticare piccolissimi fori nelle membrane cellulari. Il gruppo ha scoperto che StnI, e una versione raffinata da loro ingegnerizzata chiamata StnIG, sono sorprendentemente più efficaci nell’uccidere le cellule tumorali senescenti rispetto ai loro vicini non senescenti. In diversi tipi di cellule tumorali umane (melanoma, fegato, polmone e tumori derivati dal tessuto nervoso) indotte alla senescenza da farmaci chemioterapici, StnI e soprattutto StnIG hanno eliminato le cellule invecchiate a dosi molto inferiori rispetto a quelle necessarie per colpire le cellule in proliferazione. StnIG è risultato più selettivo di un senolitico sperimentale di riferimento, navitoclax, suggerendo che tossine opportunamente tarate possono superare gli approcci attuali.
Come le membrane alterate diventano un tallone d’Achille
Le cellule senescenti non cambiano solo all’interno; anche la loro membrana esterna — la pelle lipidica che circonda ogni cellula — viene rimodellata. Nelle cellule sane, alcuni lipidi si trovano principalmente sul lato interno della membrana, nascosti dall’ambiente esterno. Nelle cellule senescenti questo equilibrio si rompe e questi lipidi diventano esposti. Attraverso analisi chimiche dettagliate e simulazioni al computer, il gruppo ha dimostrato che StnIG riconosce e si ancora a questo paesaggio lipidico alterato. La sua struttura è particolarmente adatta ad aggrapparsi a lipidi specifici che le cellule senescenti espongono in superficie. Una volta agganciato, StnIG forma pori che permettono agli atomi carichi, o ioni, di fluire dentro e fuori in modo fortemente squilibrato.
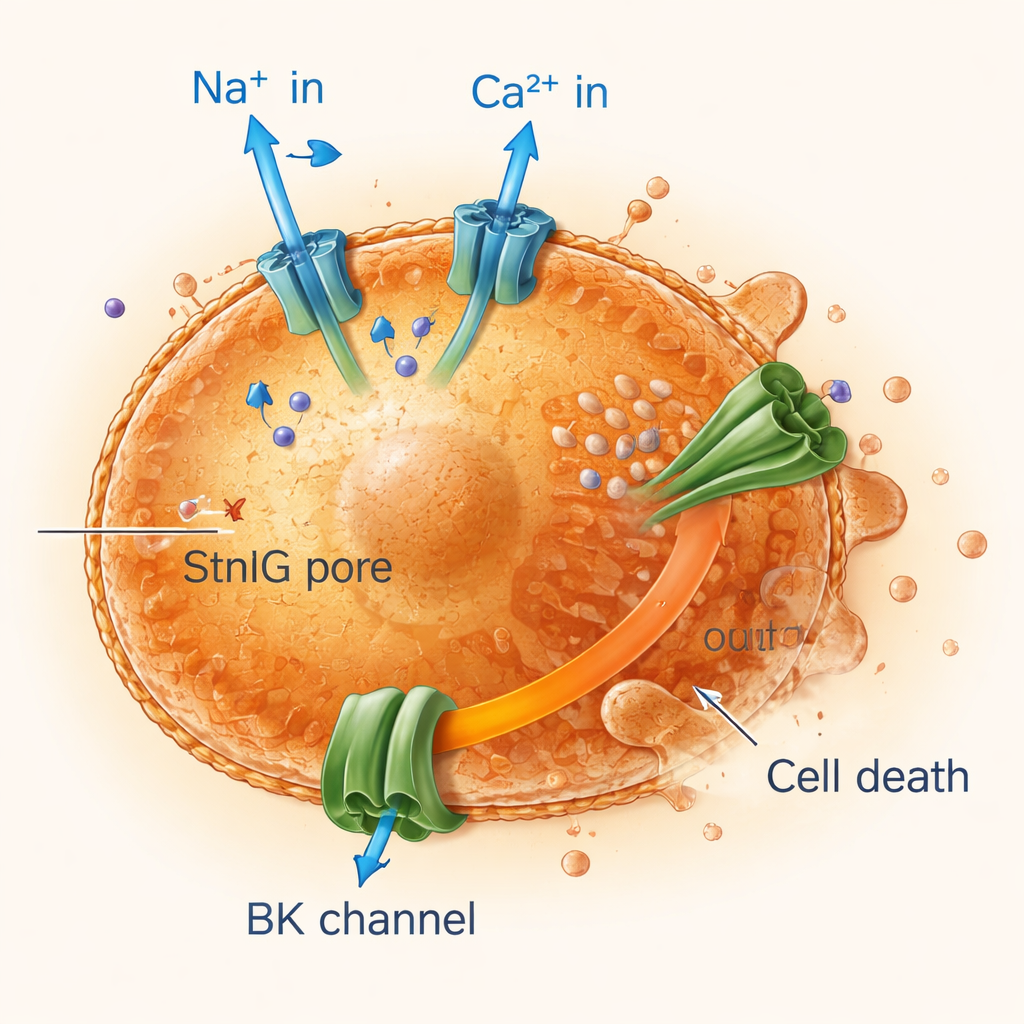
Intercettare le cellule invecchiate con uno squilibrio ionico
Tracciando corrente elettrica e movimento ionico attraverso le membrane cellulari, i ricercatori hanno scoperto che i pori di StnIG consentono al sodio e al calcio di entrare rapidamente nelle cellule senescenti mentre il potassio fuoriesce continuamente. L’ondata di calcio attiva grandi canali del potassio, amplificando la perdita di potassio, che è cruciale per mantenere il volume cellulare e la sopravvivenza. Le cellule senescenti, già meno flessibili e più fragili rispetto a quelle sane, non riescono a gestire questo persistente disturbo ionico. I loro mitocondri — le centrali energetiche della cellula — perdono il potenziale elettrico, la produzione di energia crolla e le cellule vanno incontro a forme programmate di morte, inclusa l’apoptosi e una morte infiammatoria detta piroptosi. Il blocco dell’ingresso di calcio o dei canali del potassio ha protetto le cellule senescenti, confermando che questo squilibrio ionico è centrale per l’azione della tossina.
Da piastrette cellulari ad organismi viventi
Il gruppo ha poi verificato se questa strategia funzionasse in organismi viventi. in embrioni di zebrafish contenenti cellule umane di melanoma senescenti, basse dosi di StnIG hanno ridotto il numero di queste cellule con efficacia paragonabile al navitoclax, senza tossicità evidente. In modelli murini di melanoma e cancro al fegato, la chemioterapia con un farmaco che blocca il ciclo cellulare (palbociclib) ha rallentato la crescita tumorale inducendo molte cellule tumorali alla senescenza. Quando i ricercatori hanno aggiunto StnIG in modo intermittente, i tumori si sono rimpiccioliti o sono andati in remissione più efficacemente rispetto alla sola chemioterapia, e in modo comparabile alla combinazione chemioterapia–navitoclax. È importante che i topi trattati con StnIG abbiano mostrato effetti collaterali limitati e nessun danno evidente nei principali organi, sebbene il potassio ematico sia aumentato negli animali con tumori senescenti — probabilmente riflettendo il massiccio rilascio di potassio durante la distruzione delle cellule tumorali.
Cosa significa per la cura del cancro in futuro
Questo lavoro introduce le “senotossine”: proteine ingegnerizzate ispirate ai veleni che sfruttano le particolarità della membrana e della gestione ionica delle cellule senescenti. Concentrandosi sui lipidi alterati e forzando letali squilibri ionici, StnIG può eliminare selettivamente le cellule senescenti dannose risparmiando la maggior parte dei tessuti sani. Usate insieme alla chemioterapia, queste senotossine potrebbero un giorno contribuire a ripulire le cellule zombie che alimentano le recidive e l’infiammazione cronica, rendendo i trattamenti oncologici più duraturi e potenzialmente attenuando alcuni effetti collaterali a lungo termine.
Citazione: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
Parole chiave: senescenza cellulare, senolitici, terapia oncologica, farmaci derivati da veleni, canali ionici