Clear Sky Science · it
La modifica di basi in PIK3CD adattata ai CAR aumenta la potenza anti-tumorale delle cellule T
Riprogammare le cellule che combattono il cancro
La terapia con cellule T dotate di recettore chimerico per l’antigene (CAR) ha trasformato il trattamento di alcuni tumori del sangue, ma molti pazienti ancora recidivano o non rispondono. Un problema chiave è che queste cellule immunitarie ingegnerizzate possono esaurirsi o non persistere nell’organismo a sufficienza. Questo studio pone una domanda semplice ma potente: invece di ridisegnare completamente i CAR, che cosa succederebbe se potessimo «riaccordare» sottilmente il cablaggio interno delle cellule T in modo che restino potenti più a lungo, e farlo in sicurezza?
Mirare alla manopola del volume delle cellule T
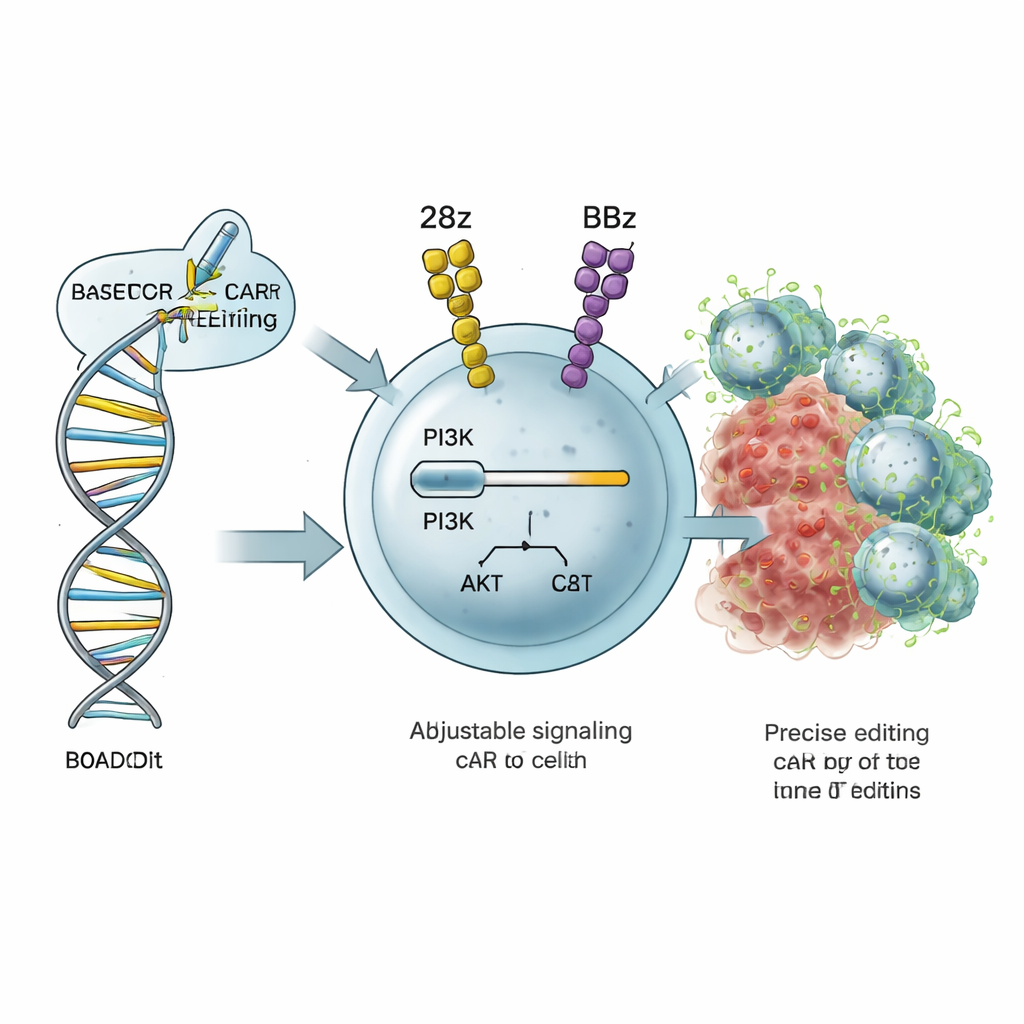
Le cellule T che uccidono il cancro si affidano a circuiti di segnalazione interni che indicano loro quanto attivarsi, quanto rapidamente proliferare e se diventare combattenti a vita breve o cellule della memoria a lunga durata. Un circuito importante è la via PI3K–AKT, nella quale una proteina chiamata PI3Kδ—codificata dal gene PIK3CD—funziona come una manopola del volume per attivazione e metabolismo. Gli autori hanno sviluppato una strategia chiamata ROADSTAR, che utilizza il base editing, una forma altamente precisa di ingegneria genomica CRISPR, per cambiare singole “lettere” nel PIK3CD. Invece di accendere o spegnere completamente la via, ROADSTAR cerca piccole mutazioni che aumentino o diminuiscano delicatamente la segnalazione in modo che corrisponda al meglio al design specifico del CAR all’interno della cellula T.
Scoprire mutazioni utili
Il gruppo ha costruito una libreria di 34 diverse modifiche di una singola lettera nella regione regolatoria di PIK3CD e le ha introdotte in cellule T umane già portatrici di uno dei due design CAR comuni: 28z (basato sulla molecola CD28) e BBz (basato su 4‑1BB). Questi CAR differiscono nel modo in cui stimolano le cellule T: 28z tende a promuovere un attacco rapido e vigoroso ma anche l’esaurimento, mentre BBz favorisce migliore sopravvivenza e memoria ma può essere meno aggressivo. Le cellule CAR T editate sono state sottoposte a una «prova di stress» esponendole ripetutamente a cellule leucemiche. Con il deep sequencing, i ricercatori hanno tracciato quali mutazioni permettevano alle CAR T editate di sopravanzare i pari non editati nel corso di diverse settimane.
Due mutazioni sono emerse con chiarezza. Nelle CAR T BBz, una modifica chiamata E81K ha leggermente aumentato l’attività di PI3Kδ, incrementando i segnali lungo la via PI3K–AKT. Nelle CAR T 28z, una diversa modifica, L32P, ha attenuato l’attività di PI3Kδ. Il modellamento strutturale ha suggerito che entrambe le modifiche alterano sottilmente l’interazione di PI3Kδ con il suo partner regolatorio, modulando la forza della segnalazione invece di azionarla completamente on o off. È importante che la mutazione benefica per un design CAR non fosse la stessa per l’altro, sottolineando che ogni architettura CAR richiede il proprio accordo interno ottimale.
Cellule CAR T più forti, più in forma e più durature
Quando le modifiche promettenti sono state testate singolarmente, E81K ha reso le CAR T BBz più attivate al contatto con le cellule tumorali, migliori nella proliferazione e notevolmente più efficaci nel distruggere bersagli tumorali, inclusi quelli con bassi livelli di antigene. Queste cellule si sono sviluppate in cellule T della memoria effettrice che combinavano una potente capacità citotossica con la capacità di persistere. In modelli murini di leucemia e di neuroblastoma metastatico, le CAR T BBz editate con E81K hanno controllato i tumori in modo più completo e per periodi molto più lunghi rispetto alle cellule BBz non editate, sconfiggendo anche più round di reintroduzione tumorale. Profilature dettagliate a singola cellula di RNA e del metabolismo hanno mostrato che le cellule E81K avevano funzione mitocondriale migliorata, maggiore riserva respiratoria e capacità glicolitica e meno segni di esaurimento—essenzialmente, erano più energetiche e resilienti.
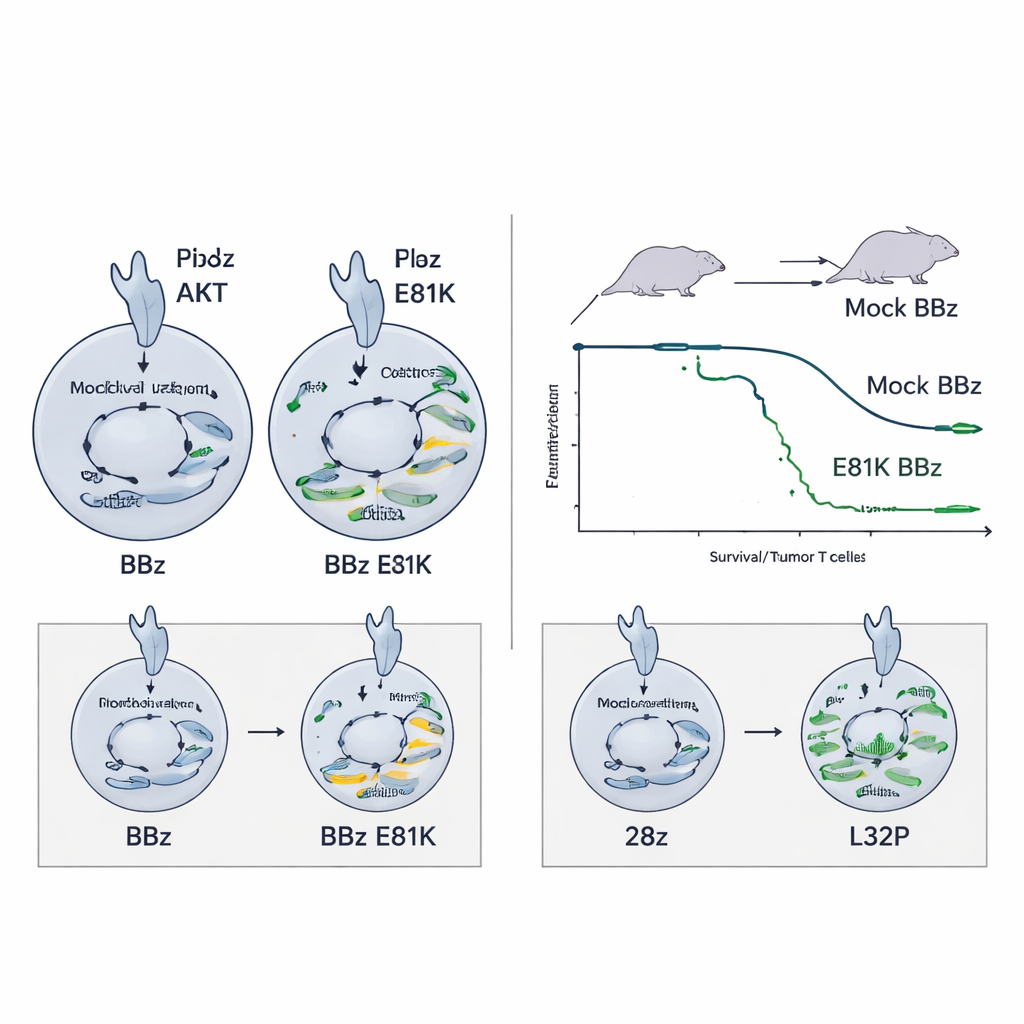
Prevenire il burnout nelle CAR altamente attive
Lo stesso incremento dovuto a E81K non ha aiutato—e poteva perfino danneggiare—le CAR T 28z, che già segnalano con forza. In questo contesto, l’aumentata attività di PI3K ha aumentato i marker di esaurimento senza migliorare le funzioni. Qui la mutazione L32P si è dimostrata più adatta: riducendo moderatamente la segnalazione PI3K–AKT, le CAR T 28z editate con L32P hanno mostrato una minore attivazione basale ma hanno preservato un’elevata capacità citotossica e hanno proliferato di più nel tempo. Hanno inoltre mantenuto uno stato meno differenziato, simile alla memoria, inclusa una riserva di cellule con caratteristiche di cellule staminali della memoria ritenuta in grado di sostenere risposte a lungo termine. In un modello impegnativo di neuroblastoma, le CAR T 28z modificate con L32P hanno migliorato la sopravvivenza rispetto alle controparti non editate.
Sicurezza e prospettive future
Una preoccupazione centrale nell’alterare in modo permanente la segnalazione immunitaria è il rischio di crescita incontrollata o tumori secondari. Gli autori hanno quindi eseguito controlli di sicurezza estesi. Le CAR T BBz editate con E81K non hanno mostrato crescita anomala in coltura, non hanno provocato danni d’organo o crisi infiammatorie nei topi e non hanno evidenziato segni di linfoma o invasione tissutale mesi dopo l’infusione. I database clinici mostrano inoltre nessun arricchimento di queste specifiche mutazioni di PIK3CD nelle leucemie delle cellule T. Nel complesso, il lavoro dimostra che modifiche genomiche di una singola lettera scelte con cura possono agire come manopole di precisione per il comportamento delle cellule T—aumentando potenza anti-tumorale e persistenza rispettando la biologia unica di ciascun CAR. Questo approccio ROADSTAR potrebbe contribuire a realizzare la prossima generazione di terapie CAR T più efficaci e più affidabili contro i tumori del sangue e, potenzialmente, contro i tumori solidi.
Citazione: Bucher, P., Brückner, N., Kortendieck, J. et al. CAR-adapted PIK3CD base editing enhances T cell anti-tumor potency. Nat Cancer 7, 368–383 (2026). https://doi.org/10.1038/s43018-025-01099-7
Parole chiave: Cellule CAR T, Segnalazione PI3K, Base editing, Immunoterapia oncologica, Metabolismo delle cellule T