Clear Sky Science · it
Glioma midline diffusa H3.3K27M-alterata de novo in organoidi del tronco encefalico umano per analizzare la funzione delle cellule CAR T anti‑GD2
Perché questo studio sul cancro cerebrale infantile è importante
Il glioma midline diffuso è uno dei tumori cerebrali infantili più letali, colpendo bambini molto piccoli nel tronco encefalico e lasciando le famiglie con quasi nessuna opzione terapeutica efficace. Poiché i tumori si trovano in profondità nel cervello e vengono raramente asportati chirurgicamente, i ricercatori dispongono di pochi tessuti da analizzare e di scarse possibilità di testare nuove terapie in modo sicuro. Questo studio costruisce un “mini‑tronco encefalico in provetta” realistico e lo utilizza per osservare come si comporta, nel corso di settimane, una promettente immunoterapia—le cellule CAR T anti‑GD2—compresi i motivi per cui talvolta fallisce.
Costruire un mini‑tronco encefalico in laboratorio
Il gruppo ha iniziato da cellule staminali umane e le ha guidate, passo dopo passo, a svilupparsi in organoidi cerebrali tridimensionali che assomigliano alla regione del tronco encefalico chiamata ponte, dove questi tumori insorgono di solito. Regolando con cura i segnali di crescita nel tempo, hanno ottenuto organoidi ricchi degli stessi tipi di cellule di supporto, o glia, che normalmente abitano quest’area. Analisi genetiche dettagliate hanno mostrato che i tipi cellulari e la loro maturazione seguivano schemi osservati nello sviluppo cerebrale umano precoce, in particolare le linee gliali tipiche del ponte e della vicina midollare. Questo significa che gli organoidi possono fungere da sfondo realistico per studiare come questo cancro inizi e progredisca.
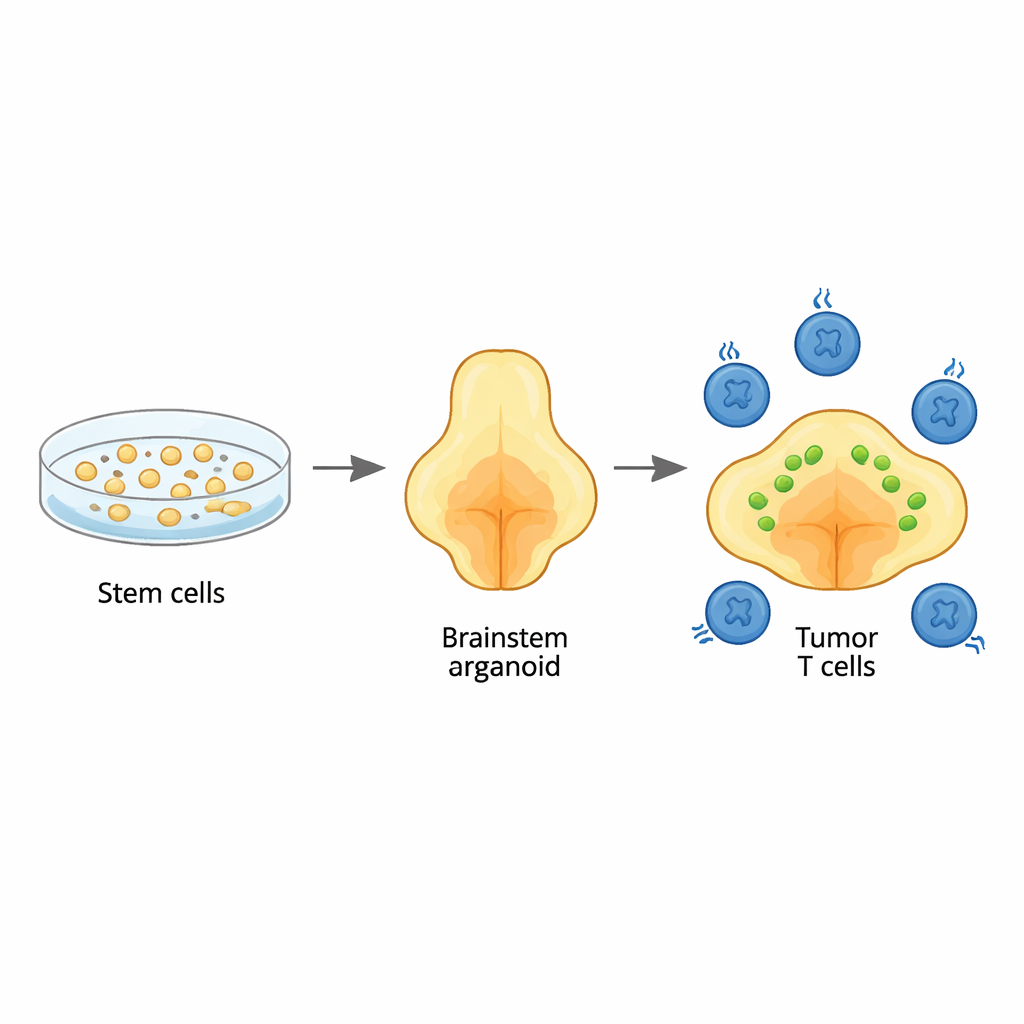
Ricreare il tumore del bambino all’interno dell’organoide
Per mimare il glioma midline diffuso, i ricercatori hanno inserito tre alterazioni genetiche chiave in organoidi giovani: una mutazione caratteristica in una proteina istonica (H3.3K27M), la perdita del soppressore tumorale TP53 e una variazione attivante nel recettore di crescita PDGFRA. Quando introdotte in una fase di sviluppo molto precoce, queste alterazioni hanno trasformato cellule gliali selezionate in cellule cancerose. I tumori risultanti si sono diffusi in modo diffuso attraverso gli organoidi, come avviene nei tronchi encefalici pediatrici, e presentavano gli stessi ampi profili di DNA e RNA osservati nei tumori dei pazienti. Il sequenziamento a singola cellula ha rivelato un mix di stati tumorali, inclusi cellule immature gliali specifiche del ponte che corrispondono a quelle trovate nei tumori pediatrici reali, sottolineando che il modello ricapitula fedelmente la malattia umana.
Osservare le immunoterapie che combattono—e si esauriscono—col tempo
Con questo modello di tumore nel tronco encefalico, il gruppo ha aggiunto cellule CAR T anti‑GD2—linfociti T dei pazienti ingegnerizzati per riconoscere una molecola chiamata GD2 sulle cellule tumorali—and ha monitorato sia le dimensioni del tumore sia il comportamento delle T per fino a un mese. Alcuni organoidi hanno mostrato un forte restringimento tumorale, altri solo un controllo parziale, rispecchiando gli esiti misti osservati negli studi clinici. Il sequenziamento dell’RNA a singola cellula di oltre 20.000 cellule CAR T esposte ai tumori ha messo in luce una sorprendente diversità di stati delle T. Alcune cellule erano altamente citotossiche “esecutrici”, altre erano attivate ma non pienamente letali, e un gruppo distinto mostrava caratteristiche di esaurimento, con geni antitumorali attenuati e alta espressione di inibitori «di freno». Le cellule esauste somigliavano molto a linfociti T logorati osservati in infezioni croniche e tumori umani, indicando che il sistema di organoidi cattura la fatica delle T clinicamente rilevante indotta dal contatto prolungato con il cancro.
Trovare T potenti ma di breve durata
Approfondendo, i ricercatori hanno identificato un sottogruppo di cellule CAR T contrassegnate da una proteina di superficie chiamata NCAM1 che erano particolarmente efficaci come killer nel breve termine. Quando queste cellule NCAM1‑positive sono state isolate e utilizzate da sole, controllavano i tumori inizialmente meglio delle controparti NCAM1‑negative. Tuttavia, si esaurivano e diminuivano più rapidamente, portando a un controllo più debole nel tempo. Questo compromesso tra potenza immediata e persistenza aiuta a spiegare perché le terapie CAR T possono produrre risposte drammatiche ma temporanee e suggerisce che pre‑selezionare o rimodellare sottotipi di T potrebbe ottimizzare la durabilità del trattamento.
Come le cellule immunitarie cerebrali possono attenuare la terapia
Nel cervello reale, i tumori sono circondati non solo da neuroni e glia ma anche da microglia, le cellule immunitarie residenti del cervello. Per catturare questo livello di complessità, gli scienziati hanno aggiunto microglia derivate da cellule staminali nei loro organoidi. Queste cellule sono maturate, hanno assunto morfologie e profili di espressione genica specifici delle microglia trovate nel glioma midline diffuso e hanno prodotto molecole associate a un ambiente immunosoppressivo. Quando le cellule CAR T sono state aggiunte ad organoidi portatori di tumore contenenti microglia, le T si sono spostate ulteriormente verso stati esausti e a basso effetto, e il controllo tumorale è peggiorato. Allo stesso tempo, fattori infiammatori legati agli effetti collaterali del trattamento, come l’IL‑6, sono aumentati, suggerendo che il modello può anche aiutare a studiare le tossicità correlate alle CAR T.
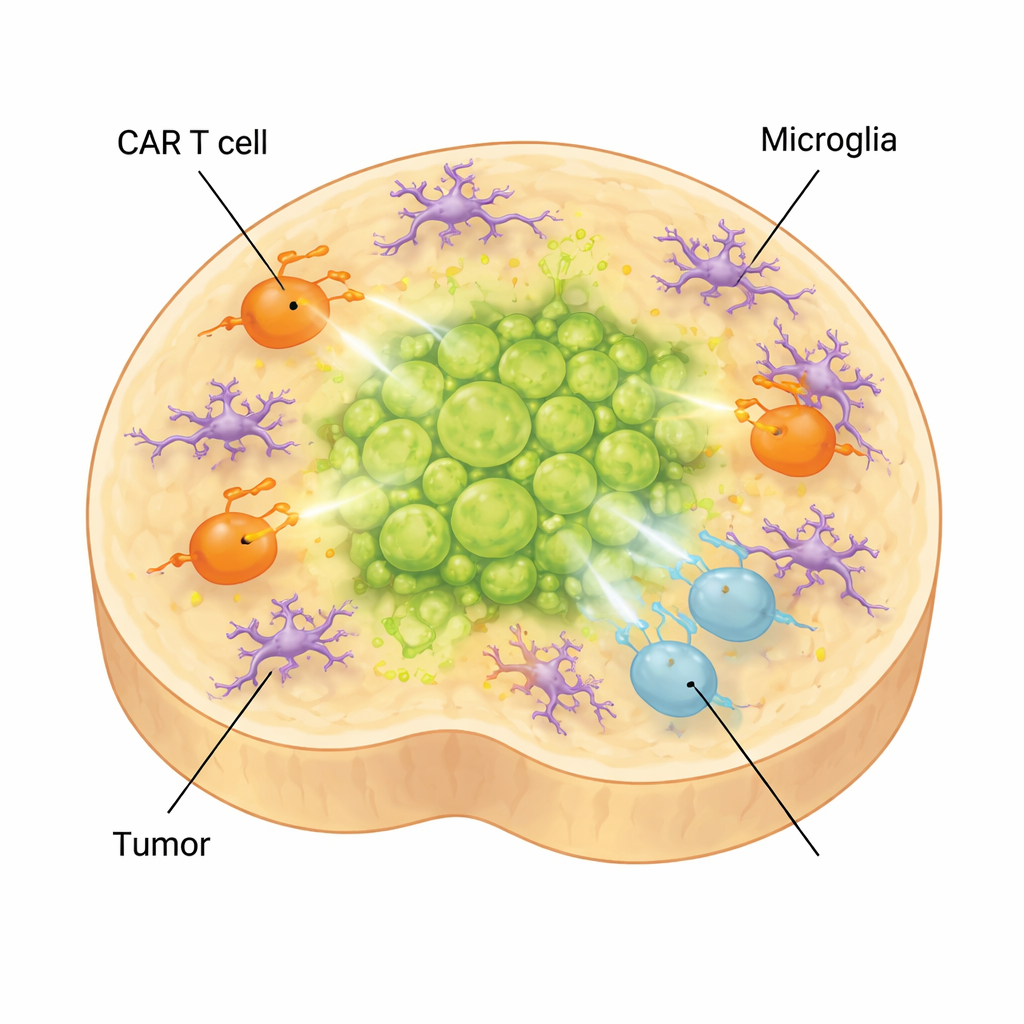
Cosa significa per i bambini affetti da questo tumore
Per le famiglie che affrontano un glioma midline diffuso, questo lavoro non offre ancora una nuova cura, ma fornisce un potente terreno di prova per arrivarci più rapidamente. Ricreando l’ambiente del tronco encefalico del bambino e il tumore in provetta, gli scienziati possono ora osservare, in tempo reale, come diverse cellule tumorali, tipi di cellule CAR T e microglia interagiscano nel corso di settimane. Questo permette di identificare quali cellule T ingegnerizzate sono più efficaci, come e quando si esauriscono e come le cellule immunitarie residenti del cervello minano i loro sforzi. In ultima analisi, tali modelli di organoidi potrebbero essere personalizzati per pazienti individuali e usati per perfezionare le immunoterapie prima della somministrazione, migliorando le probabilità che le future terapie con cellule CAR T siano sia più sicure sia più efficaci per i bambini.
Citazione: Bessler, N., Wezenaar, A.K.L., Ariese, H.C.R. et al. De novo H3.3K27M-altered diffuse midline glioma in human brainstem organoids to dissect GD2 CAR T cell function. Nat Cancer 7, 316–333 (2026). https://doi.org/10.1038/s43018-025-01084-0
Parole chiave: glioma midline diffuso, organoidi cerebrali, cellule CAR T, cancro cerebrale pediatrico, microglia