Clear Sky Science · it
Rapporto sulla riutilizzabilità: Valutazione delle prestazioni di un modello di base meta‑learning nella predizione dell’attività antibatterica di prodotti naturali
Ricercare nuovi antibiotici, più velocemente
La resistenza agli antibiotici è in aumento, ma scoprire nuovi farmaci è dolorosamente lento e spesso dipende da tentativi ed errori in laboratorio. Questo studio esplora se un potente tipo di intelligenza artificiale, addestrata originariamente su vaste collezioni di dati farmacologici, possa essere rapidamente adattata per prevedere quali composti naturali di origine vegetale potrebbero combattere i batteri—utilizzando solo piccole quantità di nuovi dati sperimentali. Se efficace, uno strumento del genere potrebbe aiutare gli scienziati a concentrare il tempo prezioso in laboratorio sui candidati più promettenti e accelerare la ricerca della prossima generazione di antibiotici.
Perché i composti vegetali sono importanti
Molti dei nostri migliori antibiotici hanno avuto origine come prodotti naturali provenienti da piante e microrganismi. Queste molecole possono arrestare la crescita batterica, ma trovarne di nuove in natura è un po’ come cercare aghi in un pagliaio. I ricercatori devono testare molti composti contro numerosi ceppi batterici, e ogni test ha un costo elevato. Peggio ancora, grandi dataset accuratamente etichettati—di cui i moderni metodi di deep learning hanno bisogno per funzionare bene—sono rari in questo campo. Ciò rende la scoperta di antibiotici un banco di prova ideale per i “modelli di base”: sistemi di IA ampi e generali che possono essere messa a punto per compiti specifici con solo pochi esempi nuovi.
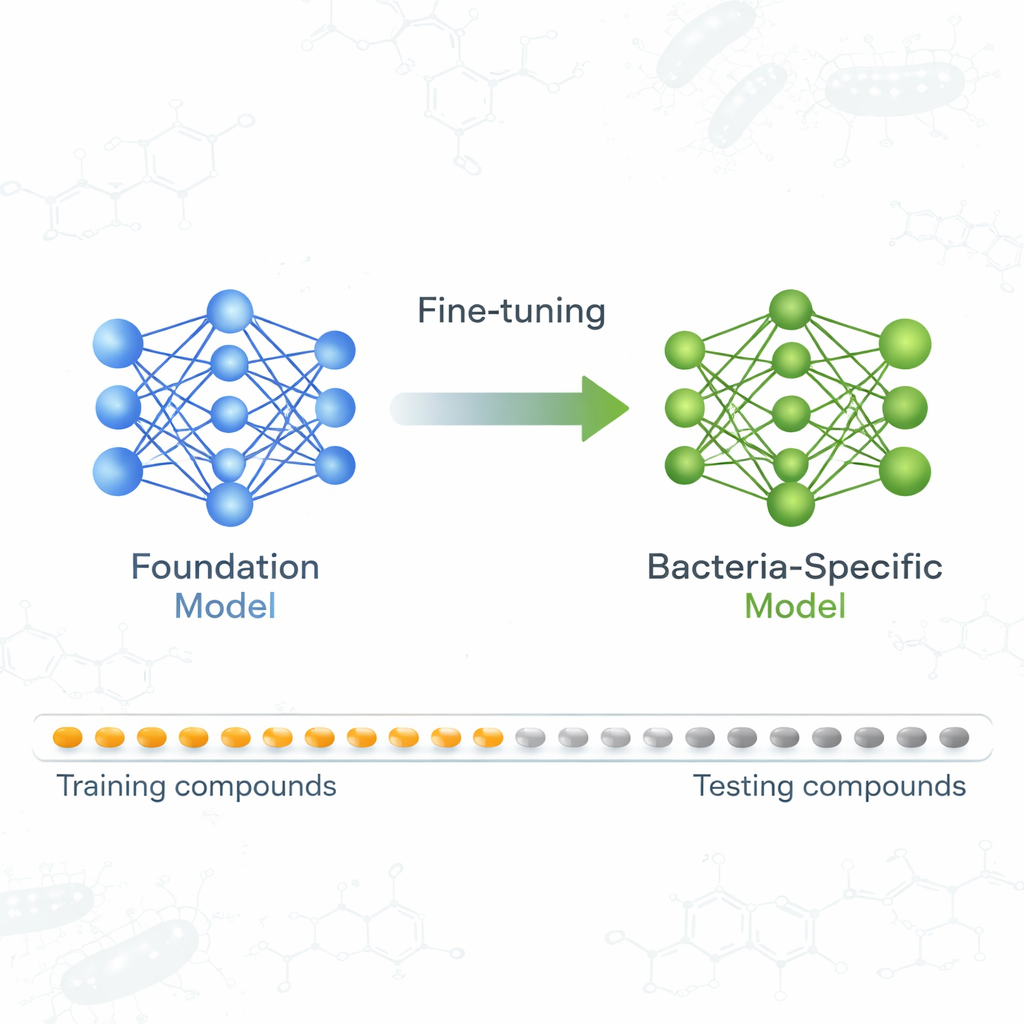
Un modello di base impara a riconoscere gli agenti antibatterici
Il gruppo si è concentrato su un modello di base chiamato ActFound, addestrato inizialmente a prevedere con quale intensità diversi composti chimici influenzano bersagli biologici, usando grandi dataset provenienti da risorse come i database ChEMBL e BindingDB. Invece di prevedere un singolo valore per ogni composto, ActFound impara confrontando coppie di composti all’interno dello stesso esperimento e stimando quale dei due è più attivo. Questo apprendimento “per coppie”, combinato con una strategia di addestramento nota come meta‑learning, è pensato per aiutare il modello ad adattarsi rapidamente a nuovi compiti di predizione quando sono disponibili solo poche osservazioni etichettate—esattamente la situazione in molti screening antibiotici.
Testare il modello su dati reali di prodotti vegetali
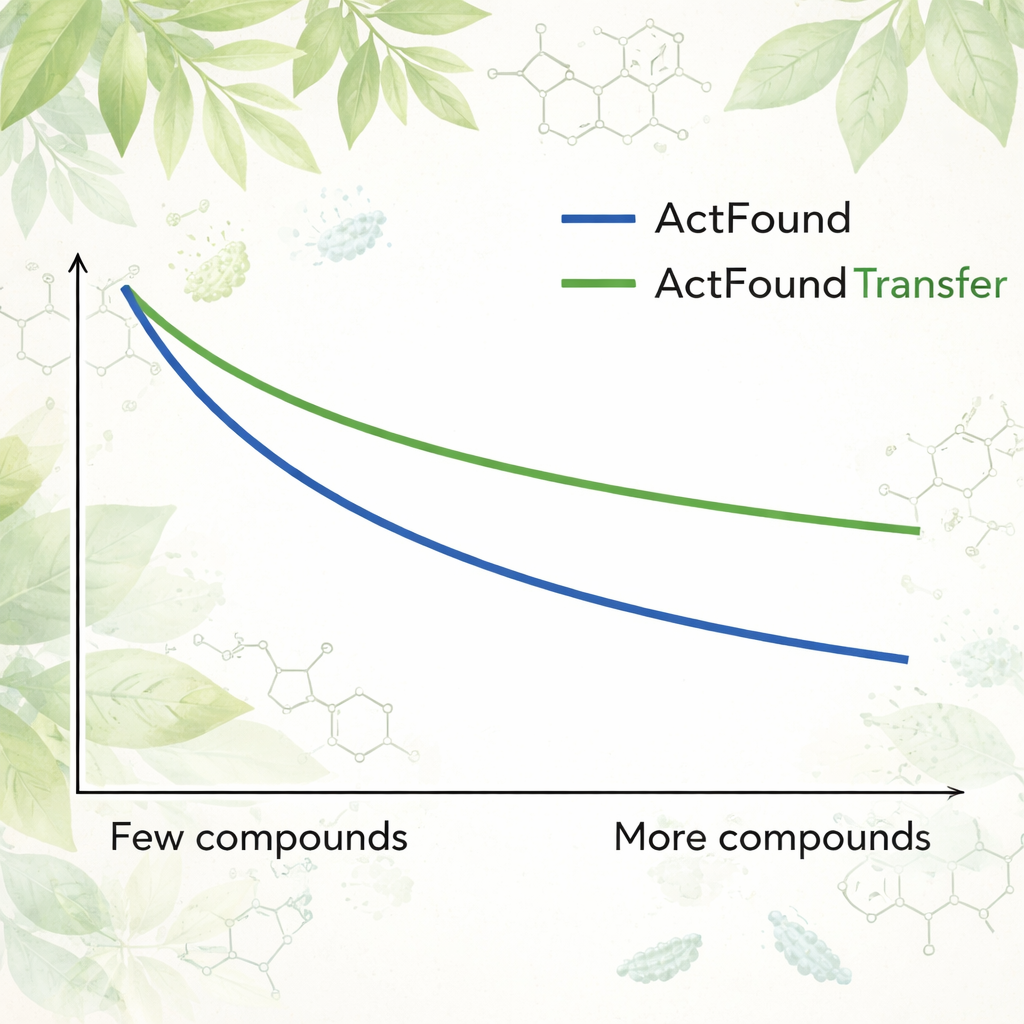
Per verificare la reale riutilizzabilità di ActFound, gli autori lo hanno messa a punto su un dataset curato di prodotti naturali di origine vegetale testati per la loro capacità di inibire la crescita di vari batteri. Ogni ceppo batterico è stato trattato come un compito a sé, e il modello è stato adattato usando solo da 8 a 128 composti per ceppo, o percentuali fisse dei dati disponibili. Hanno inoltre confrontato ActFound con modelli più semplici di meta‑learning e transfer learning che non utilizzano confronti per coppie. In questi test, ActFound non ha raggiunto la precisione mostrata in lavori precedenti su altri tipi di dati farmacologici. Tuttavia, quando i dati erano molto scarsi—circa solo una manciata di composti per ceppo—ActFound e la sua variante di transfer learning in genere eguagliavano o superavano i metodi alternativi.
Quando la similarità aiuta—e quando ostacola
ActFound presuppone che molecole simili si comportino in modo simile, un assunto che funziona bene quando i dataset sono costruiti attorno a gruppi di composti correlati. Il dataset di prodotti naturali, tuttavia, era chimicamente diversificato e spesso privo di “famiglie” di composti strettamente correlate. Questa diversità, pur essendo scientificamente preziosa, ha compromesso la strategia di apprendimento per coppie: quando i composti all’interno di un esperimento sono molto diversi tra loro, il modello fatica a imparare confronti stabili. Gli autori hanno anche riscontrato che un semplice diagnostico, proposto nel lavoro originale su ActFound per prevedere in anticipo come il modello si sarebbe comportato su un nuovo compito, non reggeva con questi dati di prodotti naturali, evidenziando un limite importante nel trasferire il modello a nuovi spazi chimici.
Cosa significa per la futura scoperta di farmaci
Per i non specialisti, la conclusione è che modelli di base come ActFound sono strumenti promettenti per la scoperta di farmaci quando i dati scarseggiano, ma non sono bacchette magiche. In questo studio, ActFound e la sua versione di transfer learning spesso hanno fatto tanto quanto o meglio dei metodi concorrenti quando erano disponibili solo pochi composti vegetali per l’addestramento, ma hanno incontrato difficoltà su questo set altamente diversificato di prodotti naturali. Il lavoro suggerisce che questi modelli di IA sono più utili quando i dati includono molti composti chimicamente simili—come negli studi mirati alle relazioni struttura‑attività—ma restano meno affidabili nel prevedere il comportamento di tipi di molecole completamente nuovi. In altre parole, l’IA può aiutare a restringere la ricerca, ma la parte più difficile dell’esplorazione di nuovi territori chimici è ancora davanti a noi.
Citazione: Butt, C.M., Walker, A.S. Reusability Report: Evaluating the performance of a meta-learning foundation model on predicting the antibacterial activity of natural products. Nat Mach Intell 8, 270–275 (2026). https://doi.org/10.1038/s42256-026-01187-y
Parole chiave: scoperta di antibiotici, prodotti naturali, deep learning, meta‑learning, screening di farmaci