Clear Sky Science · it
La fosforilazione di PLIN5 orchestra l’accoppiamento mitocondri-gocce lipidiche per controllare il flusso lipidico epatico e la steatosi
Perché il grasso nel fegato conta
Molte persone accumulano grasso nel fegato senza avvertire sintomi, eppure questo accumulo silenzioso può alla lunga portare a infiammazione, fibrosi e perfino cancro. Questo studio pone una domanda semplice ma cruciale: quando ondate di lipidi raggiungono il fegato durante il digiuno o a seguito di una dieta ricca in stile “occidentale”, come decidono le cellule epatiche se quei grassi saranno bruciati per produrre energia o immagazzinati in modo sicuro, e quando questo meccanismo di protezione comincia a cedere?
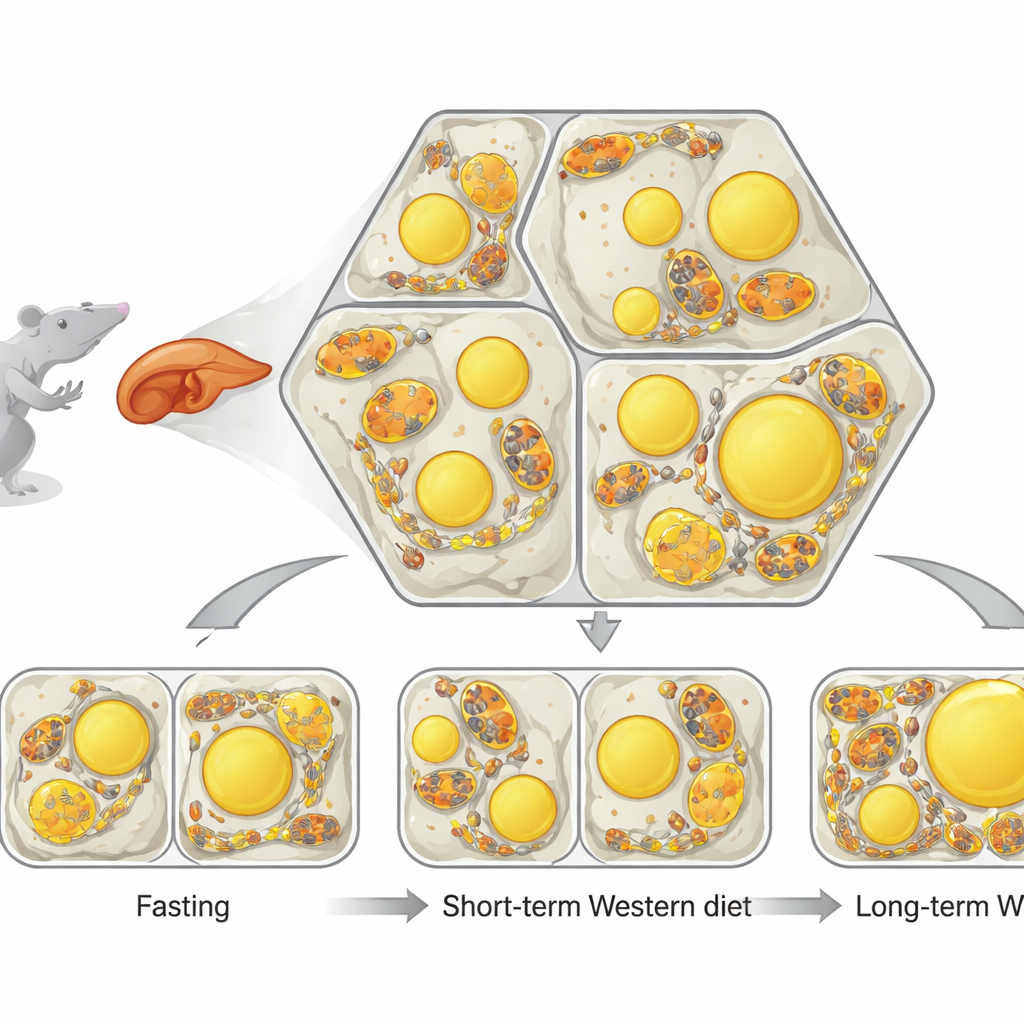
Piccole centrali e minuscole bolle di grasso
Il fegato è organizzato in unità ripetute a forma quasi esagonale dove il sangue scorre da un lato all’altro. Lungo questo percorso le cellule epatiche si specializzano: alcune prevalentemente bruciano grassi per produrre energia, altre principalmente sintetizzano e immagazzinano lipidi. All’interno di ogni cellula, due strutture sono fondamentali. I mitocondri sono le centrali energetiche della cellula, e le gocce lipidiche sono piccole bolle piene di grasso usate per lo stoccaggio. I ricercatori hanno messo a punto una potente pipeline di imaging e analisi, chiamata single-cell phenotypic profiling (scPhenomics), per mappare dimensione, forma e disposizione di queste strutture in migliaia di cellule direttamente in sezioni tissutali. Hanno scoperto che anche in animali sani la forma dei mitocondri e il contenuto di gocce lipidiche formano pattern spaziali distinti che rispecchiano dove avviene la combustione rispetto allo stoccaggio nel fegato.
Digiuno versus dieta ricca
Successivamente il team ha chiesto cosa succede quando il fegato viene improvvisamente inondato di grassi. Il digiuno mobilita i lipidi dalle riserve adipose verso il fegato, mentre una dieta in stile occidentale a breve termine apporta grassi extra direttamente dal cibo. Nei topi digiuni le gocce lipidiche aumentarono in tutto il fegato, e i mitocondri si allungarono spesso avvolgendosi strettamente attorno a queste bolle lipidiche, formando numerosi siti di contatto. Nei topi nutriti per alcune settimane con una dieta occidentale, anche il fegato si riempì di grasso, ma le gocce si disposero in modo diverso e i mitocondri rimasero per lo più separati e più arrotondati. Ciò dimostrò che il modo in cui il grasso arriva — attraverso il digiuno o l’alimentazione cronica ricca — innesca risposte strutturali molto diverse all’interno delle cellule epatiche, anche quando il contenuto lipidico complessivo appare simile.
Un interruttore molecolare per la gestione dei grassi
Per scoprire cosa controlla questi contatti tra organelli, gli autori hanno combinato l’imaging con misurazioni proteiche in cellule epatiche prelevate da zone e condizioni dietetiche diverse. Una proteina emersa con evidenza è stata perilipina‑5 (PLIN5), che riveste le gocce lipidiche e può collegare i mitocondri a queste ultime. Il digiuno aumentò i livelli di PLIN5 e la posizionò proprio all’interfaccia tra mitocondri e gocce. I ricercatori quindi usarono un virus mirato al fegato per elevare i livelli di PLIN5 e testare versioni della proteina che imitano diversi stati acceso/spento di un singolo segnale chimico chiamato fosforilazione. Una versione incapace di essere fosforilata (S155A) aumentò marcatamente i contatti mitocondri–gocce e ingrandì le gocce lipidiche, anche con dieta normale. Una versione che simulava la fosforilazione costante (S155E) fece l’opposto: i mitocondri raramente toccavano le gocce, che rimasero meno numerose e più piccole.
Proteggere le cellule dal danno indotto dai grassi
Il team valutò poi cosa ciò significasse per la salute epatica sotto una dieta occidentale. Quando i topi seguirono questa dieta per diverse settimane, la variante PLIN5 non fosforilabile (S155A) convogliò più grasso nelle gocce e aumentò il contenuto di trigliceridi epatici, eppure i marcatori di stress ossidativo dannoso risultarono in realtà più bassi. Al contrario, la versione fosfo‑mimetica (S155E) lasciò più grassi liberi e segnali di un ambiente più ossidante e potenzialmente dannoso, con riserve antiossidanti inferiori. Di fatto, strette associazioni tra mitocondri e gocce lipidiche sembravano funzionare come una valvola di sicurezza, convogliando gli acidi grassi in eccesso verso depositi neutri di trigliceridi e limitando le reazioni chimiche a catena che danneggiano membrane e proteine. Tuttavia, nel lungo periodo di esposizione a una dieta occidentale, anche i contatti mitocondri–gocce aumentarono nuovamente e furono associati a un maggiore accumulo di grasso sia nei topi sia in campioni di fegato umano, suggerendo che lo stesso circuito protettivo può essere sovraccaricato e contribuire alla progressione della malattia.
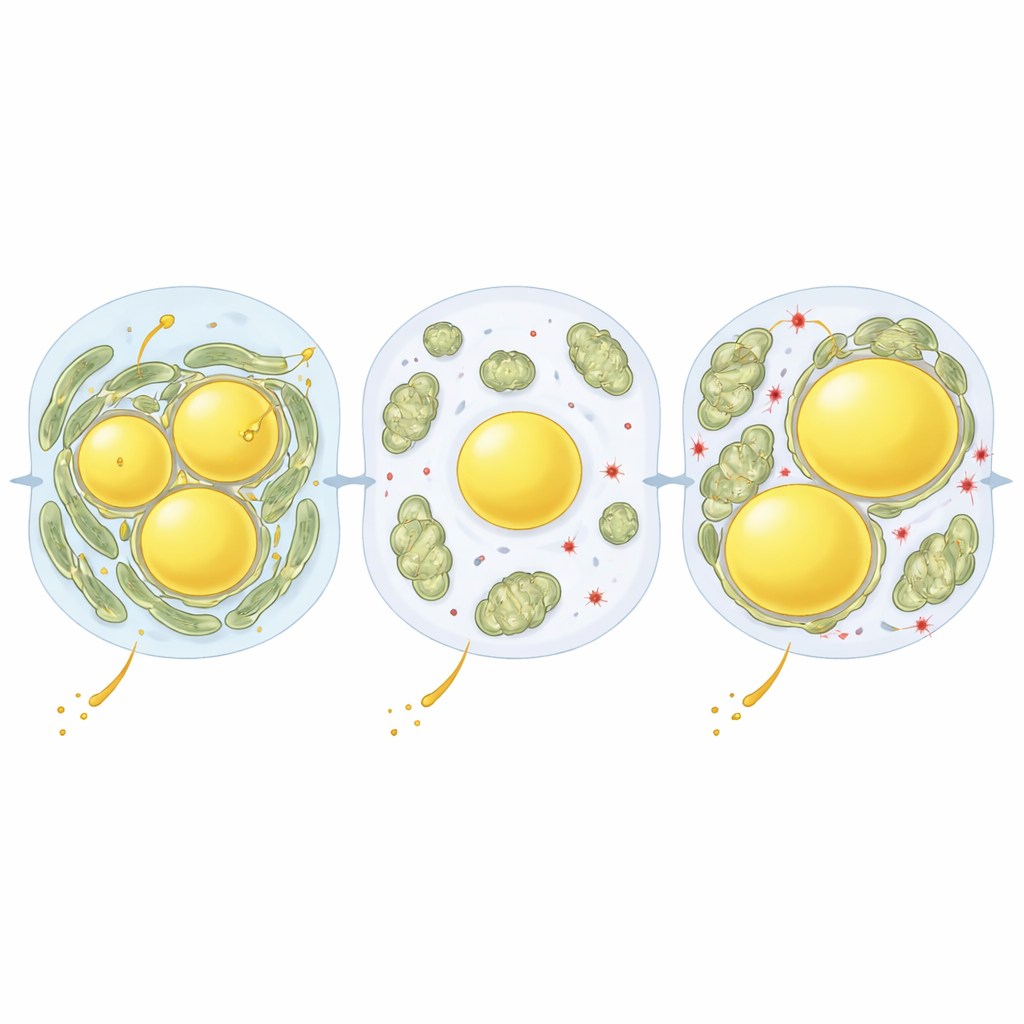
Una nuova leva sulla malattia del fegato grasso
Nel complesso, questo lavoro mostra che le cellule epatiche rimodellano attivamente le relazioni fisiche tra le loro centrali energetiche e i depositi di grasso per far fronte a condizioni nutrizionali variabili. PLIN5, e in particolare il suo stato di fosforilazione in un singolo sito, funziona come una manopola di regolazione fine che rafforza o allenta l’accoppiamento mitocondri–gocce lipidiche. Un accoppiamento stretto favorisce l’incapsulamento dei grassi liberi potenzialmente tossici in depositi più sicuri di trigliceridi e aiuta a tamponare stress nutrizionali a breve termine, come il digiuno o l’esposizione breve a una dieta ricca. Quando questo programma adattativo è attenuato, o quando l’esposizione a diete ricche di grassi persiste per mesi o anni, l’equilibrio si sposta verso lipotossicità e danno ossidativo. Rivelando questo “circuito” strutturale all’interno delle cellule epatiche, lo studio suggerisce che farmaci in grado di modulare l’attività di PLIN5 o i contatti mitocondri–gocce potrebbero offrire un nuovo modo per rallentare o prevenire la malattia del fegato grasso nell’uomo.
Citazione: Kang, S.W.S., Brown, L.A., Miller, C.B. et al. PLIN5 phosphorylation orchestrates mitochondria lipid-droplet coupling to control hepatic lipid flux and steatosis. Nat Metab 8, 587–603 (2026). https://doi.org/10.1038/s42255-026-01476-1
Parole chiave: steatosi epatica, metabolismo del fegato, mitocondri, gocce lipidiche, perilipina 5