Clear Sky Science · it
Gli acidi grassi favoriscono la respirazione disaccoppiata tramite i trasportatori ATP/ADP negli adipociti bianchi
Perché le cellule adipose possono contribuire a bruciare energia
La maggior parte delle persone considera il grasso corporeo come un silenzioso deposito di calorie. Questo studio mette in luce un aspetto sorprendentemente attivo degli adipociti bianchi: in condizioni adeguate possono disperdere combustibile e generare calore. Scoprendo un nuovo meccanismo con cui le cellule adipose permettono una «perdita» di energia, il lavoro apre la strada a strategie per aumentare il dispendio calorico e potenzialmente contrastare l’obesità.
Quando il grasso immagazzinato torna a essere combustibile
Nella vita quotidiana gli adipociti bianchi passano gran parte del tempo a immagazzinare energia sotto forma di trigliceridi—grandi goccioline di grasso. Durante l’esercizio, il digiuno o l’esposizione al freddo, segnali di stress inducono la degradazione dei trigliceridi in un processo chiamato lipolisi, con rilascio di acidi grassi e glicerolo. I ricercatori hanno confermato che quando questa degradazione è stimolata in adipociti bianchi coltivati in laboratorio, le cellule aumentano notevolmente il consumo di ossigeno, segnale che le loro centrali energetiche, i mitocondri, lavorano più intensamente. Bloccare il primo step della lipolisi ha interrotto sia il rilascio di acidi grassi sia l’aumento del consumo di ossigeno, dimostrando che il processo dipende dagli acidi grassi stessi.
Gli acidi grassi liberi come interruttori della combustione energetica
Gli acidi grassi che lasciano la cellula adiposa non escono tutti dal tessuto; alcuni rimangono all’interno. Il team ha mostrato che questi acidi grassi liberi residui sono fondamentali per aumentare l’attività mitocondriale. Quando una proteina nel mezzo di coltura è stata usata per sequestrare gli acidi grassi, le cellule hanno rilasciato più grasso in totale ma il loro consumo di ossigeno è diminuito, indicando che livelli interni elevati di acidi grassi—non solo la lipolisi in sé—guidano la respirazione extra. Al contrario, bloccare la riformazione dei trigliceridi, via che normalmente ricompone gli acidi grassi, ha aumentato il consumo di ossigeno e ulteriormente abbassato il potenziale elettrico attraverso la membrana mitocondriale. Nel complesso, questi risultati suggeriscono che gli acidi grassi liberi spingono i mitocondri in uno stato “perdente”, che spreca energia.
Un nuovo attore nella respirazione produttiva di calore
Nella classica termogenesi del tessuto adiposo bruno, una proteina chiamata UCP1 crea dei passaggi nella barriera mitocondriale in modo che l’energia del cibo venga rilasciata come calore anziché immagazzinata come carburante cellulare. Gli adipociti bianchi esprimono poca o nessuna UCP1, quindi gli autori hanno cercato un’altra via. Si sono concentrati sul trasportatore ATP/ADP, una proteina che normalmente scambia la valuta energetica della cellula attraverso la barriera mitocondriale. Usando sia un bloccante chimico specifico sia strumenti genetici per ridurre questo trasportatore, hanno dimostrato che è necessario per la perdita indotta dagli acidi grassi: bloccare il trasportatore ha mantenuto il potenziale mitocondriale e impedito l’aumento del consumo di ossigeno durante la lipolisi, nonostante la lipolisi proseguisse normalmente. Questo indica che gli acidi grassi liberi agiscono insieme al trasportatore per creare una perdita controllata di protoni attraverso la barriera mitocondriale, attivando la respirazione disaccoppiata.
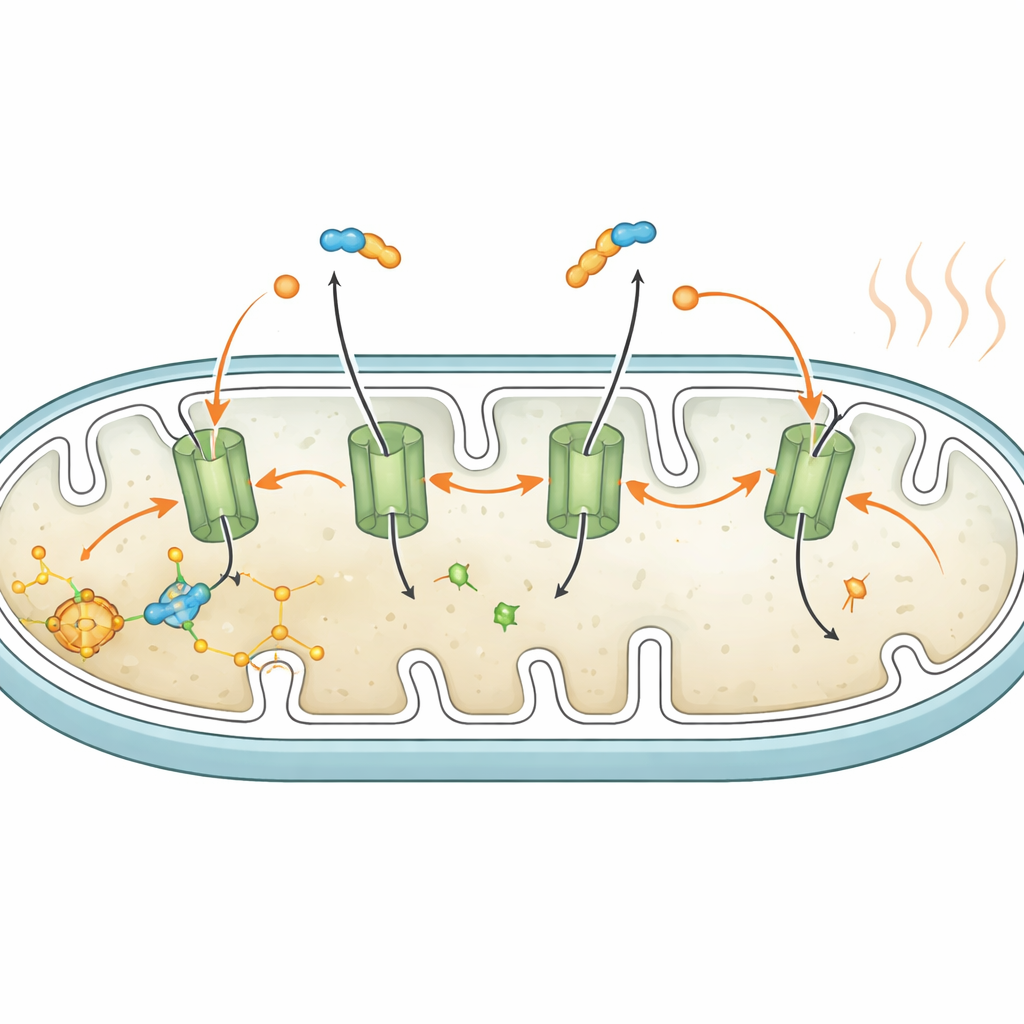
Dalla coltura cellulare agli animali viventi
Per verificare se questa perdita di energia è significativa negli animali interi, i ricercatori hanno usato topi in cui una proteina di segnalazione chiamata STAT3 era stata rimossa specificamente dagli adipociti. Questi animali eseguono la lipolisi normalmente ma presentano una respirazione indotta dagli acidi grassi ridotta nel tessuto adiposo bianco. In condizioni di laboratorio abituali, dove il grasso bruno è attivo e gestisce la maggior parte della difesa dal freddo, questi topi restavano caldi come i loro consimili normali. Tuttavia, quando i topi sono stati resi obesi e mantenuti a una temperatura in cui il grasso bruno è largamente inattivo, gli animali privi di STAT3 nel tessuto adiposo sono diventati sensibili al freddo e hanno mostrato un incremento più debole del consumo di ossigeno complessivo durante l’esposizione al freddo o la lipolisi indotta farmacologicamente. È importante notare che cambiamenti simili non sono stati osservati quando STAT3 è stato eliminato solo nel grasso bruno, indicando un ruolo specifico del tessuto adiposo bianco.
Il tessuto adiposo bianco come riscaldatore nascosto
Lo studio conclude che negli adipociti bianchi gli acidi grassi liberi generati durante la lipolisi attiva possono legarsi al trasportatore ATP/ADP nei mitocondri e innescare una perdita di energia che produce calore anziché carburante cellulare utile. Negli animali obesi mantenuti caldi, questa respirazione disaccoppiata nel tessuto adiposo bianco contribuisce in modo significativo al mantenimento della temperatura corporea e al dispendio energetico complessivo, specialmente quando il tessuto adiposo bruno e il tremore muscolare sono limitati. Poiché il tessuto adiposo bianco è abbondante negli adulti, in particolare nell’obesità, potenziare leggermente questa perdita potrebbe offrire un nuovo modo per aumentare il consumo calorico quotidiano e supportare terapie per la perdita di peso, a condizione che sia possibile farlo in modo sicuro e senza danneggiare altri tessuti.
Citazione: Ahmadian, M., Aksu, A.M., Dhillon, P. et al. Fatty acids promote uncoupled respiration via ATP/ADP carriers in white adipocytes. Nat Metab 8, 572–586 (2026). https://doi.org/10.1038/s42255-026-01467-2
Parole chiave: tessuto adiposo bianco, acidi grassi, disaccoppiamento mitocondriale, termogenesi, obesità