Clear Sky Science · it
PFKM governa i cambiamenti metabolici durante la differenziazione del muscolo scheletrico
Perché le cellule muscolari hanno bisogno di un uso intelligente dello zucchero
Quando ci alleniamo o semplicemente ci alziamo da una sedia, i nostri muscoli scheletrici entrano in azione, bruciando zucchero per alimentare ogni contrazione. Ma le giovani cellule staminali muscolari e le fibre muscolari completamente formate non trattano lo zucchero allo stesso modo. Questo studio mette in luce un sistema di commutazione incorporato — centrato su un singolo enzima chiamato PFKM — che decide se il glucosio venga ossidato per energia immediata o deviato per proteggere e ricostruire le cellule. Capire questo interruttore potrebbe aprire nuove strade per trattare la debolezza muscolare, l’invecchiamento dei muscoli e malattie metaboliche ereditarie.
Un semaforo per il carburante cellulare
Il glucosio che entra nella cellula può seguire diverse vie. Una strada principale, la glicolisi, converte rapidamente lo zucchero in energia e in mattoni per le fibre muscolari in crescita. Un’altra via, la via dei pentoso fosfati, produce molecole che difendono le cellule dallo stress ossidativo e supportano la sintesi di DNA e lipidi. I ricercatori si sono concentrati su PFKM, una variante della fosfofruttochinasi-1 che occupa un punto di snodo nella glicolisi. Misurando centinaia di metaboliti nell’arco di minuti-ore dopo l’attivazione di un segnale di crescita chiamato Wnt, hanno osservato un rapido accumulo di intermedi precoci della glicolisi mentre il prodotto dell’attività di PFKM diminuiva e aumentavano i metaboliti della via dei pentoso fosfati. Questo suggerisce che le cellule stessero effettivamente rallentando PFKM per deviare lo zucchero verso chimiche protettive invece che verso la sola produzione di energia. 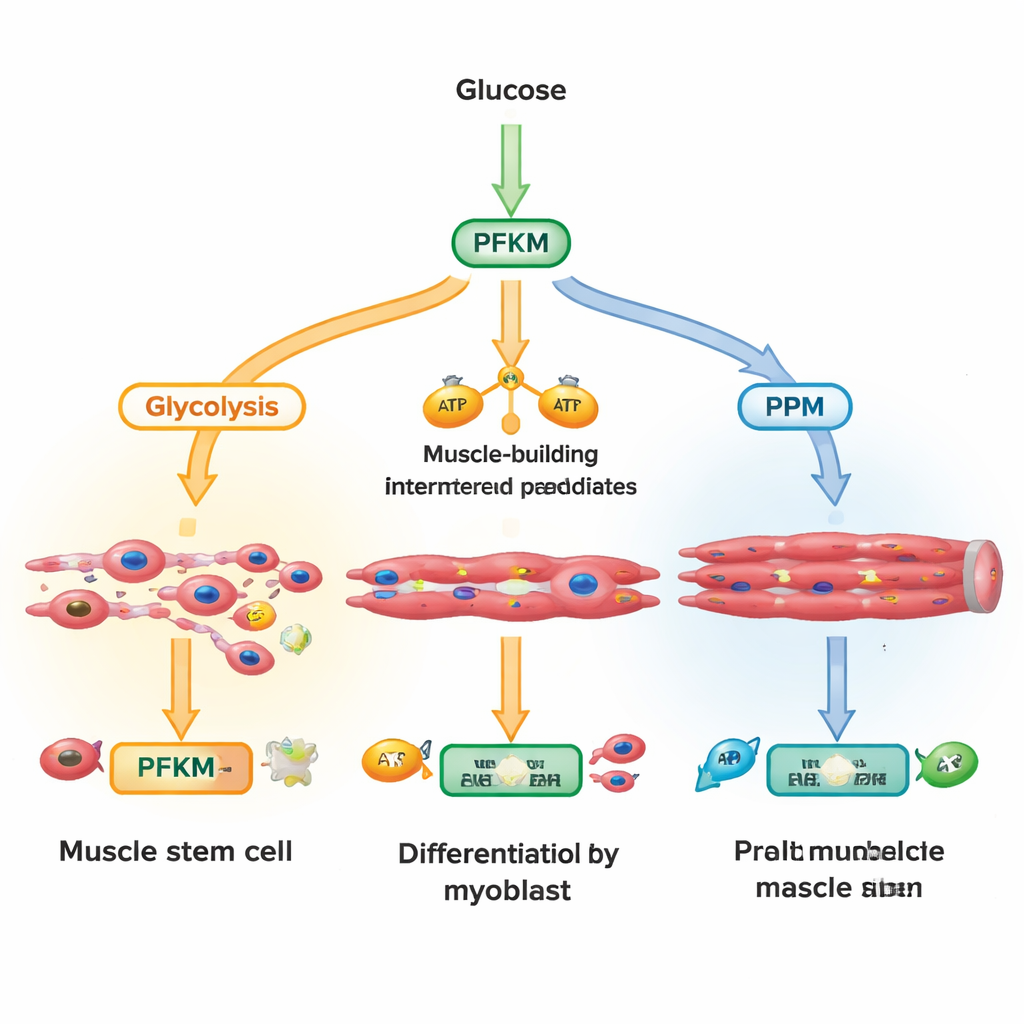
Taggare e rimuovere l’enzima guardiano
Per capire come PFKM venga regolato, il gruppo ha seguito la localizzazione della proteina nelle cellule. In condizioni di riposo, PFKM era distribuito nel citoplasma. Nei minuti successivi alla stimolazione Wnt, si è raccolto in punti luminosi che si sovrapponevano ai lisosomi, i compartimenti cellulari che degradano le proteine. Due isoforme parentali, PFKL e PFKP, non si sono spostate né hanno cambiato livello, rivelando che solo la forma muscolare PFKM veniva presa di mira. Test biochimici hanno mostrato che bloccare la funzione lisosomiale impediva la perdita di PFKM, mentre inibire il proteasoma — l’altro principale sistema di smaltimento proteico — non aveva effetto. L’analisi delle sequenze ha individuato un breve motivo «methyl arginine degron» unico per PFKM. L’enzima PRMT1 aggiungeva un’impronta di metilazione su un arginina all’interno di questo motivo, e questo tag consentiva alla macchina della microautofagia, incluso il protein VPS4, di traslocare PFKM nei lisosomi per la degradazione. Disattivare PRMT1 o VPS4 stabilizzava PFKM e bloccava la sua rimozione.
Dalla cellula staminale alla fibra muscolare funzionante
Utilizzando grandi dataset singola-cellula umani, gli autori hanno mappato i livelli di PFKM attraverso molti tipi cellulari muscolari. Le cellule staminali muscolari, che rimangono dormienti finché non sono necessarie per la riparazione, presentavano pochissimo PFKM ma esprimevano numerosi geni della via dei pentoso fosfati e componenti lisosomiali. Man mano che le cellule si impegnavano a diventare muscolo e si fondevano in fibre multinucleate, i trascritti e le proteine di PFKM aumentavano bruscamente, mentre i bersagli di Wnt e i geni lisosomiali diminuivano. In cellule muscolari umane e murine coltivate, Wnt spingeva rapidamente PFKM verso i lisosomi nelle cellule precoci a nucleo singolo ma non nelle fibre mature multinucleate. Questo schema supporta un modello in cui le cellule indifferenziate mantengono PFKM basso — tramite degradazione lisosomiale — per favorire un metabolismo protettivo, per poi riesprimerlo mentre transitano in fibre contrattili ad alto dispendio energetico.
Cosa succede quando l’interruttore resta bloccato
Per testare quanto sia cruciale PFKM per la formazione del muscolo, il team ha ridotto i suoi livelli con interferenza a RNA. Le cellule con basso PFKM faticavano ad attivare i geni caratteristici del muscolo, producevano meno proteina miosina e formavano fibre multinucleate più poche e più piccole, anche se il numero complessivo di cellule non cambiava. Il profilo dei metaboliti ha rivelato una riduzione degli intermedi glicolitici a valle e dei combustibili per il ciclo degli acidi tricarbossilici, ma un aumento dei geni e dei marcatori della via dei pentoso fosfati, insieme a una maggiore resistenza allo stress ossidativo. Importante, fornire alle cellule 3‑fosfoglicerato — un intermedio glicolitico che normalmente si trova a valle di PFKM — ha risolto molti difetti di differenziazione. I marker muscolari e la formazione delle fibre sono rimbalzati, dimostrando che i metaboliti mancanti, più che la perdita della proteina PFKM in sé, erano il collo di bottiglia principale. 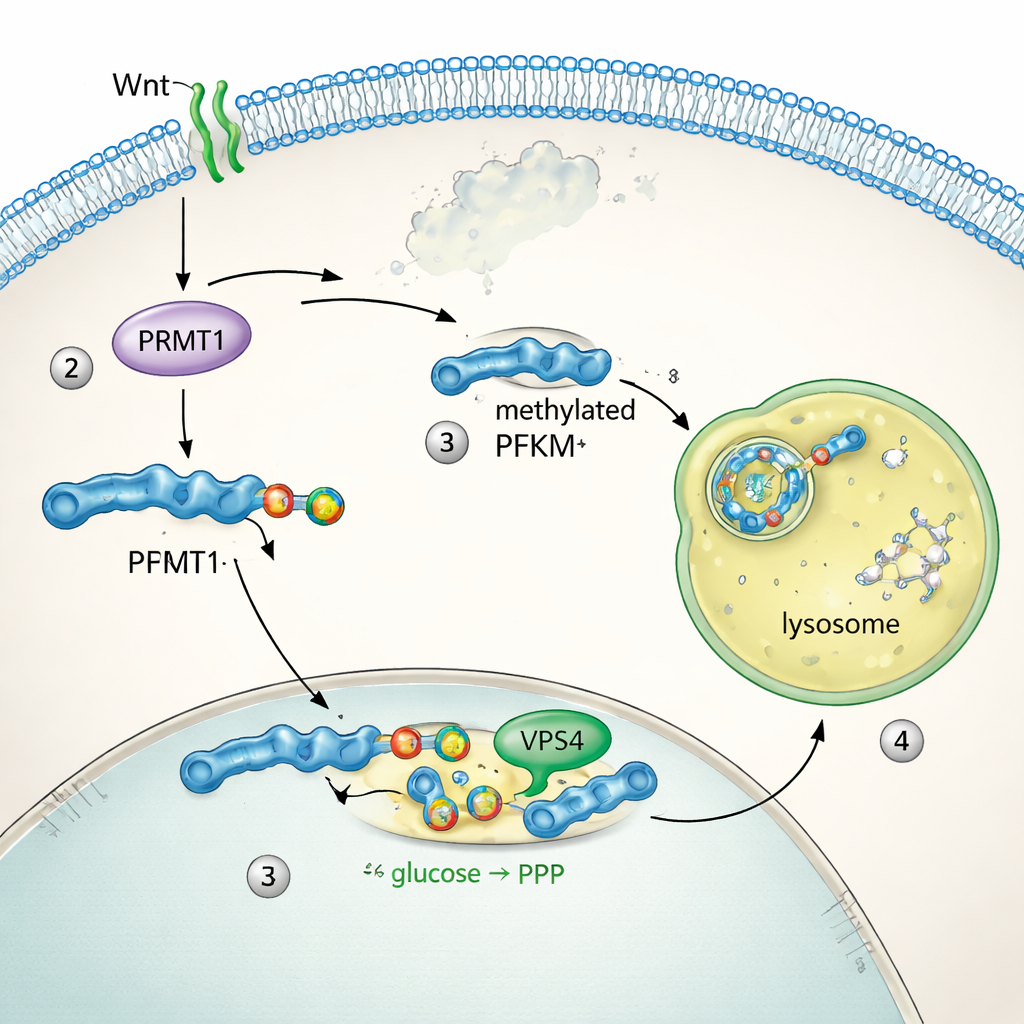
Implicazioni per la salute e la riparazione del muscolo
Per un non specialista, il messaggio centrale è che le cellule muscolari non si limitano a «bruciare zucchero» più o meno; lo reindirizzano con cura tra produzione di energia e protezione cellulare a seconda della loro fase vitale. PFKM funziona come una valvola regolabile in questo snodo. Nelle cellule di tipo staminale, il tagging indotto da Wnt e la distruzione lisosomiale di PFKM reindirizzano il glucosio verso una via che protegge le cellule e le prepara alla crescita futura. Quando le cellule maturano in fibre funzionanti, ricostituiscono le riserve di PFKM e spostano il metabolismo verso un uso energetico ad alta potenza. Interrompere questo equilibrio, come avviene in rare patologie da deficit di PFKM, compromette lo sviluppo muscolare normale. Identificando la maniglia molecolare su questo interruttore, lo studio suggerisce che terapie future potrebbero modulare la rigenerazione muscolare o proteggere i muscoli in malattie e invecchiamento regolando modestamente l’attività di PFKM o fornendo i giusti metaboliti a valle.
Citazione: Campos, M., Nguyen, S.T., Kong, X. et al. PFKM governs metabolic shifts throughout skeletal muscle differentiation. Nat Metab 8, 489–505 (2026). https://doi.org/10.1038/s42255-026-01457-4
Parole chiave: differenziazione del muscolo scheletrico, metabolismo del glucosio, enzima PFKM, via dei pentoso fosfati, degradazione proteica lisosomiale