Clear Sky Science · it
Il flusso catabolico della cisteina regolato da Lamin A/C modula il destino delle cellule staminali tramite il riprogrammazione dell’epigenoma
Come lo scheletro della cellula dialoga con il suo metabolismo
Perché alcune cellule rimangono giovani e plastiche nelle loro potenzialità, mentre altre invecchiano o si cristallizzano in un’identità sbagliata? Questo studio svela una sorprendente conversazione all’interno delle nostre cellule tra lo “scheletro” nucleare che organizza il DNA e un nutriente contenente zolfo, la cisteina. Mostrando come questo dialogo orienta le cellule staminali verso destini sani — o verso un precoce invecchiamento — il lavoro suggerisce che ciò che le cellule «mangiano» e come lo metabolizzano potrebbe un giorno essere modulato per prevenire alcune malattie genetiche e forse rallentare aspetti dell’invecchiamento.
Il ruolo nascosto del guscio nucleare
In profondità in ogni cellula, il DNA è appoggiato su una rete proteica chiamata lamina nucleare, costituita in parte da proteine note come lamin A e C. Queste lamina non solo conferiscono forma al nucleo; contribuiscono anche a decidere quali geni sono chiusi e quali restano accessibili. Gli autori hanno studiato cellule staminali embrionali di topo nel loro stato più flessibile, o «naive», e hanno scoperto che lamin A/C mantiene normalmente sotto controllo due enzimi metabolici, CBS e CTH, che partecipano alla sintesi e alla degradazione della cisteina. Quando lamin A/C è presente e attivo, questi enzimi sono repressi e l’elaborazione della cisteina rimane bassa, sostenendo uno stato staminale stabile e giovanile. 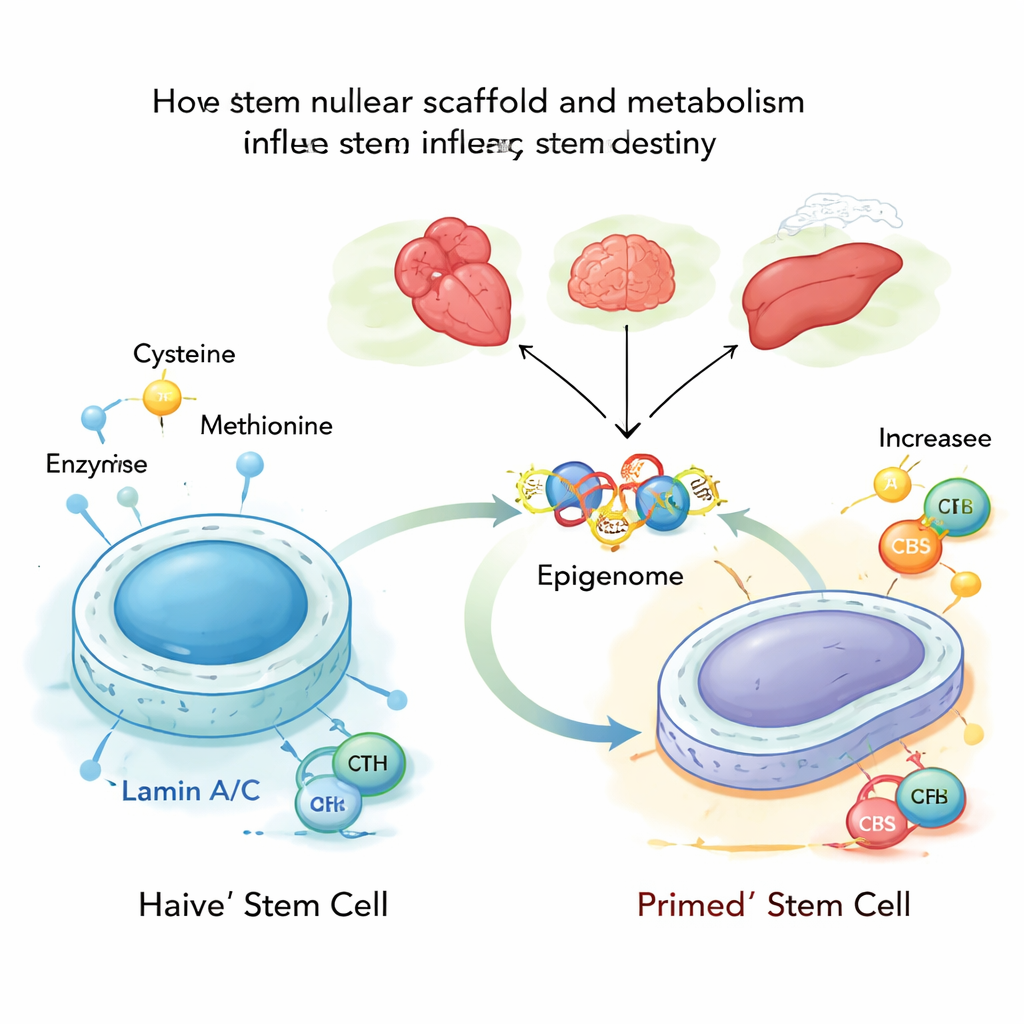
Quando la struttura cede, il metabolismo accelera
Successivamente i ricercatori hanno rimosso lamin A/C o introdotto una mutazione collegata a una malattia che imita un disturbo umano di invecchiamento precoce chiamato progeria di Hutchinson–Gilford. In assenza di lamin A/C normale, i geni CBS e CTH diventano più accessibili e vengono maggiormente legati da un fattore di trascrizione chiamato SP1, venendo attivati. Questo cambiamento convoglia più cisteina attraverso una via metabolica che termina in acetil‑CoA, una piccola molecola che trasporta gruppi acetile usati per allentare il confezionamento del DNA. Man mano che più cisteina viene incanalata verso l’acetil‑CoA, i gruppi acetile vengono preferenzialmente aggiunti a siti specifici sulle proteine istoniche — in particolare due posizioni sull’istone H3 note come K9 e K27 — rendendo i geni vicini più facilmente attivabili.
Dai marcatori chimici alle decisioni sul destino cellulare
Questi spostamenti nei «marchi» istonici agiscono come una ritonificazione globale del pannello di controllo cellulare. Nelle cellule staminali naive, l’aumento di CBS e CTH, o semplicemente la fornitura di più cisteina, spinge le cellule verso uno stato più avanzato, «primed», più vicino alla formazione di tessuti reali. I geni coinvolti nello sviluppo cardiaco e in altre linee diventano più attivi, e il ripiegamento tridimensionale del DNA cambia per favorire questi programmi. Al contrario, ridurre l’attività di CBS e CTH o limitare la cisteina aiuta a ristabilire un’identità più naive e giovanile anche quando la lamina nucleare è danneggiata. In modelli embrionali, questo disallineamento metabolico ha portato a una formazione alterata dei tre foglietti germinativi — i precursori di tutti gli organi — e a un’anomala propensione verso le cellule del muscolo cardiaco salvo che CBS e CTH venissero riequilibrati. 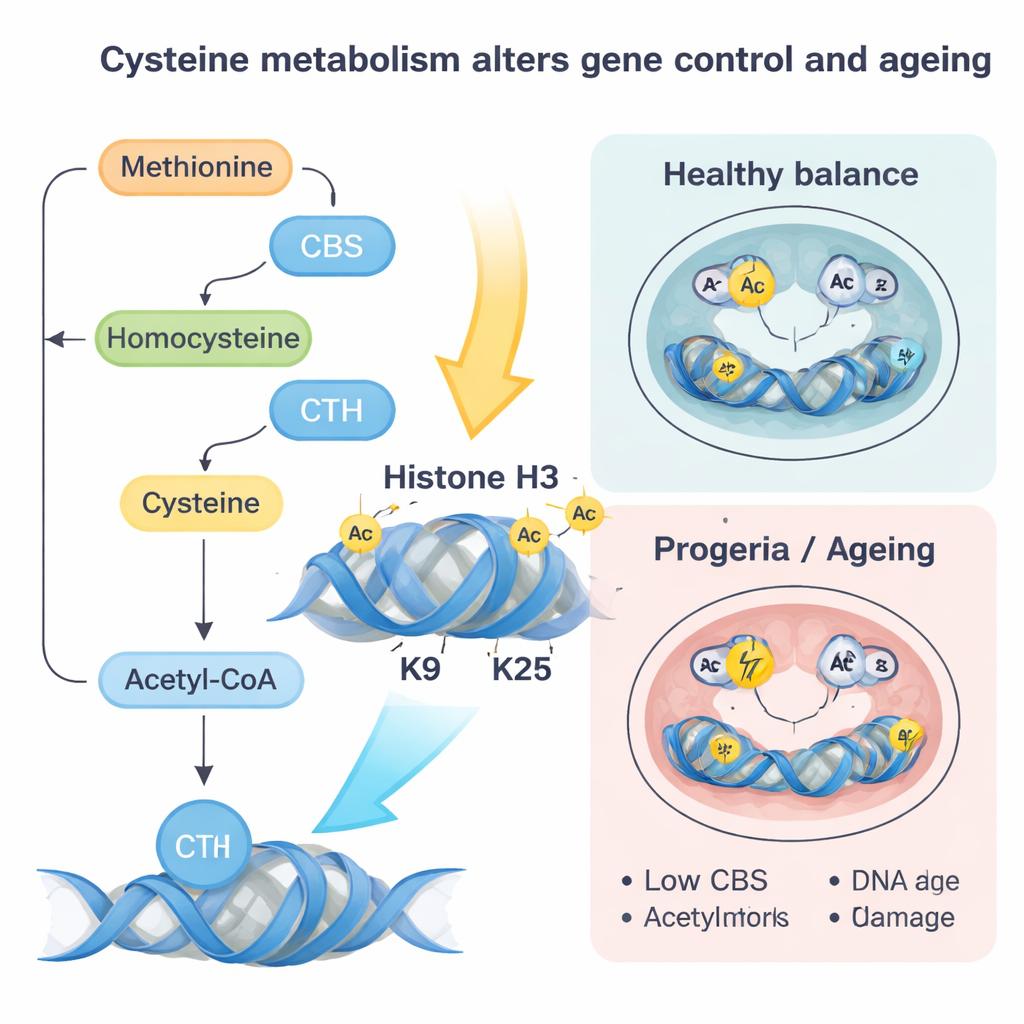
Metabolismo, marche sul DNA e invecchiamento precoce
La mutazione laminica simile alla progeria ha raccontato una storia complementare. Qui, i livelli di CBS e CTH diminuiscono, riducendo il flusso di cisteina e la produzione di acetil‑CoA da questa via. Allo stesso tempo, l’omocisteina viene rimandata nel ciclo della metionina, aumentando i livelli di SAM, il donatore universale di gruppi metile. Questo favorisce l’aggiunta di marchi metilici repressivi, soprattutto una modifica chiamata H3K9me3 posta dall’enzima SUV39H1, che compatta la cromatina ed è legata a una riparazione del DNA compromessa. Gli autori hanno mostrato che ripristinare moderatamente CBS o limitare la metionina abbassa SAM, riduce questi marchi metilici repressivi, migliora la riparazione del DNA, diminuisce lo stress ossidativo e i marcatori di senescenza, e in parte recupera la differenziazione verso cellule cardiache. Calo simile di CBS e aumento di marchi repressivi sono stati osservati in cuori di topo invecchiati naturalmente e in fibroblasti umani di persone anziane e pazienti con progeria, suggerendo che questo circuito opera anche nell’invecchiamento naturale.
Cosa significa per la salute e l’invecchiamento
Per un lettore non specialista, il messaggio è che l’impalcatura strutturale della cellula e il suo metabolismo sono strettamente connessi: quando il guscio nucleare fatto di lamin A/C è alterato, cambia il modo in cui la cisteina viene utilizzata, e questo riscrive a sua volta i marchi chimici sulle proteine che confezionano il DNA. Questi marchi decidono quali geni si attivano mentre le cellule staminali costruiscono il corpo e influenzano quanto bene le cellule riparano i danni nel corso della vita. Modulando con cura enzimi come CBS e CTH — o regolando l’apporto di nutrienti come metionina e cisteina — potrebbe essere possibile correggere parte della scrittura erronea di questi marchi nelle malattie legate alla lamina e forse attenuare aspetti dell’invecchiamento precoce o normale.
Citazione: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
Parole chiave: cellule staminali, lamina nucleare, metabolismo della cisteina, epigenetica, invecchiamento