Clear Sky Science · it
ABEL-FRET colma il divario temporale nelle misure a singola molecola della dinamica strutturale nel recettore A2A dell’adenosina
Osservare piccoli interruttori cellulari in tempo reale
Molti dei farmaci odierni agiscono attivando o disattivando dei “interruttori” molecolari sulla superficie cellulare, detti recettori. Questi interruttori cambiano continuamente forma mentre accendono e spengono i segnali, ma la maggior parte degli strumenti riesce a cogliere solo i movimenti più rapidi oppure quelli molto lenti — non entrambi. Questo studio presenta un metodo per osservare un singolo recettore bersaglio farmacologico in soluzione per molto più tempo rispetto al passato, rivelando come esso persista in conformazioni particolari che sono cruciali per l’azione dei farmaci.
Perché questi proteine che cambiano forma sono importanti
Lo studio si concentra su una grande classe di proteine di superficie note come recettori accoppiati alle proteine G, o GPCR. Queste proteine controllano processi vitali come la vista, l’umore, la pressione sanguigna e le risposte immunitarie; oltre un terzo dei farmaci approvati agisce su di esse. Un membro ben studiato, il recettore A2A dell’adenosina, contribuisce a regolare sonno, dolore, infiammazione e segnalazione cerebrale, ed è un promettente bersaglio per trattare disturbi come il morbo di Parkinson e il cancro. I GPCR sono molto flessibili: quando si legano molecole diverse, il recettore viene spinto in conformazioni distinte che favoriscono alcune vie di segnalazione rispetto ad altre. Proprio questa flessibilità rende però difficile progettare farmaci basandosi su istantanee statiche ottenute con raggi X o criomicroscopia elettronica.
Seguire un singolo recettore senza immobilizzarlo
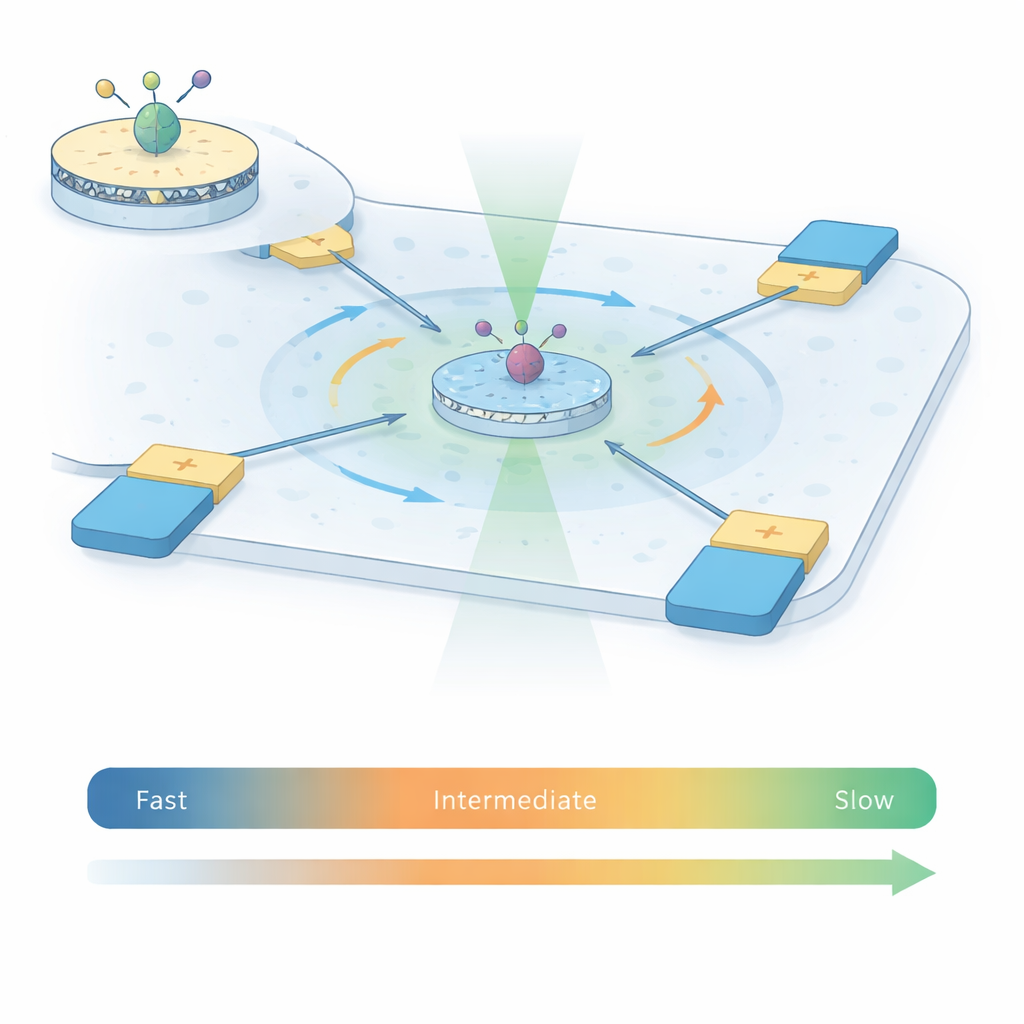
Per catturare come si muove il recettore A2A, gli autori combinano due tecniche potenti in ciò che chiamano ABEL‑FRET. Innanzitutto, ricostituiscono singoli recettori in piccole porzioni di membrana artificiale chiamate nanodischi, offrendo a ciascuna proteina un ambiente più naturale rispetto al solo detergente. Legano una coppia di coloranti fluorescenti a due parti mobili all’interno del recettore. Quando il recettore cambia forma, la distanza e l’orientamento relativo fra questi coloranti variano, modificando il trasferimento di energia fra loro — un fenomeno noto come Förster resonance energy transfer (FRET). In secondo luogo, invece di fissare il recettore su una superficie, usano una trappola elettrocinética anti‑Browniana (ABEL): una camera microfluidica con elettrodi che rilevano la posizione di una particella fluorescente e la spingono delicatamente verso il centro, contrastando il moto browniano casuale.
Colmare la finestra temporale mancante
Gli esperimenti tradizionali di FRET a singola molecola osservano recettori in diffusione libera per pochi millesimi di secondo, oppure recettori immobilizzati su una superficie per secondi o minuti. Ogni approccio copre una diversa finestra temporale. Utilizzando la trappola ABEL, questo lavoro mantiene singoli recettori A2A in vista per uno o due secondi mentre restano liberi in soluzione, circa 100 volte più a lungo rispetto agli esperimenti limitati dalla diffusione. Questo tempo di osservazione prolungato permette al team di misurare come il segnale FRET fluttui all’interno di ogni burst intrappolato e attraverso migliaia di recettori, in quattro condizioni: senza ligando, con un antagonista e con due diversi attivatori (agonisti). Strumenti statistici presi dall’analisi dei segnali — varianza, correlazione e analisi di ricorrenza — consentono di distinguere il rumore fotonico casuale da veri e propri cambiamenti strutturali lenti nel recettore.
Forme nascoste e durature rivelate
Le letture FRET mostrano che i recettori occupano molteplici conformazioni distinte che non si interconvertono completamente durante i tempi di osservazione tipici di qualche centinaio di millisecondi. In tutte le condizioni, la distribuzione dei valori di FRET è molto più ampia di quanto ci si aspetterebbe dal solo rumore, rivelando eterogeneità strutturale: molecole diverse stazionano in conformazioni diverse e di lunga durata. Quando si legano molecole attivanti, il livello medio di FRET si sposta verso l’alto, indicando che il recettore trascorre più tempo in un arrangiamento interno delle eliche simile allo stato attivo. Tuttavia, anche in tali condizioni, le analisi di correlazione mostrano che una volta che un recettore è in uno stato di FRET alto o intermedio ha una forte probabilità di rimanervi per almeno centinaia di millisecondi. Questi risultati aggiornano stime precedenti basate su esperimenti più rapidi, estendendo i tempi caratteristici di permanenza negli stati di lunga durata da pochi millisecondi a ben oltre un decimo di secondo.
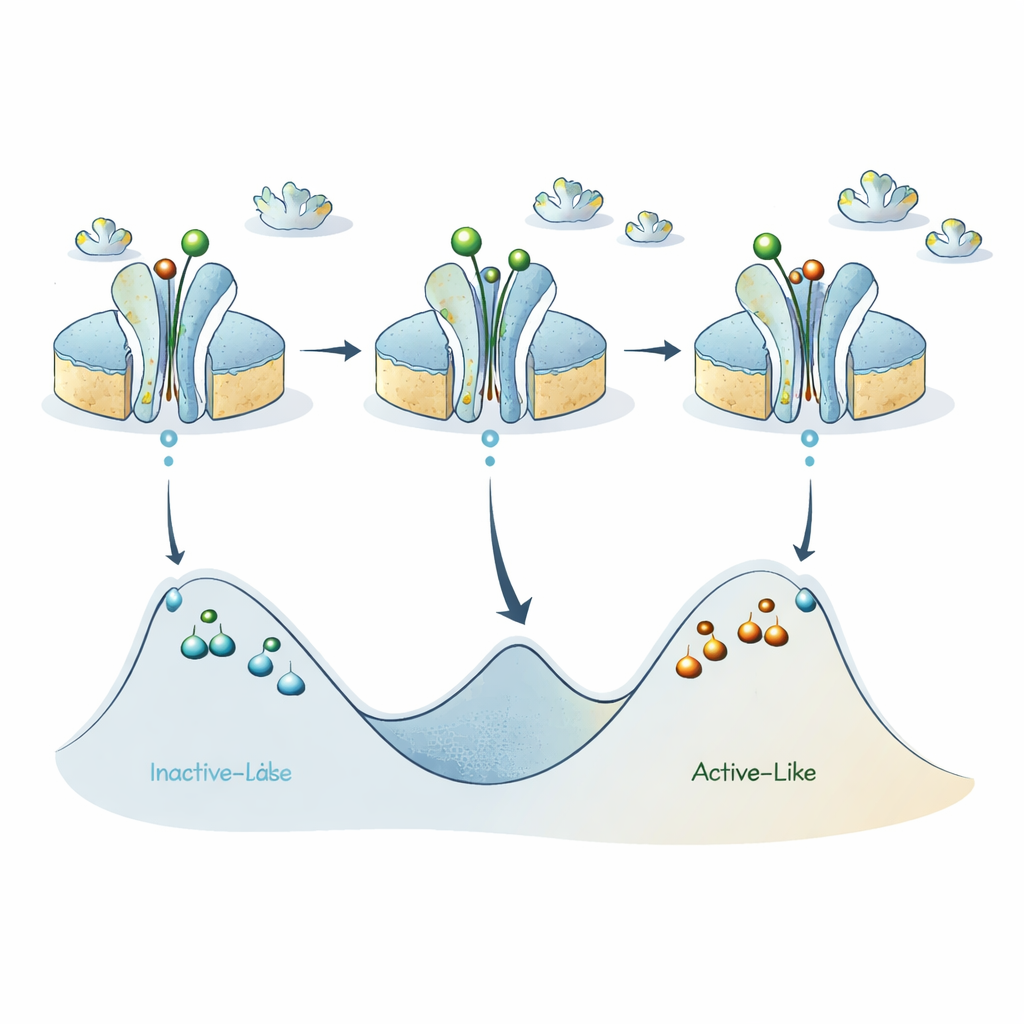
Una nuova mappa del paesaggio energetico del recettore
Mettendo insieme questi elementi, gli autori affinano un modello precedente secondo cui il recettore A2A oscilla principalmente tra uno stato simile all’inattivo e uno simile all’attivo. I nuovi dati suggeriscono che ciascuna di queste due categorie ampie nasconde in realtà diversi sottostati separati da barriere energetiche rilevanti, per cui singoli recettori possono rimanere “bloccati” in una specifica versione dello stato attivo‑like o inattivo‑like per tempi sorprendentemente lunghi. I ligandi attivanti abbassano la barriera tra i principali bacini inattivo‑like e attivo‑like, favorendo cambi rapidi su scala sub‑millisecondo, ma le barriere interne a ciascun bacino rimangono elevate, dando origine ai sottostati di lunga durata che ABEL‑FRET rileva.
Cosa significa questo per i futuri farmaci
Per i non specialisti, il messaggio chiave è che un bersaglio farmacologico come il recettore A2A non si limita a passare semplicemente da “spento” a “acceso”. Piuttosto, esplora un paesaggio irregolare di conformazioni, alcune delle quali persistono abbastanza a lungo da influenzare il modo in cui i segnali vengono trasmessi all’interno delle cellule e l’effetto dei farmaci nel tempo. Estendendo la durata durante la quale singoli recettori possono essere osservati nel loro stato naturale e non vincolato, ABEL‑FRET colma un divario cruciale tra misure ultraveloci e molto lente. Questo approccio può ora essere applicato a molte proteine di membrana, offrendo un quadro temporale più completo di come i potenziali bersagli farmacologici si aprono, si spostano e rispondono ai composti terapeutici.
Citazione: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
Parole chiave: Recettori accoppiati alle proteine G, FRET a singola molecola, recettore dell’adenosina A2A, dinamica conformazionale delle proteine, trappola ABEL