Clear Sky Science · it
Studio meccanicistico sulla migrazione del solfato nei glicosaminoglicani durante la frammentazione MS
Perché lo spostamento di marcatori chimici sugli zuccheri conta
Le nostre cellule sono rivestite da lunghe catene di zuccheri che aiutano a controllare processi che spaziano dalla coagulazione del sangue alla difesa immunitaria, fino al modo in cui i virus si agganciano alle cellule. Molte di queste catene portano piccole marcature chimiche chiamate gruppi solfato il cui posizionamento preciso lungo lo scheletro zuccherino funziona come un codice molecolare, indicando alle proteine quando e dove legarsi. Gli scienziati si affidano molto alla spettrometria di massa, una tecnica potente per pesare le molecole, per leggere questi codici. Questo studio rivela che durante tali misurazioni i gruppi solfato possono spostarsi silenziosamente di posizione, potenzialmente inducendo in errore i ricercatori sulla reale struttura di questi zuccheri biologicamente cruciali.
Catene zuccherine complesse con marcature critiche
I glicosaminoglicani sono lunghe catene lineari di zuccheri spesso attaccate a proteine sulla superficie cellulare. Le loro decorazioni sulfato non sono casuali; lievi variazioni nella posizione di un gruppo solfato su una specifica unità zuccherina possono alterare radicalmente l’interazione della catena con fattori di crescita, proteine della coagulazione o patogeni. Per questo motivo gli scienziati cercano di determinare non solo quanti solfati sono presenti ma esattamente dove sono collocati. La spettrometria di massa, spesso combinata con la rottura controllata delle catene zuccherine, è uno dei metodi principali per farlo. Tuttavia, indizi precedenti suggerivano che gruppi carichi come i solfati potrebbero spostarsi durante la misurazione, complicando gli sforzi per ricostruire il vero schema delle modifiche.
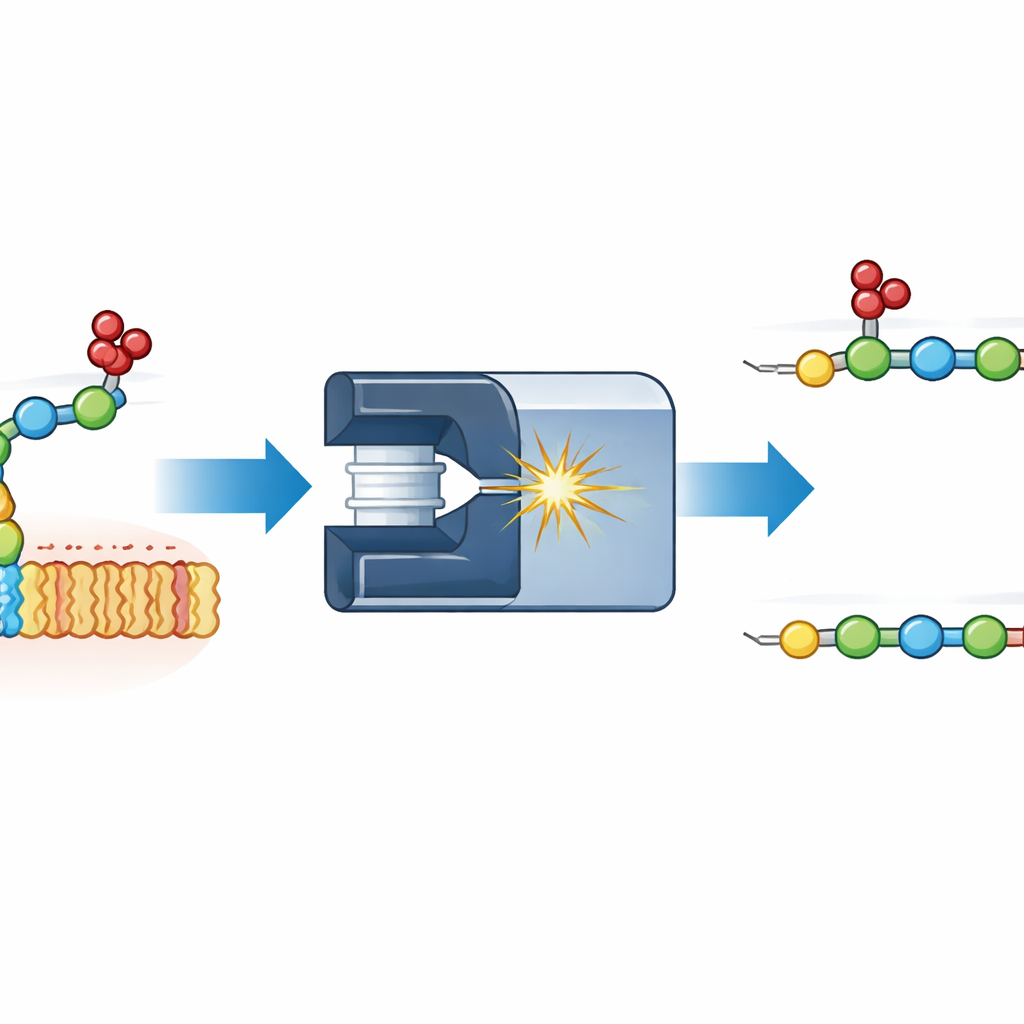
Osservare i solfati muoversi durante la misurazione
Gli autori si sono concentrati su un modello semplice: un frammento disaccaridico di eparan solfato, uno dei glicosaminoglicani più noti. Hanno attaccato diversi marcatori fluorescenti a un’estremità del disaccaride e lo hanno frammentato all’interno di uno spettrometro di massa. Misurando come i pezzi risultanti si spostavano attraverso un gas sotto un campo elettrico — una tecnica chiamata mobilità ionica — hanno potuto distinguere conformazioni che altrimenti avrebbero la stessa massa. È apparso un frammento inaspettato più pesante di esattamente un gruppo solfato nella posizione sbagliata: invece di rimanere sul primo zucchero, il solfato era migrato sul secondo. Confronti con composti di riferimento sintetizzati con cura hanno mostrato che il solfato migrante poteva posarsi in due punti distinti sul secondo zucchero, dando origine a due conformazioni diverse che la mobilità ionica ha risolto chiaramente.
Individuare i nuovi siti di atterraggio e testare i marcatori
Per comprendere meglio dove il solfato fosse finito e se altre posizioni fossero possibili, il team ha combinato le misure sperimentali con dettagliate simulazioni al computer. Hanno calcolato molte possibili forme tridimensionali per le strutture candidate e previsto come ciascuna dovrebbe comportarsi nella fase gassosa. Solo i solfati localizzati in due siti specifici sul secondo zucchero — noti agli specialisti come posizioni 6O e 3O — hanno corrisposto al comportamento sperimentale, mentre altre collocazioni ipotetiche sono sembrate improbabili. I ricercatori hanno quindi verificato se i marcatori stessi potessero favorire il rimescolamento, sostituendo il marcatore originale con tre marche più semplici. In ogni caso la migrazione del solfato è persista e ha prodotto frammenti simili, indicando che la scelta del marcatore ha scarso effetto sulla probabilità che la migrazione avvenga, sebbene possa influenzare sottilmente quanto sia facile distinguere i diversi prodotti.
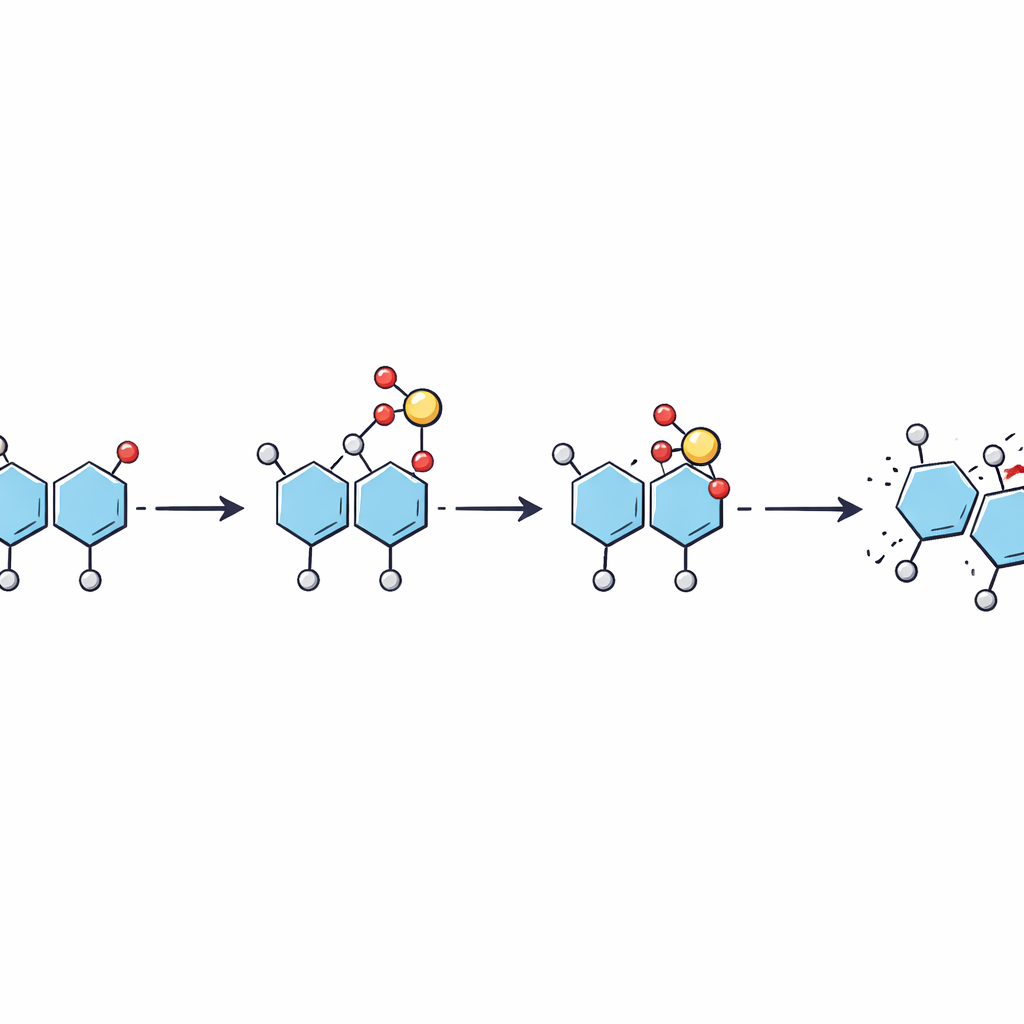
Saltare per gradi invece di un unico balzo
Utilizzando esperimenti di frammentazione a energia modulata insieme ad ulteriori simulazioni, gli autori hanno ricostruito un quadro graduale di come il solfato si muove. All’aumentare dell’energia dell’ione nello spettrometro di massa, un protone mobile attiva per primo il gruppo solfato, che poi salta dall zucchero originale su uno specifico sito dello zucchero vicino mentre il legame tra di essi si rompe. Questo produce un frammento in cui il solfato occupa una posizione intermedia. Con energia addizionale, il solfato può spostarsi di nuovo lungo lo stesso zucchero verso un sito più stabile. Il lavoro suggerisce che questi riarrangiamenti possono avvenire a energie inferiori rispetto a quelle necessarie per rompere lo scheletro zuccherino, il che significa che possono verificarsi silenziosamente durante le analisi di routine.
Cosa significa per decodificare le strutture zuccherine
Per i non specialisti, il messaggio chiave è che le marcature chimiche sugli zuccheri biologicamente rilevanti non sono sempre bloccate in posizione durante l’analisi; possono scivolare lungo la catena mentre la molecola vola attraverso lo spettrometro di massa. Lo studio mostra in dettaglio che, almeno per un frammento rappresentativo di eparan solfato, un gruppo solfato può migrare da un’unità zuccherina a un’altra e poi stabilizzarsi in nuove posizioni, producendo frammenti fuorvianti che imitano caratteristiche strutturali genuine. Ciò significa che alcune misurazioni passate e future potrebbero interpretare erroneamente il codice del solfato a meno che non vengano impiegate tecniche aggiuntive, come la mobilità ionica e la modellizzazione avanzata, per cogliere questi spostamenti nascosti. Il lavoro invita a studi più sistematici per capire quanto sia diffusa tale migrazione del solfato, in modo che i ricercatori possano collegare in modo più affidabile i modelli zuccherini sulla superficie cellulare alla salute e alla malattia.
Citazione: Polewski, L., Yaman, M., Tokić, M. et al. Mechanistic study on the sulfate migration in glycosaminoglycans during MS fragmentation. Commun Chem 9, 130 (2026). https://doi.org/10.1038/s42004-026-01939-2
Parole chiave: eparan solfato, glicosaminoglicani, spettrometria di massa, migrazione del solfato, mobilità ionica