Clear Sky Science · it
La profondità della posa di legame modula l’efficacia dei ligandi fotoswitchabili sul recettore 5-HT2A
Illuminare i farmaci cerebrali commutabili
Immagina un medicinale che puoi accendere e spegnere con un lampo di luce, dirigendo con precisione i recettori cerebrali ed evitando effetti collaterali. Questo studio esplora proprio quell’idea per un recettore chiave della serotonina collegato a umore, percezione e droghe psichedeliche. I ricercatori hanno indagato perché due molecole fotosensibili quasi identiche si comportano in modo così diverso: una agisce quasi come un interruttore perfetto on/off, l’altra si rifiuta ostinatamente di spegnersi completamente. La loro risposta si riduce a un fattore sorprendentemente semplice: quanto profondamente la molecola si inserisce all’interno del recettore.
Farmaci guidati dalla luce nel cervello
I farmaci attivati dalla luce, chiamati anche strumenti fotofarmacologici, sono progettati in modo che un fascio luminoso faccia ruotare parte della molecola tra due forme, per esempio una piegata e una raddrizzata. Quelle forme possono modificare quanto saldamente il farmaco si lega al suo bersaglio. In questo lavoro, il bersaglio è il recettore umano 5-HT2A, una proteina sulle cellule cerebrali che risponde alla serotonina ed è centrale sia per effetti antipsicotici sia psichedelici. Le molecole studiate sono derivati della N,N-dimetiltriptamina (DMT), modificati con un’unità azobenzene fotosensibile. Due versioni differiscono solo nella posizione di un piccolo gruppo metossile su un anello — in posizione “para” o “meta” — eppure il loro comportamento biologico sotto luce è drasticamente diverso.
Due molecole quasi gemelle, interruttori molto diversi
Nei test cellulari, la versione para, chiamata composto 1, si comporta quasi come un interruttore digitale. Al buio, la sua forma “trans” attiva appena il recettore e lo blocca perfino leggermente, agendo come un debole antagonista. Quando la luce la trasforma nella forma “cis”, la stessa molecola diventa un attivatore moderato, accendendo parzialmente il recettore. La versione meta, composto 2, rifiuta di cooperare in questo modo: entrambe le sue forme, luce e buio, mantengono il recettore abbastanza attivo, senza mai fornire un vero stato “off”. Il rompicapo centrale di questo lavoro è perché una modifica chimica così minima — spostare di poco un gruppo su un anello — cambi così fortemente la risposta del recettore.
Guardare dentro con filmati a livello atomico
Per risolvere il problema, il team ha usato estese simulazioni di dinamica molecolare all-atom, eseguendo di fatto filmati dettagliati di ogni atomo nel recettore, nella membrana circostante, nell’acqua e in ciascun ligando per un totale di circa 80 microsecondi. Hanno simulato entrambe le molecole in ciascuna delle loro forme controllate dalla luce, e nelle forme inattiva e attiva del recettore 5-HT2A. Seguendo noti “microswitch” strutturali all’interno della proteina — come un triptofano chiave che si capovolge, un ponte salino che si rompe, e il movimento di sodio e acqua nel nucleo profondo — hanno potuto dire quando il recettore tendeva verso uno stato off o on. Hanno inoltre confrontato quanto strettamente le nuove molecole imitassero la posa di legame dell’LSD, un parziale attivatore ben studiato, usando la sovrapposizione dei loro sistemi di anelli come guida.
La profondità conta più della sola forma
L’intuizione principale è che l’efficacia delle molecole è governata principalmente da quanto in profondità si inseriscono nella tasca di legame del recettore. Nel recettore inattivo, la forma trans del composto para forma una serie particolare di legami a idrogeno che la tirano in profondità, al di sotto della regione dove si stabiliscono di solito i contatti attivanti. Questa “iper-inserzione” le impedisce di raggiungere residui polari chiave che aiutano a commutare il recettore in modo attivo, perciò stabilizza lo stato spento. La trans del composto meta non può creare gli stessi ancoraggi e invece resta più in alto in una posa più simile a quella dell’LSD, compatibile con l’attivazione, spiegando la sua attività residua. Quando la luce converte entrambe le molecole nelle forme cis, esse si spostano in genere in posizioni più superficiali, più simili a quelle degli attivatori. Tuttavia anche qui la geometria è importante: nel recettore attivo, il cis del composto 2 può scivolare più in profondità in un tunnel idrofobico tra due eliche e formare un legame a idrogeno persistente che rinforza il suo comportamento da forte agonista, mentre il cis del composto 1 è stericamente impedito dal farlo.
Controllo fine di acqua e ioni interni
Le simulazioni mostrano inoltre che la profondità di legame regola sottilmente una tasca interna per il sodio e un percorso d’acqua noti per influenzare l’attivazione del recettore. Un legame profondo e rigido del composto para nella sua forma trans mantiene uno ione sodio strettamente intrappolato e la regione circostante relativamente secca, caratteristiche associate a uno stato off. Al contrario, il legame più mobile del composto meta o delle forme cis permette a più acqua di penetrare e allenta l’ambiente del sodio, preparando il recettore all’attivazione. Un residuo aromatico chiave che funge da “interruttore” può capovolgere la sua orientazione più facilmente quando i ligandi sono flessibili e non iper-ancorati, spingendo ulteriormente il recettore verso uno stato on, specialmente con il cis del composto 2.
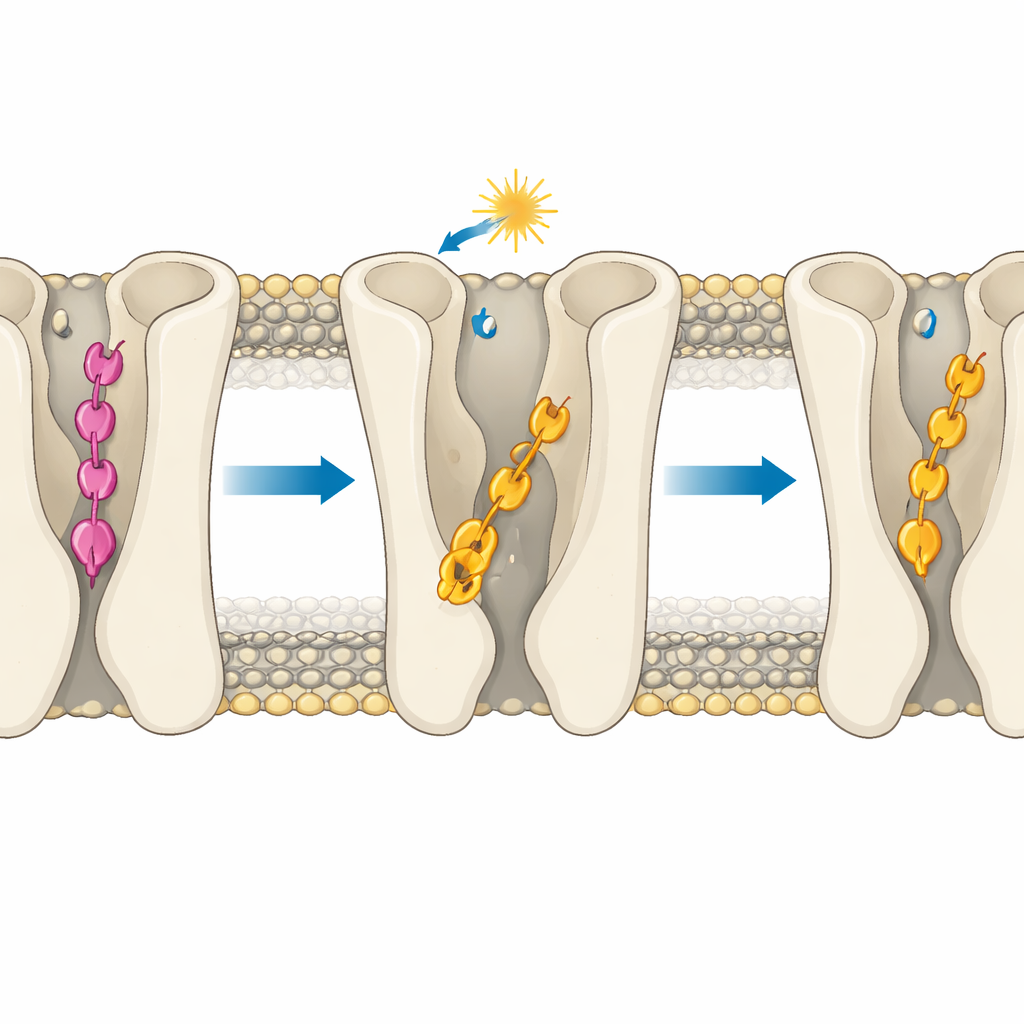
Regole di progettazione per futuri farmaci controllati dalla luce
Per un lettore non specialista, il messaggio è che la profondità esatta con cui un farmaco siede nella tasca del recettore può fare la differenza tra spento, parzialmente acceso e fortemente acceso — anche quando il cambiamento chimico sembra minuscolo sulla carta. Mostrando come un ligando fotoswitchabile possa iper-inserirsi e bloccare il recettore spento, mentre uno strettamente correlato si mantiene a una profondità favorevole all’attivazione, lo studio offre una regola di progettazione chiara: controllare la profondità di inserzione con la stessa cura con cui si controllano i cambiamenti di forma indotti dalla luce. Questi insight potrebbero guidare la creazione di composti fotosensibili di nuova generazione per trattare disturbi cerebrali con una precisione senza precedenti, modulando segnali biologici in modo controllato e reversibile riducendo al minimo gli effetti collaterali.
Citazione: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
Parole chiave: fotofarmacologia, recettore della serotonina 5-HT2A, ligandi fotoswitchabili, attivazione GPCR, simulazioni di dinamica molecolare