Clear Sky Science · it
Comportamento scaffold-client e organizzazione strutturale nei condensati proteici multicomponenti rivelati dallo studio delle goccioline tau/TDP-43
Proteine che si comportano come minuscole goccioline d’olio
All’interno delle nostre cellule molte proteine non rimangono uniformemente disperse nel fluido acquoso. Piuttosto, si aggregano in piccole goccioline liquide, un po’ come l’olio nell’acqua. Questo studio esamina come due di queste proteine, tau e TDP-43, strettamente collegate alla malattia di Alzheimer e ad altre demenze, si raggruppino insieme in goccioline. Svelando come queste goccioline si formano, si mescolano e si organizzano, il lavoro fornisce indizi sul perché compaiano aggregati proteici dannosi nel cervello che invecchia e su come potremmo un giorno controllarli.
Perché queste due proteine cerebrali sono importanti
Tau e TDP-43 sono entrambe note per formare aggregati tossici nelle malattie neurodegenerative. Tradizionalmente gli scienziati le hanno studiate separatamente, ma sempre più autopsie mostrano che entrambe le proteine possono ritrovarsi nelle stesse regioni danneggiate. Questo solleva una domanda centrale: quando tau e TDP-43 sono presenti insieme nelle cellule, come condividono lo spazio all’interno delle goccioline e questo ambiente condiviso favorisce l’aggregazione correlata alla malattia? Gli autori hanno scelto un modello semplificato ma realistico usando tau e la coda a bassa complessità di TDP-43 (LCD), la porzione più responsabile della formazione delle goccioline e della loro eventuale solidificazione.
Goccioline, “scaffold” e “client”
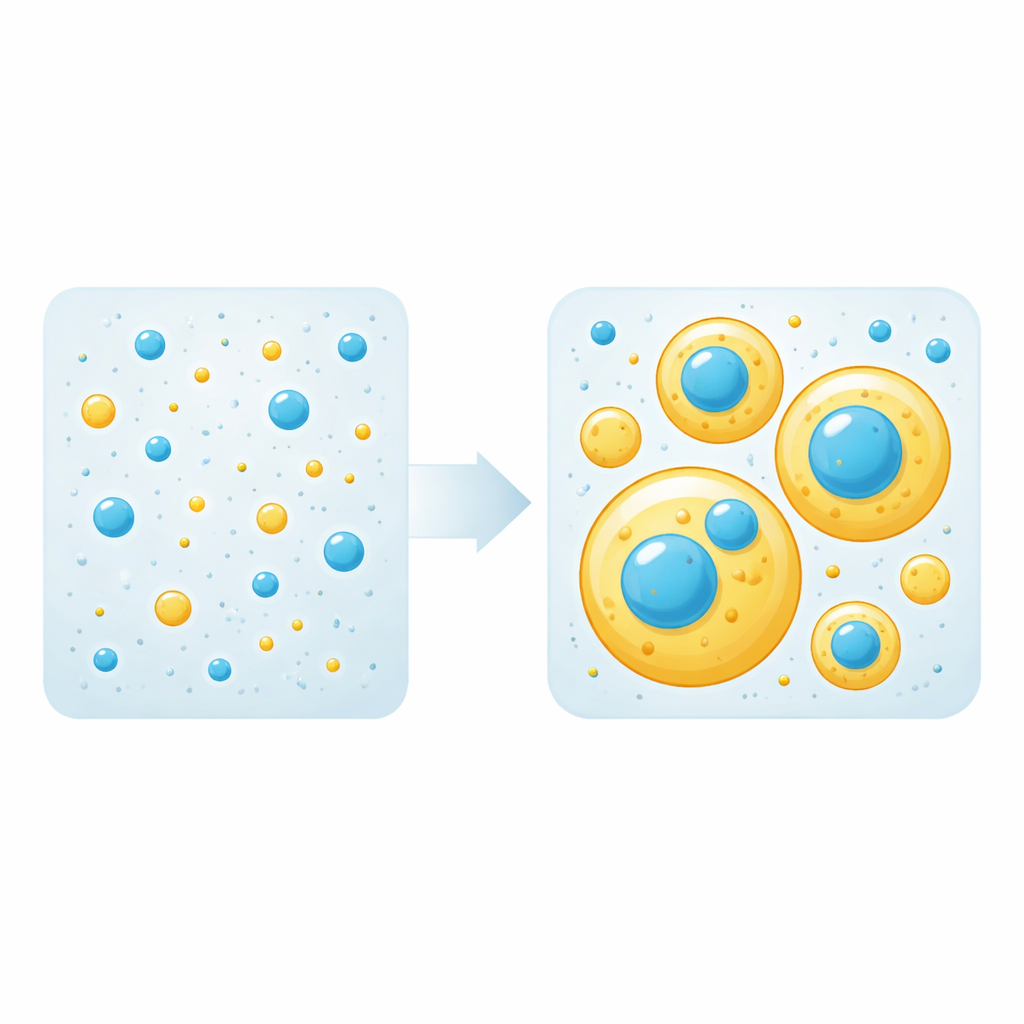
Goccioline liquide come queste si formano quando le attrazioni proteina–proteina superano quelle proteina–acqua, provocando la separazione della soluzione in una fase densa (goccioline) e una fase diluita. Nelle miscele, solo alcune proteine sono necessarie per costruire le goccioline; queste sono chiamate “scaffold”. Altre si limitano a farsi trasportare all’interno delle goccioline come “client”. Il gruppo ha prima misurato la soglia di concentrazione alla quale ciascuna proteina comincia da sola a formare goccioline. Poi ha miscelato diverse quantità di tau e TDP-43 LCD e osservato, con microscopìa a fluorescenza, se comparivano goccioline e come le proteine si disponevano. In modo sorprendente, hanno scoperto che ciascuna proteina può comportarsi da scaffold o da client a seconda unicamente della sua concentrazione: al di sopra della propria soglia costruisce goccioline, al di sotto viene reclutata passivamente nelle goccioline formate dall’altra.
Goccioline stratificate e un alone misterioso
Quando entrambe le proteine erano presenti in quantità sufficienti a formare goccioline da sole, non si mescolavano in una singola gocciolina uniforme. Invece, goccioline più grandi ricche di tau avvolgevano goccioline più piccole ricche di TDP-43, creando una struttura stratificata e multifase. Misurazioni di come le goccioline si estendono sul vetro hanno mostrato che le goccioline di TDP-43 hanno una tensione superficiale più alta, perciò è energeticamente favorevole che stiano all’interno delle goccioline tau più bagnanti. Emersa a queste interfacce c’è una caratteristica evidente: tau si accumulava a livelli particolarmente elevati come un brillante “alone” che rivestiva la superficie delle goccioline di TDP-43, anche quando tau stessa era al di sotto della propria soglia di formazione. Nel tempo, le regioni ricche di TDP-43 tendevano ad irrigidirsi diventando più simili a materiali solidi, mentre le regioni ricche di tau restavano liquide, suggerendo diverse propensioni a trasformarsi in aggregati di lunga durata.
Modulare le interazioni e sondare il meccanismo microscopico
Gli autori hanno poi testato come forze molecolari specifiche controllino quale proteina agisce da scaffold o da client. Hanno indebolito selettivamente le interazioni idrofobiche (che respingono l’acqua) che guidano la condensazione del TDP-43 LCD usando 1,6-esanediolo, e separatamente hanno attenuato le interazioni elettrostatiche (basate sulla carica) che guidano la condensazione di tau aumentando la salinità. In ciascun caso, disabilitare le interazioni chiave di una proteina le impediva di formare goccioline e la trasformava in client all’interno delle goccioline dell’altra, imitando ciò che accade quando la sua concentrazione viene diminuita. Per comprendere più a fondo l’alone, hanno variato la salinità per vedere quanto tau entrasse nelle goccioline di TDP-43 e hanno usato simulazioni al computer che trattano ogni amminoacido come una perlina semplificata. Queste simulazioni hanno riprodotto l’alone e mostrato che i primi ~40 amminoacidi della regione N-terminale carica negativamente di tau si ancorano alla superficie della gocciolina, mentre il resto della molecola si estende verso l’esterno nel liquido circostante, creando un involucro “anfifilico” (in parte amante della gocciolina, in parte amante dell’acqua). Esperimenti con un frammento di tau accorciato privo di questa porzione N-terminale hanno confermato che, senza di essa, l’alone scompare.

Cosa significa per le malattie cerebrali
Nel loro insieme, i risultati rivelano un insieme di regole generali su come si assemblano e si organizzano goccioline proteiche multicomponenti. In questo sistema tau/TDP-43, che rispecchia situazioni nei neuroni malati, concentrazione e forza delle interazioni determinano congiuntamente quali proteine costruiscono le goccioline e quali le occupano soltanto. Tensione superficiale e arrangiamenti anfifilici poi scolpiscono goccioline stratificate e aloni che possono concentrare più proteine legate alla malattia nello stesso spazio confinato, favorendo potenzialmente la loro indurimento in aggregati. Per un osservatore non esperto, il messaggio chiave è che tau e TDP-43 non si aggregano in modo casuale; si auto-organizzano in goccioline liquide strutturate la cui architettura è governata da semplici principi fisici. Capire e infine manipolare questi principi potrebbe aprire nuove strade per rallentare o prevenire l’accumulo proteico dannoso nelle malattie neurodegenerative.
Citazione: Monnaka, V.U., Shipley, B., Boyko, S. et al. Scaffold-client behavior and structural organization in multicomponent protein condensates as revealed by studying tau/TDP-43 droplets. Commun Chem 9, 126 (2026). https://doi.org/10.1038/s42004-026-01933-8
Parole chiave: condensati proteici, separazione di fase liquido-liquido, tau, TDP-43, neurodegenerazione