Clear Sky Science · it
Esplorare la stabilità di BOx su diversi supporti inorganici
Carburanti più puliti da un elemento comune
Trasformare il propano ordinario — quello nelle bombole del barbecue — in blocchi di valore superiore per la plastica richiede di solito processi ad alta temperatura e ad alto consumo energetico che producono anche molta anidride carbonica. Questo studio indaga come i composti del boro, un elemento relativamente abbondante, possano facilitare questa trasformazione in modo più dolce e pulito. Scoprendo come il boro si comporta su diverse superfici solide ad alte temperature, gli autori indicano nuove vie per progettare catalizzatori che producano sostanze utili con meno sprechi e minore consumo energetico.
Perché la chimica propano→plastica è importante
La vita moderna dipende fortemente da olefine leggere come il propene e l’etene, ingredienti chiave per plastiche, fibre e innumerevoli materiali di uso quotidiano. Oggi la maggior parte di questi composti viene prodotta da petrolio o gas naturale tramite processi energivori che rilasciano grandi quantità di CO₂. Un processo alternativo, chiamato deidrogenazione ossidativa del propano, può in linea di principio generare queste olefine a temperature più basse e con meno sottoprodotti indesiderati. I materiali a base di boro sono recentemente emersi come catalizzatori promettenti per questa reazione perché sono altamente selettivi: favoriscono la trasformazione del propano in olefine invece di ossidarlo completamente a CO₂. Tuttavia i ricercatori non comprendono ancora pienamente quale sia la specie di boro “attiva” né dove avvenga esattamente la reazione — sulla superficie del catalizzatore, in fase gassosa o in entrambi i luoghi.
Sorpresa: il boro è mobile nei reattori caldi
Gli autori si sono concentrati sull’ossido di boro, un semplice composto boro‑ossigeno spesso indicato come BOx, supportato su tre materiali inorganici comuni: silice pura, allumina pura e una miscela silice–allumina. Usando una combinazione di tecniche che tracciano i gas rilasciati dalla superficie durante il riscaldamento e metodi che sondano la struttura locale degli atomi nei solidi, hanno dimostrato che il boro non resta sempre fisso. Sulla silice, l’ossido di boro tende a formare aggregati debolmente legati che possono evaporare, creando specie volatili contenenti boro nel flusso gassoso. Su supporti ricchi di allumina, invece, il boro si lega più strettamente agli atomi di ossigeno legati all’alluminio, formando una rete più stabile, simile a un vetro, che resiste al distacco in fase gassosa. Semplici test di lavaggio hanno confermato questo quadro: la maggior parte del boro poteva essere risciacquata via dai campioni su silice, ma molto meno da quelli a base di allumina.
Collegare la stabilità del boro al comportamento catalitico
Queste differenze nella mobilità del boro si sono rivelate strettamente correlate al comportamento dei catalizzatori nella reazione sul propano. L’ossido di boro su silice ha iniziato a convertire il propano in olefine a temperature circa 80 °C più basse rispetto ai catalizzatori contenenti allumina, anche se tutti e tre i sistemi mostravano alla fine relazioni molto simili tra conversione del propano e selettività verso le olefine. Riscaldando i campioni e monitorando i frammenti contenenti boro nella fase gassosa è emerso che la silice rilasciava molto più ossido di boro e specie correlate alle temperature di reazione rispetto all’allumina. Ciò suggerisce che supporti che consentono al boro di sfuggire più facilmente possono attivare la reazione prima, perché più intermedi reattivi contenenti boro entrano in fase gassosa dove possono avviare catene reattive che trasformano il propano.
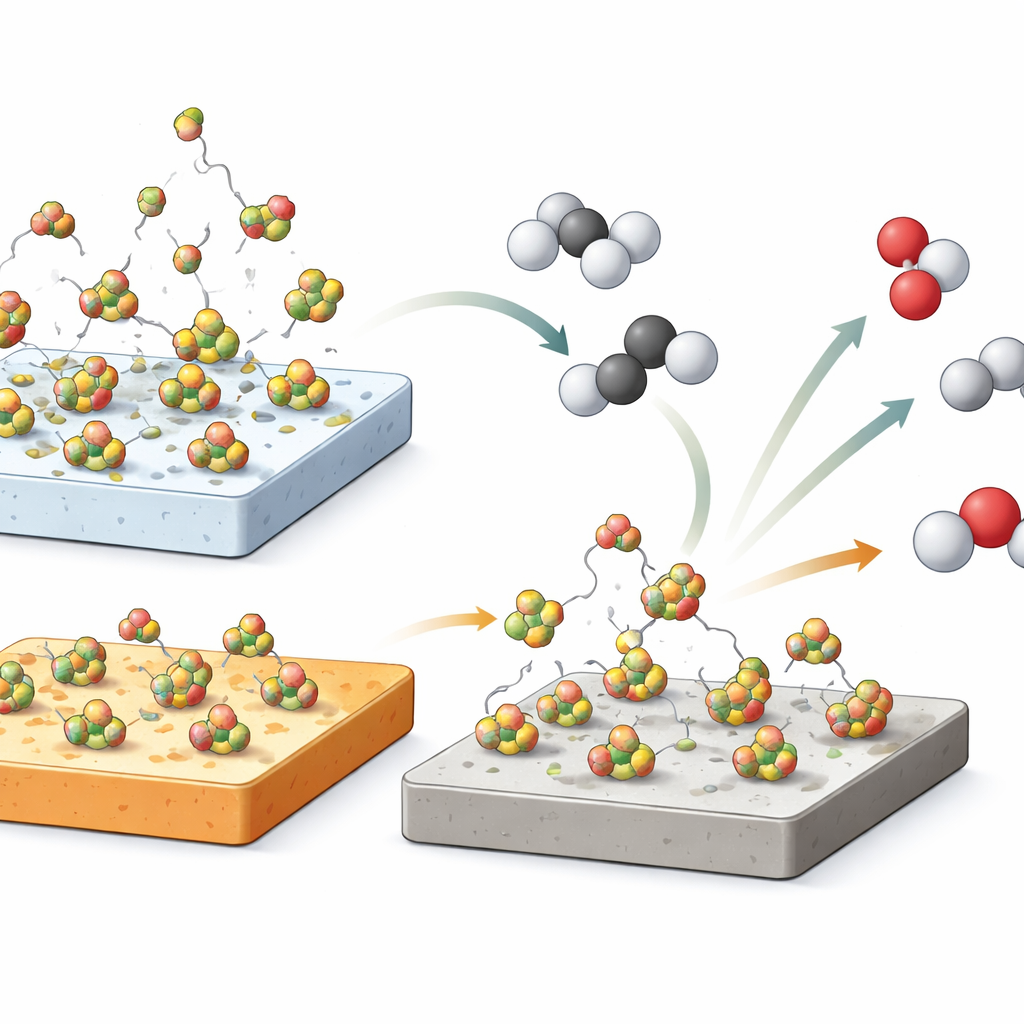
Il boro in fase gassosa come assistente invisibile
Per verificare se il boro presente solo in fase gassosa potesse guidare la chimica, i ricercatori hanno eseguito un esperimento notevole: hanno rimosso completamente il catalizzatore solido e hanno semplicemente iniettato un minuscolo impulso di soluzione di acido borico, equivalente a circa un settantesimo del boro normalmente presente su un catalizzatore, direttamente in un reattore vuoto e caldo. Quando la soluzione si è rapidamente decomposta in ossido di boro a 500 °C, la conversione del propano è aumentata di circa il 20%, con una selettività alle olefine simile a quella osservata sui catalizzatori solidi. Un test di controllo con sola acqua ha prodotto solo un effetto piccolo e di breve durata. Insieme alle misure di desorbimento, questo risultato indica con forza che specie volatili di boro in fase gassosa giocano un ruolo importante, probabilmente avviando catene radicaliche che trasformano il propano in propene ed etene.
Cosa significa questo per i catalizzatori futuri
Per i non specialisti, la conclusione principale è che il supporto solido sotto un catalizzatore a base di boro non è solo un’impalcatura inerte: controlla attivamente quanto boro può sfuggire in fase gassosa e, con esso, quanto facilmente la reazione si avvia. Supporti come la silice, che rilasciano il boro più facilmente, portano all’attivazione del propano a temperature più basse, mentre i supporti ricchi di allumina trattengono il boro più saldamente e richiedono temperature più alte, anche se tutti arrivano a selettività di prodotto simili una volta che la reazione è avviata. Questa intuizione suggerisce che tarare con cura quanto fortemente il boro è ancorato al supporto potrebbe permettere ai chimici di progettare catalizzatori che bilanciano stabilità e attività, abilitando vie più pulite ed efficienti in termini di energia per trasformare combustibili semplici come il propano nelle molecole che sostengono i materiali moderni.
Citazione: Johánek, V., Wróbel, M., Knotková, K. et al. Exploring the stability of BOx at various inorganic supports. Commun Chem 9, 116 (2026). https://doi.org/10.1038/s42004-026-01926-7
Parole chiave: catalizzatori a ossido di boro, deidrogenazione ossidativa del propano, chimica radicalica in fase gassosa, supporti di silice e allumina, produzione di olefine