Clear Sky Science · it
Cristallizzazione innescata dalla diffusione di massa a una supersaturazione locale inferiore
Perché questo conta oltre il laboratorio
I cristalli di sale possono sembrare banali, ma il modo in cui si formano ha conseguenze enormi — da come vengono prodotti i farmaci a come recuperiamo risorse da acque di scarto saline. Questo studio rivela che i cristalli possono iniziare a formarsi prima, e in punti diversi, quando il liquido viene delicatamente portato fuori equilibrio da gradienti di temperatura e concentrazione. Comprendere questo comportamento sottile potrebbe aiutare a progettare modi più puliti e meno costosi per gestire le salamoie, produrre materiali migliori e controllare l’incrostazione indesiderata in tubazioni e impianti.

Come i cristalli nascono di solito
La cristallizzazione avviene quando una sostanza disciolta, come il cloruro di potassio (KCl) in acqua, supera la quantità che può rimanere comodamente in soluzione. Questo stato è chiamato supersaturazione. Le teorie classiche dicono che i cristalli appaiono solo quando la supersaturazione è sufficientemente alta da superare una barriera energetica e che la nucleazione dovrebbe iniziare dove la soluzione è più supersatura. In ambito industriale, le soluzioni vengono solitamente portate in questo stato raffreddandole, facendo evaporare il solvente o aggiungendo un “antisolvente”. In queste condizioni convenzionali, quasi uniformi, i ricercatori hanno tracciato una zona metastabile — una finestra in cui il liquido è supersaturo ma non si sono ancora formati cristalli visibili.
Tre modi diversi per far cristallizzare lo stesso sale
Gli autori hanno esaminato come compaiono i cristalli di KCl in tre scenari controllati all’interno di una cella piana costruita su misura con controllo termico separato in alto e in basso. Per prima cosa hanno eseguito esperimenti di raffreddamento standard, abbassando uniformemente la temperatura da 20 °C e osservando quando apparivano i primi cristalli. Questo ha stabilito un confine di riferimento nella mappa concentrazione–temperatura: sotto una certa temperatura i cristalli si formavano sempre; sopra di essa la soluzione restava priva di cristalli per ore. Hanno poi confrontato questo riferimento con due situazioni più complesse in cui la soluzione sperimentava un trasporto di massa direzionale invece del semplice raffreddamento uniforme.
Quando il calore spinge il sale a muoversi
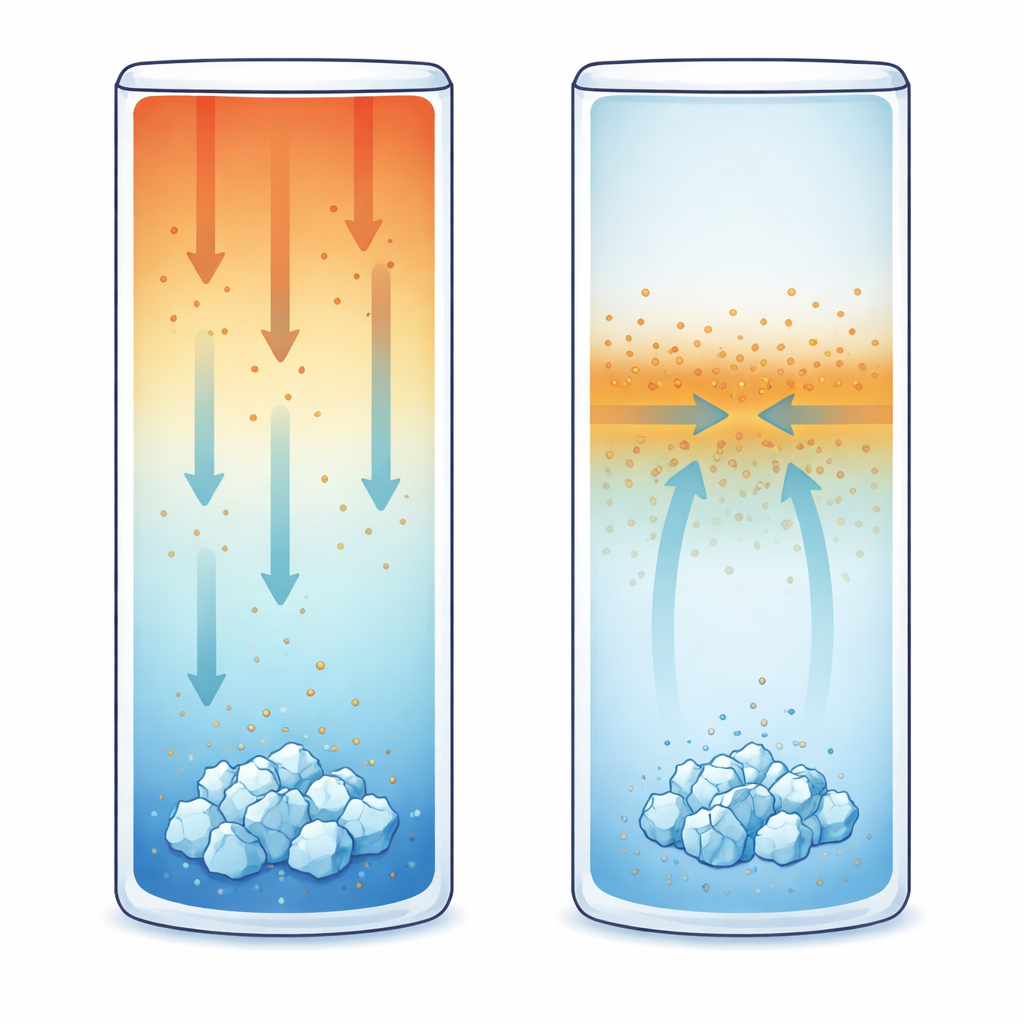
Nel secondo gruppo di esperimenti la soluzione partiva dalla stessa composizione ma veniva mantenuta con la parte superiore a 20 °C e la parte inferiore raffreddata a 15 °C. Questo gradiente di temperatura verticale causa la termodiffusione, cioè gli ioni disciolti migrano in risposta alla temperatura, non solo alla concentrazione. Per il KCl nell’intervallo testato il comportamento è termofobico: gli ioni tendono a spostarsi verso la regione più fredda, accumulando più sale in prossimità del fondo. Utilizzando un metodo ottico sensibile chiamato interferometria a sfasamento di fase, i ricercatori hanno seguito piccole variazioni dell’indice di rifrazione che rivelano come evolvono concentrazione e temperatura. Hanno constatato che i cristalli si formavano costantemente sulla parete inferiore fredda, nelle regioni dove il gradiente di concentrazione era più ripido — eppure la supersaturazione locale lì era leggermente inferiore rispetto al caso di raffreddamento uniforme. In altre parole, la presenza di un flusso di massa sostenuto ha permesso alla cristallizzazione di iniziare prima del previsto.
Quando il sale diffonde a temperatura perfettamente uniforme
Il terzo scenario ha eliminato del tutto le differenze di temperatura. L’intera cella è stata mantenuta a 17 °C uniformi, inizialmente riempita con la soluzione di riferimento. Poi è stato iniettato delicatamente da un angolo superiore un piccolo volume di soluzione di KCl più diluita, creando un netto contrasto di concentrazione ma quasi nessuna turbolenza del fluido. La diffusione ha quindi attenuato questo contrasto mentre gli ioni migravano dalla regione più concentrata a quella più diluita. Anche in questo caso l’interferometria ha rivelato come il campo di concentrazione si è evoluto nel tempo. Sorprendentemente, i primi cristalli visibili non sono apparsi dove la soluzione era più supersatura. Si sono formati invece approssimativamente a metà altezza della cella, vicino all’interfaccia dove il gradiente di concentrazione — e quindi il flusso diffusivo di massa — era più intenso.
Cosa significa per teoria e tecnologia
Attraverso tutti e tre i metodi — raffreddamento, termodiffusione e diffusione isoterma — i primi cristalli comparsi erano molto simili: per lo più cristalli cubici di KCl con forme di crescita familiari. Ciò che cambiava non era la struttura cristallina ma le condizioni che ne hanno innescato la nascita. Sotto flussi di massa imposti, i cristalli sono comparsi a una supersaturazione locale più bassa e in posizioni governate dai gradienti piuttosto che dai picchi di concentrazione. Questo suggerisce che il traffico molecolare direzionale nel liquido può aiutare gli ioni ad allinearsi in zone dense che fungono da nuclei precoci, restringendo di fatto la zona metastabile. Sebbene la teoria classica della nucleazione non possa spiegare completamente questo comportamento, le idee più recenti sulla nucleazione a più stadi sono coerenti con i risultati. Dal punto di vista pratico, il lavoro indica la possibilità di controllare in modo più intelligente la cristallizzazione in processi come la desalinizzazione a zero scarico liquido, dove sfruttare la termodiffusione potrebbe aiutare a trasformare le salamoie di scarto in sali solidi con meno energia e meno prodotti chimici.
Citazione: Xu, S., Torres, J.F. Crystallisation triggered by mass diffusion at a lower local supersaturation. Commun Chem 9, 125 (2026). https://doi.org/10.1038/s42004-026-01925-8
Parole chiave: cristallizzazione, termodiffusione, supersaturazione, desalinizzazione, trasporto di massa