Clear Sky Science · it
Effetti sinergici tra cationi e faccette potenziano la cinetica dell’evoluzione dell’idrogeno in ambiente alcalino su superfici di Pt a gradini
Perché è importante per l’energia pulita
Produrre idrogeno pulito dall’acqua è un elemento chiave di molti piani per raggiungere emissioni nette zero, ma i dispositivi più pratici oggi sprecano energia perché la reazione che genera le bolle di idrogeno può essere sorprendentemente lenta in soluzioni alcaline (basiche). Questo studio scende fino al livello di singoli atomi e molecole d’acqua per spiegare perché alcune superfici di platino funzionano meglio di altre e come ioni comuni disciolti nel liquido possano collaborare con la superficie metallica per accelerare la produzione di idrogeno.
Modellare le superfici del metallo per guidare l’acqua
I ricercatori si concentrano sul platino, il materiale di riferimento per scindere l’acqua, e confrontano due tipi di paesaggi atomici sulla sua superficie. Uno è piatto, come una terrazza liscia (chiamata Pt(111)); l’altro è a gradini, come una piccola scala (Pt(311)). Utilizzando sofisticate simulazioni quantomeccaniche che includono sia gli elettroni sia le molecole d’acqua in movimento, modellano il comportamento di queste diverse superfici a tensioni operative realistiche in un elettrolizzatore alcalino. L’obiettivo è capire come l’ambiente locale immediatamente accanto al metallo — dove acqua, ioni ed elettroni si incontrano — controlli la velocità del primo passo nella formazione dell’idrogeno.
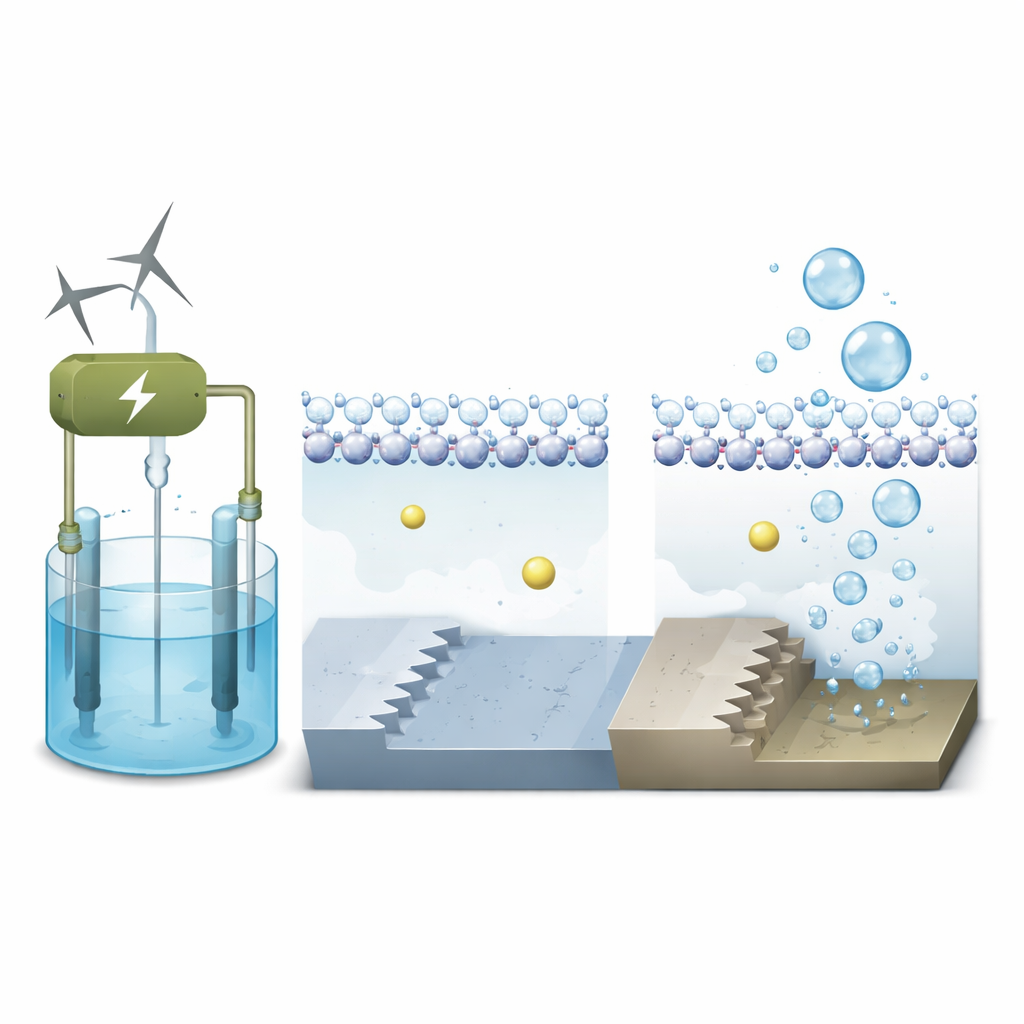
Gli ioni salini come aiutanti nascosti
Negli elettrolizzatori alcalini il liquido contiene ioni di metalli alcalini come il sodio. Questi ioni carichi positivamente fanno più che galleggiare: possono raggrupparsi vicino all’elettrodo e rimodellare sottilmente il campo elettrico all’interfaccia. Le simulazioni mostrano che sulla terrazza piatta di platino l’acqua forma uno strato compatto e ordinato con gli atomi di idrogeno rivolti verso la superficie carica negativamente. Gli ioni sodio rimangono più lontani, separati dal metallo da questo foglio d’acqua, perciò la loro influenza sulla reazione è modesta. Sulla superficie a gradini, invece, gli atomi sottocoordinati al bordo del gradino legano l’acqua più fortemente e creano una struttura d’acqua locale più irregolare e disordinata.
Un cluster vicino alla superficie che avvicina gli ioni
In corrispondenza di questi bordi a gradino, il gruppo scopre un motivo strutturale ricorrente: una molecola d’acqua legata direttamente al gradino di platino che, a sua volta, trattiene un vicino ione sodio circondato da ulteriori molecole d’acqua. Questo compatto cluster platino–acqua–sodio effettivamente trascina l’ione di circa 2,3 angstrom più vicino al metallo rispetto alla superficie piatta. Essere più vicino rafforza molto il campo elettrico locale in questa piccola regione, che polarizza fortemente le molecole d’acqua vicine. Le simulazioni rivelano che uno dei legami O–H in queste molecole d’acqua si allunga più del normale, indicando che è parzialmente avviato verso la rottura ancora prima che la reazione proceda formalmente.
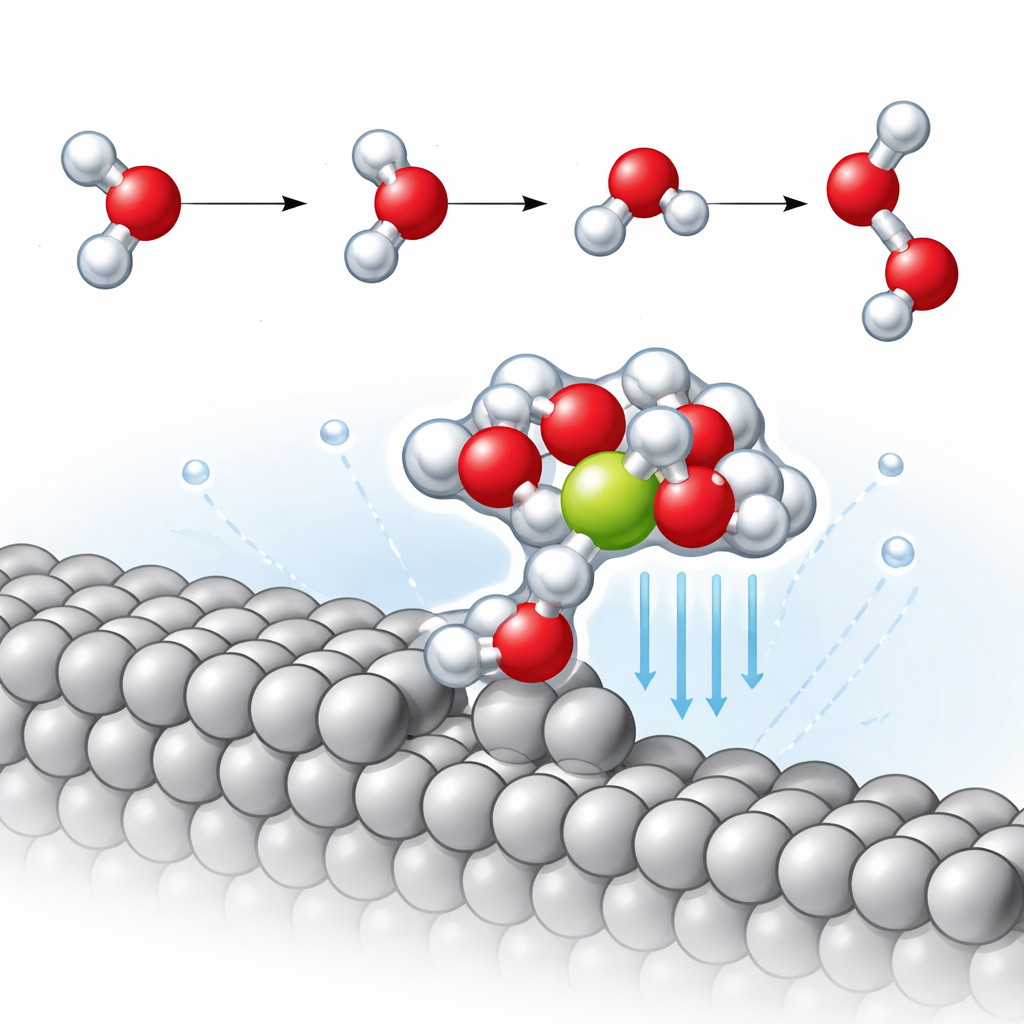
Abbassare la barriera per formare idrogeno
Il passaggio lento chiave nell’evoluzione dell’idrogeno in ambiente alcalino è noto come passo di Volmer, in cui una molecola d’acqua si scinde: l’idrogeno si lega al metallo mentre l’idrossido rimanente si allontana nel liquido. Tracciando il percorso di reazione a minima energia, gli autori trovano che sulla superficie piatta di platino il sodio ha solo un piccolo effetto sulla barriera energetica per questo passo. Al contrario, sulla superficie a gradini il cluster stabilizzato dal sodio nelle vicinanze riduce l’energia di attivazione di circa 0,14 elettronvolt — approssimativamente tre volte il miglioramento osservato sulla faccetta piatta. Un’analisi dettagliata dei moti vibrazionali mostra che il legame O–H rivolto verso la superficie diventa significativamente più debole in presenza dell’ione ravvicinato, rendendolo più facile da rompere e accelerando così la formazione di idrogeno.
Una regola di progettazione per catalizzatori dell’idrogeno migliori
Complessivamente, lo studio conclude che la migliore prestazione nella produzione di idrogeno alcalino non deriva solo dalla superficie metallica o dall’elettrolita, ma dalla loro sinergia. I siti di platino a gradini che possono ancorare speciali cluster acqua–ione avvicinano i cationi alcalini, intensificano il campo elettrico locale, pre‑rompono parzialmente i legami d’acqua e accelerano fortemente il passo iniziale cruciale dell’evoluzione dell’idrogeno. Per il lettore non specialistico, il risultato pratico è che modellando con cura la forma microscopica delle superfici catalitiche e scegliendo elettroliti che portino gli ioni giusti nei punti giusti, gli ingegneri possono superare alcuni dei rallentamenti fondamentali dei dispositivi alcalini e progettare sistemi più efficienti e a risparmio energetico per la produzione di idrogeno pulito.
Citazione: Zhang, Q., Sun, P., Li, H. et al. Synergistic cation-facet effects boost alkaline hydrogen evolution kinetics on stepped Pt surfaces. Commun Chem 9, 113 (2026). https://doi.org/10.1038/s42004-026-01924-9
Parole chiave: evoluzione dell’idrogeno, elettrolisi alcalina, catalizzatore al platino, acqua interfaciale, cationi di metalli alcalini