Clear Sky Science · it
Base strutturale per la formazione di filamenti umani di RegⅢα
Come l’intestino combatte i germi
I nostri intestini sono continuamente esposti a miliardi di batteri, molti dei quali sono innocui o addirittura utili. Ma quando compaiono microrganismi pericolosi, il corpo ha bisogno di modi rapidi e precisi per attaccarli senza danneggiare i propri tessuti. Questo studio esamina da vicino una di queste protezioni naturali, chiamata RegIIIα, e rivela come cambi forma per uccidere i batteri e poi si trasformi in una forma più sicura e meno dannosa. Comprendere questo cambiamento di conformazione potrebbe aiutare gli scienziati a capire meglio come manteniamo l’equilibrio dei microbi intestinali e cosa va storto nelle malattie.
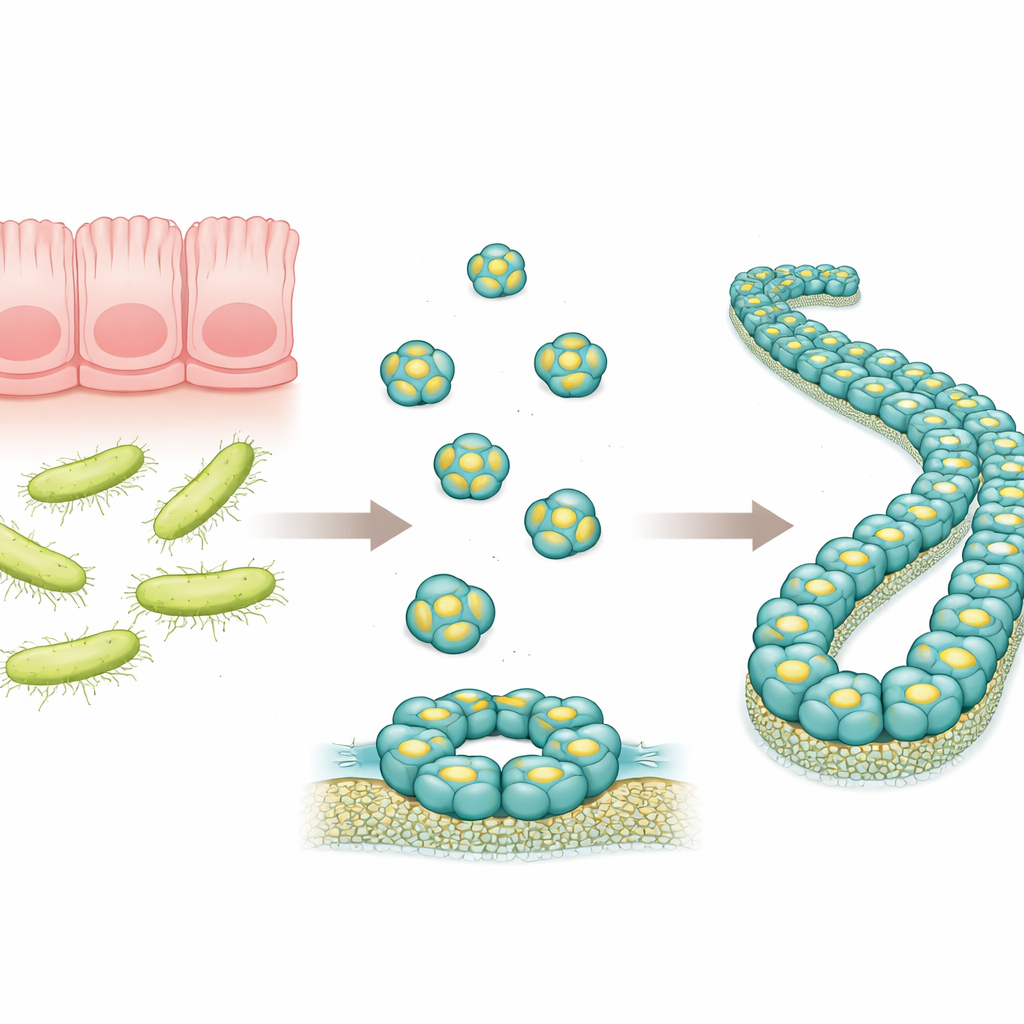
Un piccolo difensore nell’intestino
RegIIIα è una proteina prodotta nell’apparato digerente che prende di mira alcuni batteri, in particolare quelli con pareti esterne spesse note come batteri Gram-positivi. Studi precedenti suggerivano che RegIIIα possa perforare le membrane batteriche formando strutture ad anello, permettendo il fuoriuscire del contenuto microbico e portando alla morte del microrganismo. I ricercatori avevano inoltre osservato che, nel tempo, questi anelli possono impilarsi in lunghi filamenti, che sembrano ridurre il potere uccidente della proteina. Tuttavia, la precisa disposizione delle molecole di RegIIIα in questi assemblaggi maggiori non era nota nei dettagli, rendendo difficile comprendere come la proteina funzioni e come la sua attività sia regolata.
Osservare il filamento a risoluzione atomica
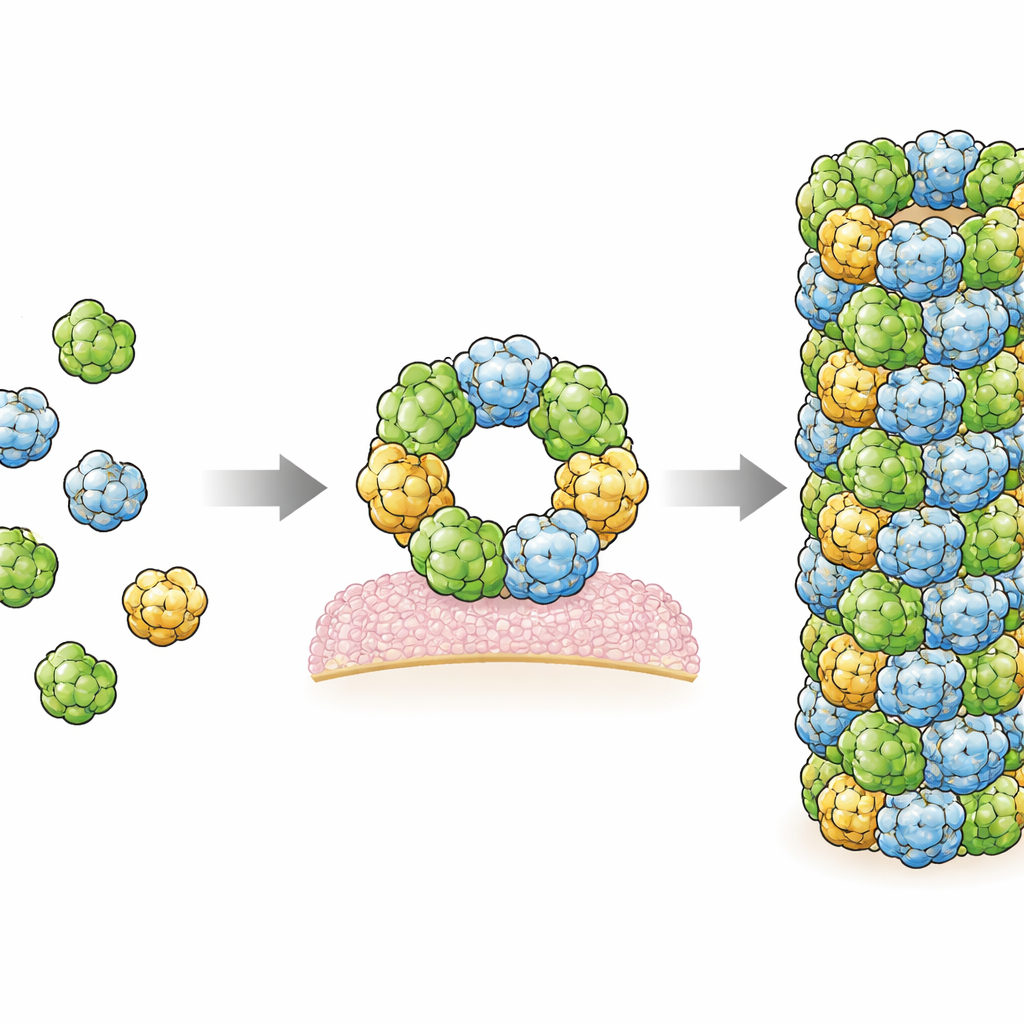
In questo lavoro gli autori hanno prodotto RegIIIα umano in batteri e hanno poi indotto la sua assemblaggio in filamenti in condizioni controllate. Hanno utilizzato un potente metodo di imaging chiamato crio-microscopia elettronica, che può visualizzare molecole biologiche congelate in uno strato sottile di ghiaccio a risoluzione prossima a quella atomica. Hanno scoperto che i filamenti sono costruiti da unità ripetute di tre identiche molecole di RegIIIα, chiamate trimetri, che si impilano secondo un regolare motivo elicoidale. Ogni singola molecola di RegIIIα appare molto simile a quanto osservato in precedenti strutture cristallografiche, ma la loro orientazione all’interno del filamento è diversa rispetto a un modello precedente a risoluzione più bassa. Questa correzione di orientamento cambia l’idea di come la proteina interagisca con le membrane batteriche e con il suo segmento regolatorio.
Come si legano le proteine e perché i lipidi contano
Esaminando la struttura in dettaglio, i ricercatori hanno identificato due principali regioni di contatto, o interfaccie, dove le molecole adiacenti di RegIIIα si toccano e mantengono il filamento insieme. Hanno quindi modificato specifici amminoacidi in queste interfaccie e hanno dimostrato che tali cambiamenti impediscono la formazione del filamento, confermando che questi siti di contatto sono essenziali. Interessante notare che, in entrambe le interfaccie, le mappe crio-EM mostravano regioni extra sfocate che probabilmente rappresentano piccole molecole allungate bloccate tra le superfici proteiche. La loro forma e l’ambiente chimico suggeriscono che possano essere lipidi, gli stessi tipi di molecole oleose che compongono le membrane cellulari. Questo supporta indizi precedenti secondo cui i lipidi aiutano a promuovere l’assemblaggio di RegIIIα, forse agendo come una colla molecolare che stabilizza le connessioni tra le subunità.
Il interruttore on–off: pH e un segmento nascosto
Il gruppo ha anche investigato cosa controlla quando RegIIIα può assemblarsi. Prima di diventare attiva, la proteina porta un breve “pro-segmento” che deve essere tagliato dagli enzimi digestivi. Nella loro struttura del filamento ad alta risoluzione non c’è spazio al centro dell’assemblaggio per ospitare questo pezzo aggiuntivo, il che implica che il pro-segmento impedisce la capacità di RegIIIα di formare gli anelli e i filamenti che perforano le membrane. Hanno osservato che la tendenza a formare filamenti dipende anche dall’acidità: i filamenti si formano facilmente a un pH simile a quello dell’intestino tenue ma meno a un pH più acido. Un singolo amminoacido, l’istidina 50, sembra agire come un interruttore sensibile al pH; quando viene sostituito con un altro residuo, la formazione del filamento diventa molto meno sensibile al pH. Queste caratteristiche — taglio enzimatica, legame ai lipidi e pH — creano insieme un sistema di controllo a più livelli che regola quando e dove RegIIIα è attivo.
Cosa significa per la salute intestinale
Nel complesso, questo lavoro fornisce l’immagine più dettagliata finora di come le molecole di RegIIIα si assemblano in strutture maggiori che collegano sia la loro azione antibatterica sia il loro comportamento autolimitante. Le stesse interfaccie che costruiscono i filamenti costruiscono anche gli anelli esamerici ritenuti responsabili della formazione di pori nelle membrane batteriche, suggerendo un equilibrio delicato tra una forma altamente letale e uno stato più sicuro e attenuato. Mappare le mutazioni associate a malattie su questa struttura mostra che molte ricadono in punti di contatto chiave, suggerendo che alterazioni nell’assemblaggio potrebbero essere alla base di alcuni disturbi intestinali o pancreatici. Chiarendo come questo antibiotico naturale viene attivato, guidato dai lipidi e modulato dal pH locale, lo studio pone le basi per futuri tentativi di modulare le nostre difese innate — sia potenziandole contro le infezioni sia attenuandole quando sono disfunzionali.
Citazione: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
Parole chiave: RegIIIα, immunità intestinale, crio-microscopia elettronica, filamenti proteici, peptidi antibatterici