Clear Sky Science · it
Glicosidi anfifilici ionizzabili giunzati con azobenzene per la somministrazione pDNA controllata dalla luce, a componente singola e modulabile per organi
Illuminare una consegna genica più intelligente
Le terapie geniche promettono di curare le malattie alla radice consegnando frammenti di codice genetico direttamente nelle nostre cellule. Ma guidare questo fragile carico in modo sicuro attraverso il flusso sanguigno, verso gli organi giusti e all’interno delle cellule bersaglio resta una sfida notevole. Questo studio presenta una nuova classe di particelle minute a base di zuccheri il cui comportamento può essere commutato con la luce prima ancora che entrino nel corpo, permettendo ai ricercatori di rimodulare dove finisce un gene terapeutico e quanto intensamente viene espresso, il tutto mantenendo le cellule per lo più intatte. 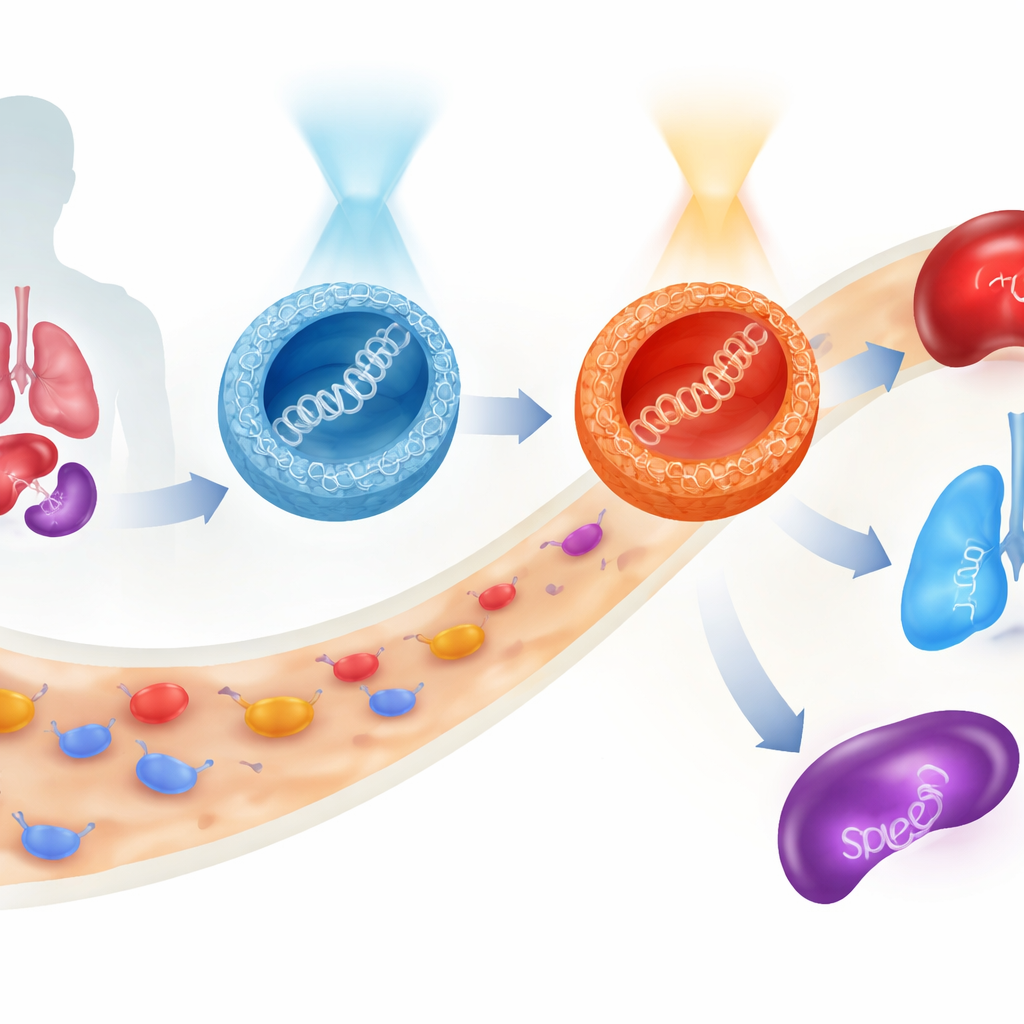
La necessità di corrieri genetici precisi
I veicoli di consegna genica più efficaci oggi sono le nanoparticelle lipidiche, che hanno reso possibili i vaccini a mRNA contro il COVID-19. Queste goccioline multi-componente avvolgono e proteggono gli acidi nucleici, ma tendono ad accumularsi principalmente nel fegato e rilasciano solo una piccola frazione del loro carico all’interno delle cellule. Modificare le loro composizioni può cambiare quali organi prediligono, tuttavia le miscele sono complesse e difficili da controllare con precisione. Il gruppo dietro questo lavoro ha quindi progettato molecole singole, ben definite, che si autoassemblano in nanoparticelle con forme e comportamenti prevedibili — e che possono essere regolate attivamente dall’esterno con un semplice impulso luminoso.
Una bilancia molecolare controllata dalla luce
Al centro del nuovo sistema ci sono due glicosidi «di Giunone» (Janus): molecole costruite da due unità di glucosio, dotate di teste cariche idrofile e code idrofobe, unite tramite un «perno» centrale di azobenzene. L’azobenzene può ruotare tra due conformazioni speculari, chiamate E e Z, quando è esposto a colori di luce diversi. In acqua, in presenza di DNA, molte copie di queste molecole si aggregano spontaneamente in particelle morbide e stratificate che avvolgono filamenti di DNA plasmidico. I ricercatori hanno preparato due varianti — una con ponti ossigeno e una con ponti zolfo tra lo zucchero e il perno — per modulare sottilmente stabilità e comportamento biologico. Pre-irraggiando le soluzioni, potevano arricchire la forma E o la forma Z e studiare come ciascuno stato influenzasse le particelle risultanti per la consegna genica.
Come si comportano le particelle che cambiano forma
Le misurazioni delle dimensioni delle particelle, della carica superficiale e della struttura interna hanno mostrato che il passaggio indotto dalla luce tra gli stati E e Z ha conseguenze fisiche nette. In generale, la forma Z generava nanoparticelle più piccole, di forma più uniforme e con un interno più ordinato e stratificato rispetto alla forma E. La microscopia ha rivelato che questi arrangiamenti interni somigliano a fogli alternati di materiale lipidico e DNA. Importante, entrambi gli stati proteggevano il DNA dalla degradazione enzimatica. In colture cellulari derivanti da rene, fegato e tessuto immunitario, i diversi isomeri hanno prodotto livelli di espressione genica sorprendentemente differenti, pur essendo il DNA sottostante identico. Impulsi luminosi ripetuti applicati dopo che le particelle erano entrate nelle cellule hanno aumentato l’espressione genica di diverse volte, suggerendo che lo scossone meccanico provocato dallo switching aiuti le particelle a allentarsi e rilasciare il loro carico, e possa anche facilitare la fuga da compartimenti intracellulari. 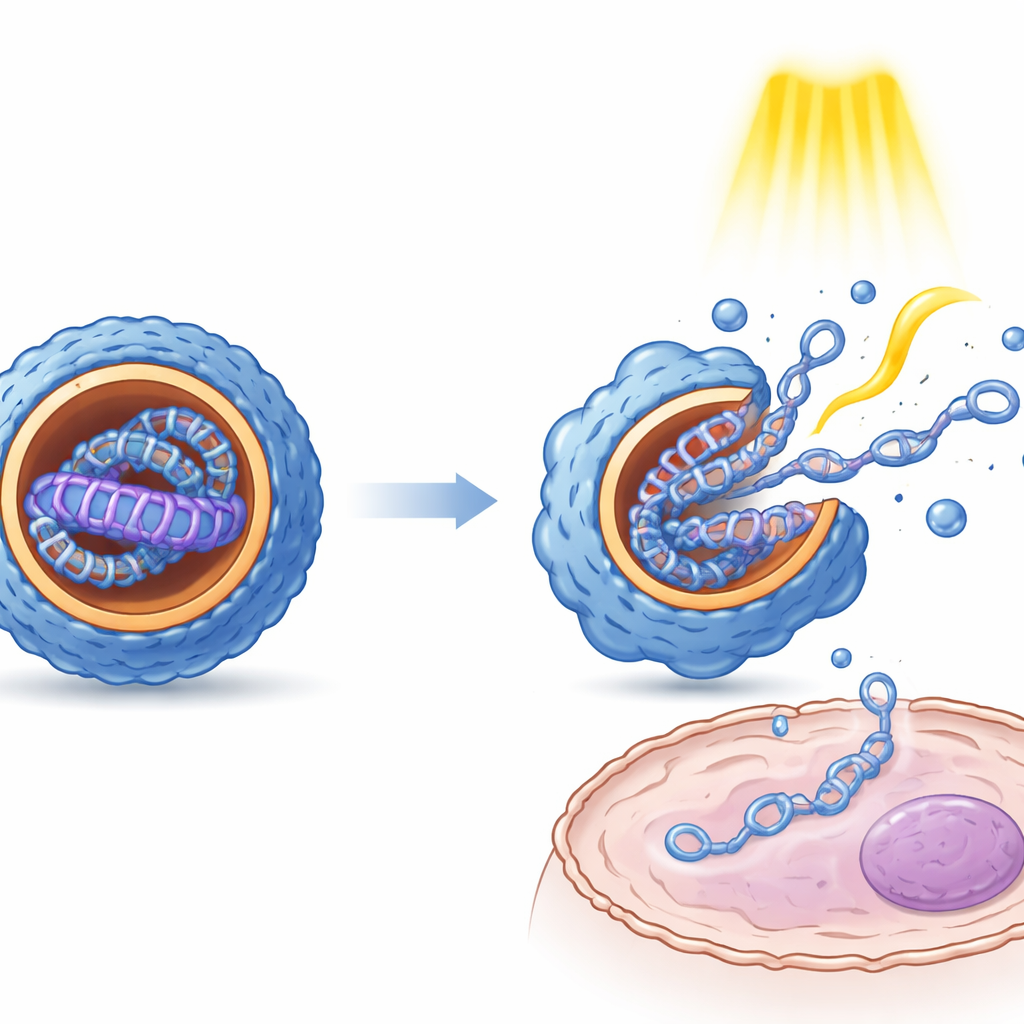
Indirizzare i geni verso organi specifici
Il comportamento più sorprendente è emerso nei topi. Quando le particelle con ponti ossigeno venivano somministrate nella loro forma ricca di E, l’espressione di un gene marcatore si verificava principalmente nel fegato con una componente nei polmoni. Pre-switcharle nella forma Z prima dell’iniezione non solo aumentava l’espressione totale, ma spostava anche l’equilibrio verso i polmoni. Le particelle con ponte zolfo raccontavano una storia diversa: la loro forma Z favoriva la milza, un organo immunitario chiave. Così, con lo stesso impianto molecolare di base — e senza cambiare il carico di DNA — i ricercatori potevano dirigere l’attività genica prevalentemente verso fegato, polmone o milza semplicemente scegliendo il legame (ossigeno o zolfo) e la forma attivata dalla luce (E o Z) del vettore. In tutti questi test, la vitalità cellulare è rimasta elevata, suggerendo che il sistema è relativamente delicato.
Una via modulabile dalla luce per le future medicine geniche
In termini pratici, il gruppo ha costruito un piccolo shuttle per DNA commutabile con la luce. Prima dell’iniezione, un breve trattamento luminoso «programma» gli shuttle in una delle due forme. Ogni forma si autoassembla in nanoparticelle con dimensioni e caratteristiche superficiali specifiche, che a loro volta determinano quanto fortemente aderiscano a diversi tipi cellulari e dove finiscono nell’organismo. Poiché lo stesso scaffold chimico può essere modificato in molti piccoli modi, e poiché lo switching è reversibile e non altera il DNA stesso, questa piattaforma offre un modo flessibile per affinare dove e come agiscono le terapie geniche. Pur restando molto lavoro da fare prima dell’uso clinico, lo studio dimostra che vettori a molecola singola progettati con cura e controllabili con la luce potrebbero diventare strumenti potenti per medicine genetiche più sicure e precise.
Citazione: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
Parole chiave: consegna genica, nanoparticelle sensibili alla luce, interruttori azobenzene, terapia del DNA mirata, nanomedicina