Clear Sky Science · it
La proteasi S9 WprP2 catalizza un taglio uniforme del peptide precursore nella biosintesi dei RiPP
Perché sono importanti gli «strumenti» di taglio nelle cellule
All’interno dei batteri, forbici molecolari specializzate tagliano lunghe catene di amminoacidi in frammenti più piccoli e attivi che spesso diventano antibiotici o altri prodotti naturali utili. Questo studio svela uno strumento di taglio finora sconosciuto — una proteasi chiamata WprP2 — che rifila il peptide bersaglio con precisione insolita. Capire come funziona questo enzima potrebbe aiutare gli scienziati a progettare nuovi peptidi bioattivi e antibiotici di nuova generazione.
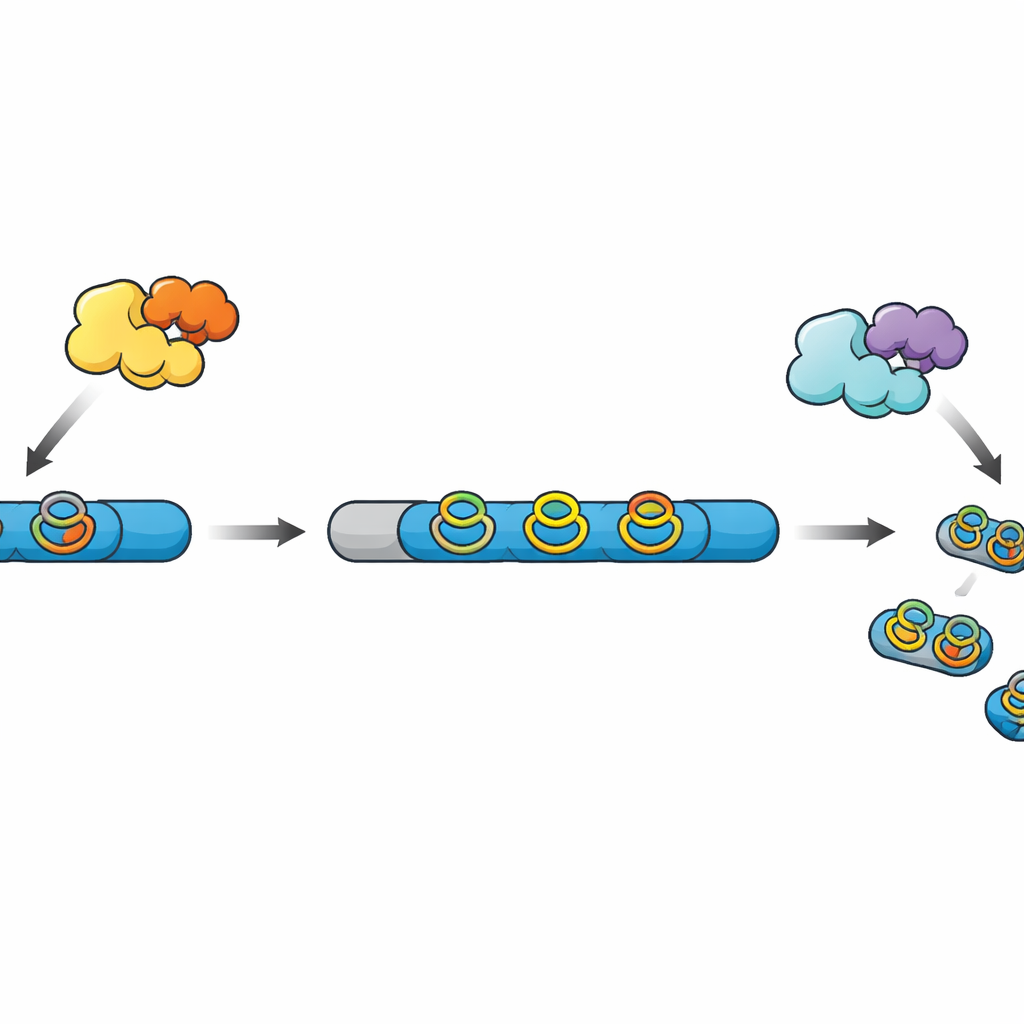
Dalle catene grezze ai mini‑medicinali finiti
Molti prodotti naturali a base di peptidi, noti collettivamente come RiPP, nascono come catene semplici sintetizzate dal ribosoma. Queste catene contengono una regione leader che funge da maniglia e una regione core che diventerà il prodotto finale dopo una serie di modifiche chimiche. Altri enzimi aggiungono legami incrociati e anelli che rendono il peptide più stabile e più attivo, e infine una proteasi taglia via il leader rilasciando la molecola matura. In una famiglia di RiPP recentemente scoperta, enzimi radical SAM costruiscono anelli compatti «ciclofani» che coinvolgono amminoacidi aromatici, ma nella maggior parte dei cluster genici noti la proteasi corrispondente manca, lasciando misteriosi gli ultimi passaggi di processamento.
Alla ricerca di un enzima partner scomparso
Gli autori avevano studiato in precedenza un enzima radical SAM chiamato WprB1 che installava legami identici in tre segmenti ripetuti WPR di un peptide precursore. Nel nuovo lavoro hanno cercato nei genomi batterici parenti di questo enzima e hanno controllato i geni vicini alla ricerca di potenziali proteasi. In Streptomyces venezuelae hanno individuato un cluster promettente contenente un enzima di crosslinking simile, la sua proteina ausiliaria, un peptide precursore corrispondente con tre ripetizioni WPR e una candidata serina proteasi della famiglia S9, che hanno chiamato WprP2. Questo sistema si è rivelato un banco di prova ideale per scoprire come il peptide viene infine tagliato per rilasciare i frammenti attivi.
Osservare il peptide mentre viene affettato
Per studiare WprP2, il gruppo ha prodotto il peptide precursore in batteri, sia con che senza l’enzima di crosslinking, lo ha purificato e poi lo ha miscelato con la proteasi in reazioni in vitro controllate. La spettrometria di massa ha rivelato che WprP2 prima tronca la catena immediatamente dopo ogni segmento WPR, e poi esegue un secondo taglio a una distanza fissa prima di una specifica prolina più avanti nella sequenza. Questi due passaggi generano una serie di frammenti più piccoli e uniformi. È notevole che WprP2 esegua questo schema di tagli sia che gli anelli ciclofano fossero già stati installati dall’enzima di crosslinking sia che non lo fossero, mostrando che gli anelli non sono necessari per il riconoscimento. Rispetto alla tripsina commerciale, che non può tagliare in alcuni siti crosslinkati, WprP2 ha continuato a funzionare, sottolineando la sua robustezza insolita.
Decifrare ciò che l’enzima riconosce
I ricercatori si sono poi chiesti quali caratteristiche del peptide WprP2 effettivamente legge. Modificando in modo sistematico singoli amminoacidi intorno ai siti di taglio, hanno scoperto che cambiare molti residui vicini aveva poco effetto, ma alterare un arginina chiave all’interno del segmento WPR o la glutamina o la prolina nel secondo sito di taglio poteva bloccare quel particolare passaggio. Esperimenti con un peptide precursore correlato contenente residui di flank diversi hanno mostrato che la proteasi continuava a tagliare dopo le ripetizioni WPR ma eseguiva il secondo taglio solo quando era presente una coppia glutammina‑prolina. Modelli strutturali generati al computer con AlphaFold3 hanno supportato questo quadro: nei complessi previsti, i siti basati su WPR e la coppia glutammina‑prolina si allineavano ciascuno a turno con il centro catalitico dell’enzima, coerente con un meccanismo sequenziale in due fasi.
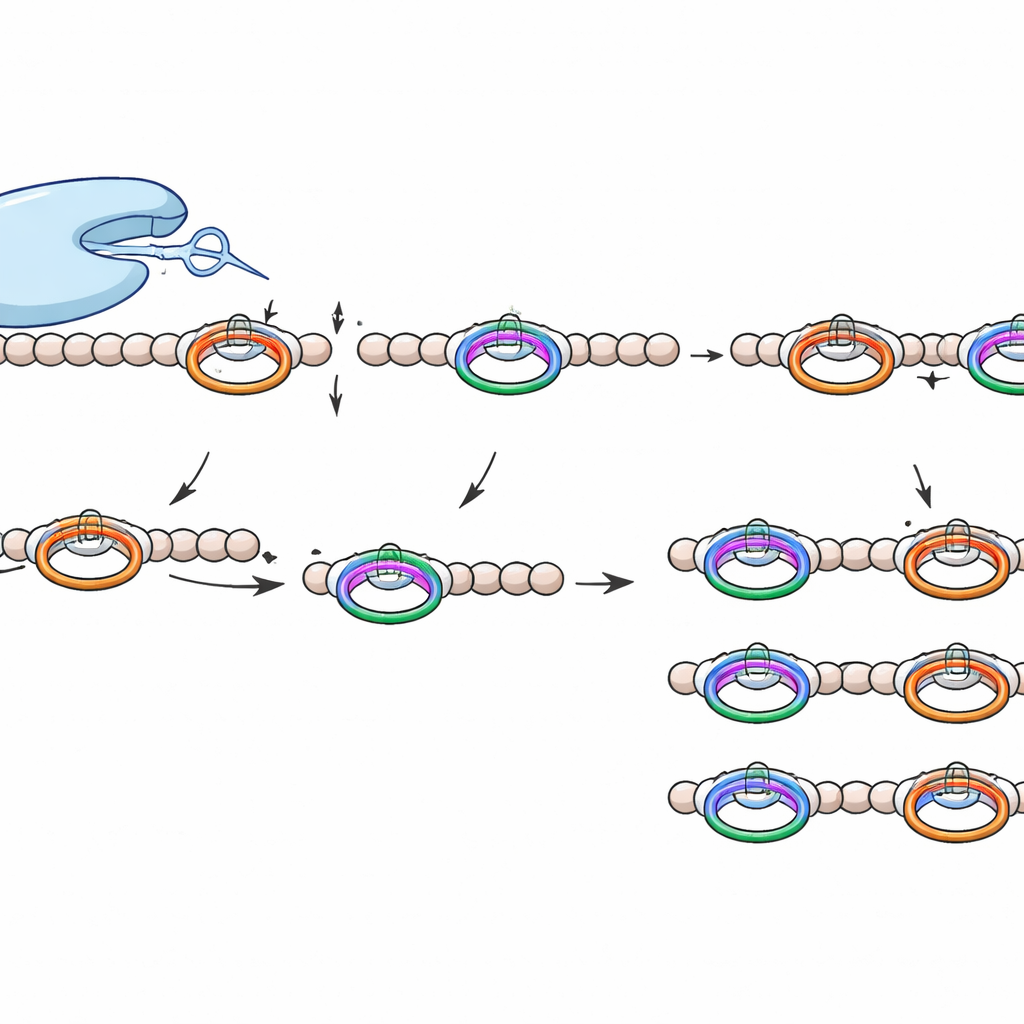
Cosa rende speciale questo strumento di taglio
WprP2 appartiene a una più ampia famiglia S9 di proteasi che include già enzimi rilevanti in ambito medico, ma si distingue per diversi aspetti. Taglia sul lato N‑terminale di una residuo di prolina anziché dopo di esso, agisce su un motivo ripetuto per generare frammenti di dimensioni regolari lungo l’intera catena precursore e mostra una vasta tolleranza agli amminoacidi che si trovano tra i suoi due siti di riconoscimento. Questa combinazione di precisione e flessibilità non era stata osservata prima nelle proteasi correlate ai RiPP.
Come potrebbe essere utilizzata questa scoperta
Svelando una proteasi che riconosce semplici segnali di sequenza ed esegue tagli ripetuti e uniformi, questo lavoro aggiunge un potente nuovo strumento al crescente arsenale per l’ingegneria peptidica. In termini pratici, WprP2 potrebbe essere sfruttata per rilasciare o rimodellare peptidi progettati, inclusi quelli con legami complessi che resistono a enzimi standard come la tripsina. Per i non specialisti, il messaggio chiave è che gli scienziati hanno scoperto un nuovo tipo di forbici molecolari che taglia lunghe catene peptidiche in pezzi precisi e di dimensioni uniformi, aprendo la strada a una produzione più controllata di potenziali antibiotici e di altre molecole bioattive.
Citazione: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
Parole chiave: peptidi RiPP, serina proteasi, WprP2, prodotti naturali ciclofani, ingegneria peptidica