Clear Sky Science · it
Sonda a emissione indotta da confinamento sterico per monitorare le conformazioni proteiche in cellule vive
Osservare le proteine che cambiano forma in tempo reale
All'interno di ogni cellula vivente, le proteine sono in continuo cambiamento strutturale mentre trasmettono segnali, percepiscono l'ambiente e svolgono funzioni essenziali. Molte malattie nascono quando questi cambiamenti di forma non avvengono correttamente, ma è stato finora notevolmente difficile osservare direttamente tali movimenti nelle cellule vive, specialmente su scale temporali sia molto veloci sia molto lente. Questo articolo presenta una nuova sonda luminosa, chiamata BIOSCE, che trasforma minuscoli movimenti delle proteine in lampi visibili, permettendo ai ricercatori di seguire singole proteine mentre si piegano, si torcono e interagiscono in tempo reale all'interno delle cellule vive. 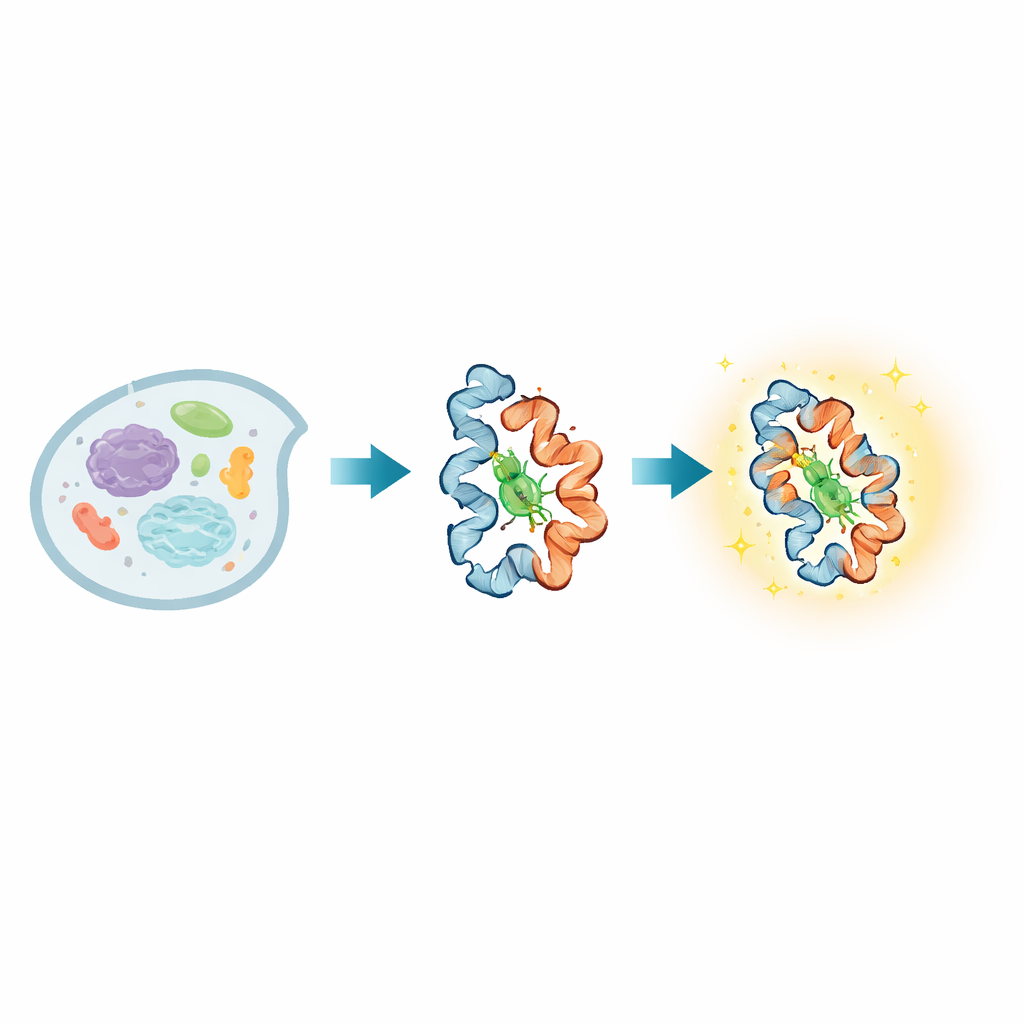
Un nuovo interruttore luminoso per proteine in movimento
Al centro di BIOSCE c'è una piccola molecola colorante, MTPABP-Cl, che diventa più luminosa quando viene compressa. I ricercatori legano questo colorante a un ampiamente usato tag proteico chiamato HaloTag, che può essere fuso geneticamente a quasi qualsiasi proteina di interesse. Quando la proteina marcata cambia forma o si avvicina ai vicini, altera lo “spazio” disponibile per il colorante per muoversi. In un ambiente meno vincolato le parti interne del colorante possono ruotare liberamente e gran parte della luce assorbita viene dissipata in movimento; in una tasca più stretta questi movimenti sono bloccati e il colorante rilascia invece più di quell'energia sotto forma di luce. Questa “emissione indotta da confinamento sterico” trasforma spostamenti sottili nella densità locale attorno a una singola proteina in un cambiamento fluido di luminosità, piuttosto che in un semplice segnale on–off, rendendo la sonda altamente sensibile a piccoli cambiamenti conformazionali.
Costruire e testare il colorante sensibile alla compressione
Il gruppo ha progettato e sintetizzato per primo MTPABP-Cl in modo che fosse tenue in soluzione ma si illuminasse quando trattenuto in posizione da HaloTag o da una proteina di fusione più compatta. Misure accurate hanno mostrato che il colorante assorbe luce blu ed emette in regione rosso-lontano, proprietà favorevoli per l'imaging profondo nelle cellule e per osservazioni a lungo termine. Quando legato solo a HaloTag, la sua emissione aumentava; quando HaloTag era fuso a una proteina partner che si richiudeva attorno al colorante, la luminosità aumentava ulteriormente. Simulazioni al computer hanno confermato che, in disposizioni proteiche più compatte, il colorante sperimenta un maggiore affollamento, una superficie esposta minore e contatti più stabilizzanti, tutti fattori che limitano il moto e aumentano l'emissione. Il colorante si lega inoltre in modo rapido e specifico a HaloTag, mostra un’attività di background molto bassa nelle cellule prive del tag e rimane non tossico alle concentrazioni operative, supportando il suo impiego in esperimenti su cellule vive. 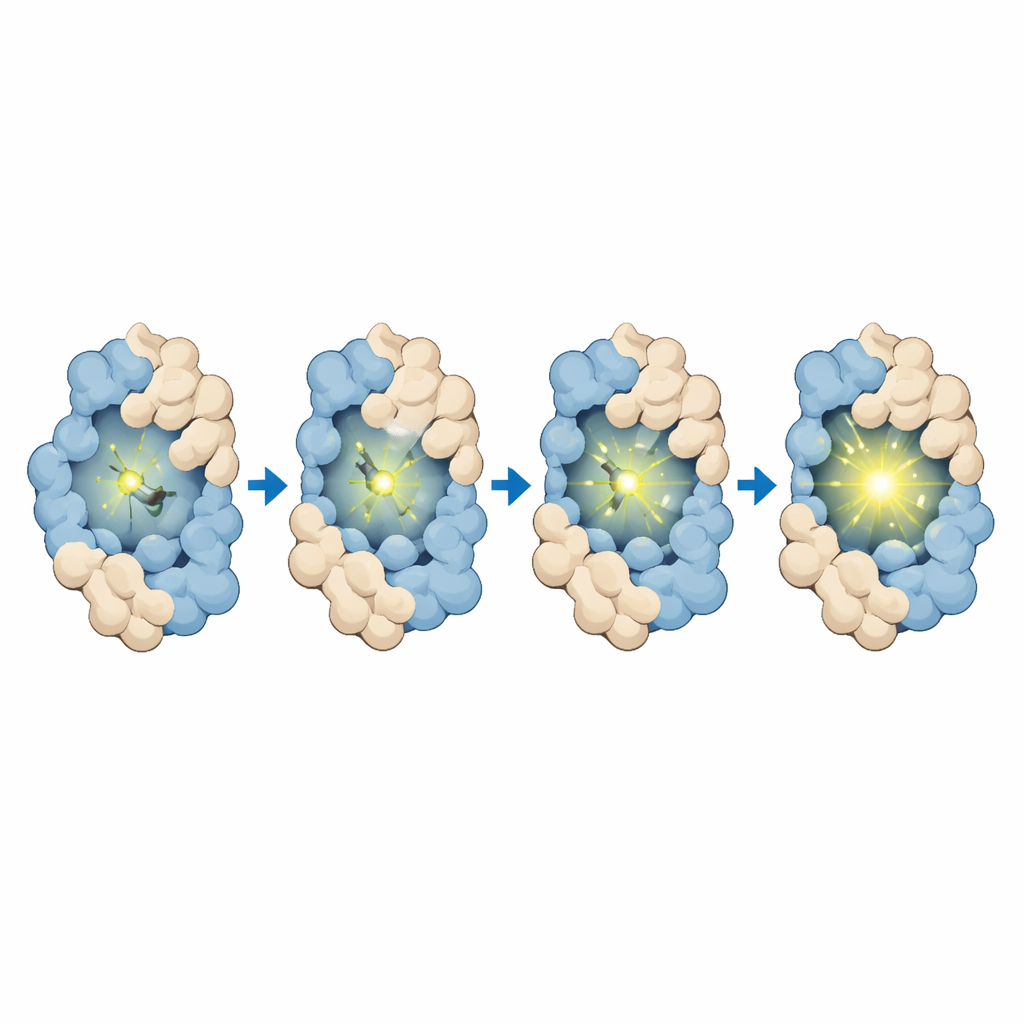
Seguire segnali rapidi e incontri proteici
Per dimostrare le capacità di BIOSCE, gli autori l'hanno applicata a diversi processi cellulari noti. Per prima cosa hanno adattato un sensore del calcio basato sulla calmodulina, una proteina che cambia forma quando lega ioni calcio, messaggeri centrali nell’attività neuronale e in molti altri eventi cellulari. Fondendo la calmodulina a HaloTag e marcandola con MTPABP-Cl, hanno creato un indicatore chemiogenetico chiamato SCECaMP. In cellule umane e in cellule di tipo neuronale, questo indicatore si è illuminato e attenuato in sincronia con i picchi di calcio indotti da stimolazione con potassio, con tempi di risposta paragonabili alle proteine fluorescenti GCaMP ampiamente usate. Poiché il segnale BIOSCE dipende direttamente dall’affollamento locale attorno al colorante, può rispecchiare fedelmente i cambiamenti strutturali della calmodulina offrendo al contempo una fluorescenza stabile e duratura adatta per imaging prolungato.
Osservare interazioni indotte da farmaci e danni da tossine
I ricercatori hanno poi verificato se BIOSCE potesse seguire il riavvicinamento di due proteine indotto da un farmaco. Hanno usato un sistema classico in cui la rapamicina avvicina due partner, FKBP e FRB, in una via di controllo della crescita. Attaccando HaloTag a FKBP o a FRB e marcando con MTPABP-Cl, hanno osservato rapidi aumenti di fluorescenza su scala di millisecondi mentre la rapamicina induceva l’avvicinamento e il riarrangiamento delle proteine. L’aumento di luminosità rifletteva un microambiente più compatto attorno al colorante man mano che i partner si avvicinavano. In una prova più complessa hanno studiato SNAP25, una proteina delle terminazioni nervose cruciale per il rilascio di neurotrasmettitori e principale bersaglio della neurotossina botulinica A. Posizionando HaloTag su entrambi i lati del sito di clivaggio della tossina e marcando con il colorante, hanno potuto tracciare separatamente i movimenti dei frammenti N-terminali e C-terminali dopo il taglio. Il tracciamento di singole particelle ha rivelato che un frammento restava ancorato vicino alla membrana cellulare, mentre l’altro diffondeva più liberamente nel citoplasma, e che il comportamento preciso dipendeva dal fatto che la marcatura fosse avvenuta prima o dopo l’esposizione alla tossina. La sonda ha persino segnalato rapidi ritocchi conformazionali indotti dallo zinco in SNAP25 durante questo processo.
Cosa significa per la biologia e la medicina
Nel complesso, questi risultati mostrano che BIOSCE è un nuovo strumento versatile per visualizzare come singole proteine si muovono, si ripiegano e interagiscono all’interno di cellule vive su un ampio intervallo di scale temporali. Poiché il metodo si basa su una fusione generale con HaloTag e su una singola piccola molecola colorante, può in linea di principio essere applicato a molte diverse proteine senza dover riprogettare l’intero sensore ogni volta. Il cambiamento continuo di luminosità dipendente dal confinamento permette ai ricercatori di rilevare spostamenti strutturali sottili invece di limitarsi a grandi eventi binari. Guardando al futuro, gli autori intendono migliorare la consegna della sonda e la profondità di imaging in modo che BIOSCE possa essere utilizzata in tessuti e organismi interi. Se questi sviluppi avranno successo, questo approccio potrebbe diventare uno strumento potente per collegare la localizzazione delle proteine, i loro movimenti e le loro funzioni in salute e malattia, e potrebbe infine alimentare modelli computazionali dettagliati del comportamento cellulare.
Citazione: Jia, H., Yang, L., Yang, Y. et al. Steric confinement-induced emission probe for monitoring protein conformations in live cells. Commun Chem 9, 109 (2026). https://doi.org/10.1038/s42004-026-01914-x
Parole chiave: dinamica conformazionale delle proteine, imaging in cellule vive, biosensori fluorescenti, sonde HaloTag, tossina botulinica